REVIEW
Tuberk Toraks 2020;68(1):66-75
Akciğer kanserinde immünoterapi ve tedavide multidisipliner yaklaşım
Nuri KARADURMUŞ1 , Akın KAYA2 , Tuncay GÖKSEL3 , Ülkü YILMAZ4 , Necla TÜLEK5
1Sağlık Bilimleri Üniversitesi Gülhane Eğitim ve Araştırma Hastanesi, Tıbbi Onkoloji Bölümü, Ankara, Türkiye.
1Department of Medical Oncology, Health Sciences University Gulhane Training and Research Hospital, Ankara, Turkey.
2Ankara Üniversitesi Tıp Fakültesi, Göğüs Hastalıkları Anabilim Dalı, Ankara, Türkiye.
2Department of Chest Diseases, Faculty of Medicine, Ankara University, Ankara, Turkey.
3Ege Üniversitesi Tıp Fakültesi, Göğüs Hastalıkları Anabilim Dalı, İzmir, Türkiye.
3Department of Chest Diseases, Faculty of Medicine, Ege University, Izmir, Turkey.
4Sağlık Bilimleri Üniversitesi Atatürk Göğüs Hastalıkları ve Göğüs Cerrahisi Sağlık Araştırma ve Uygulama Merkezi, Göğüs Hastalıkları Kliniği, Ankara, Türkiye.
4Department of Chest Diseases, Health Sciences University Atatürk Chest Diseases and Chest Surgery Health Research and Application Center, Ankara, Turkey.
5Atılım Üniversitesi Tıp Fakültesi, İnfeksiyon Hastalıkları ve Klinik Mikrobiyoloji Anabilim Dalı, İmmünoloji Bilim Dalı, Ankara, Türkiye.
5Division of Immunology, Department of Infectious Diseases and Clinical Microbiology, Faculty of Medicine, Atilim University, Ankara, Turkey.
Makale atıfı: Karadurmuş N, Kaya A, Göksel T, Yılmaz Ü, Tülek N. Akciğer kanserinde immünoterapi ve tedavide multidisipliner yaklaşım. Tuberk Toraks 2020;68(1):66-75.
ÖZ
Akciğer kanserinde immünoterapi ve tedavide multidisipliner yaklaşım
Akciğer kanseri dünya genelinde kanserle ilişkili ölümlerin başlıca nedeni olmaya devam etmektedir. Son 20 yılda kanser biyolojisi ve patogenezi hakkındaki bilgiler artmış, immün kontrol noktası inhibitörleri (İKNİ) kullanıma sunulmuş ve böylece solid kanserlerin tedavisinde önemli bir dönem başlamıştır. Bu derlemede; tedavide yenilikler, immünoterapi ve tedavide multidisipliner yaklaşım çerçevesinde akciğer kanseri ele alınmıştır. Küçük hücreli dışı akciğer kanseri (KHDAK) en sık görülen ve özellikleri nedeniyle İKNİ tedavisinden ideal olarak yararlanabilecek akciğer kanseri türü olması nedeniyle yazının odak noktasını oluşturmuştur. Bu derleme, akciğer kanseri tedavisinde immünoterapi yaklaşımının göğüs hastalıkları başta olmak üzere tüm branşlarda multidisipliner farkındalığını artırmayı ve yönetimi hakkında bilgi sağlamayı amaçlayan ilk Türkçe derlemedir. Ayrıca bu derleme, KHDAK tedavisinde İKNİ kullanımına ilişkin son klinik çalışmaların dikkat çekici sonuçlarını sunması açısından önem teşkil etmektedir. İmmünoterapi kanser tedavisinde yeni bir dönem başlatmıştır ve İKNİ tedavisinin kendine özgü etki mekanizması yeni bazı advers olay grubunun ortaya çıkmasına neden olmuştur, bunlar arasında pnömonitis özellikle önemlidir ve advers olaylar konusunda gerektiğinde hastaların ilgili uzmanlık dalları ile konsülte edilmesi gerekmektedir. Akciğer kanserinde tedavi, hastanın özellikleri, histolojik özellikler, genetik durum göz önünde bulundurularak her bir hastaya özel planlanmalı ve akciğer kanserli bir hastanın tanısal değerlendirilmesi ve en uygun şekilde tedavisi için göğüs hastalıkları, göğüs cerrahisi, tıbbi onkoloji, radyasyon onkolojisi, patoloji ve radyoloji uzmanlık dalları arasında işbirliği sağlanmalıdır. Bununla birlikte, aile hekimleri de akciğer kanserinin erken tanınmasında ve ayrıca hastalarını tütün bırakmayı teşvik ederek kanserin önlenmesinde önemli rol oynayabilirler. Ayrıca, toplumda farkındalık yaratmak ve erken tanı için akciğer kanseri yönünden tarama çalışmaları yapmak hedeflenmelidir.
Anahtar kelimeler: Akciğer kanseri; immünoterapi
ABSTRACT
Immunotherapy and multidisciplinary approach to treatment in lung cancer
Lung cancer remains as the main cause of cancer-related deaths worldwide. Over the last two decades, information about biology and pathogenesis of cancer has increased, immune checkpoint inhibitors (ICIs) have been introduced, and thus a significant period has started in treatment of solid cancers. This review discussed lung cancer in the framework of innovations in treatment, immunotherapy, and multidisciplinary approach to treatment. Non-small cell lung cancer (NSCLC) was the focal point of this article as it is the most frequent lung cancer type and the type of lung cancer which can ideally benefit from ICI treatment due to its characteristics. This review is the first review in Turkish language, which aimed to raise the multidisciplinary awareness about immunotherapy approach in lung cancer treatment in all branches, primarily in chest diseases, and to provide information about its management. Moreover, this review has importance as it presents the remarkable results of recent clinical trials on the use of ICIs in NSCLC treatment. Immunotherapy has initiated a new era in cancer treatment; the specific mechanism of action of ICIs has resulted in a group of some new adverse events, among which pneumonitis is particularly important and when necessary, patients are needed to be consulted with relevant specialties about adverse events. Lung cancer treatment should be planned specific to each patient by considering patient characteristics, histological features, and genetic status and specialty areas of chest diseases, thoracic surgery, medical oncology, radiation oncology, pathology, and radiology should collaborate together for diagnostic evaluation and optimal treatment of a lung cancer patient. Moreover, family physicians may have an important role in early diagnosis of lung cancer and in preventing lung cancer by encouraging their patients regarding tobacco cessation. Moreover, screening studies for lung cancer should be targeted to create awareness in society and for early diagnosis.
Key words: Lung cancer; immunotherapy
Geliş Tarihi/ Received: 25.02.2020 - Kabul Ediliş Tarihi/ Accepted: 05.03.2020
GİRİŞ
Akciğer kanseri dünya genelinde kanserle ilişkili ölümlerin başlıca nedenidir. Mortaliteyi azaltmada risk faktörlerinden kaçınmanın yanı sıra erken tanı ve tedavi büyük önem taşımaktadır. Son 20 yılda kanseri biyolojisi ve patogenezi hakkındaki bilgiler artmış, immün kontrol noktası inhibitörleri (İKNİ) kullanıma sunulmuş ve böylece solid kanserlerin tedavisinde önemli bir dönem başlamıştır (1). Kanser tedavisinde cerrahi, kemoterapi ve radyoterapiye ilave olarak “immünoterapi” dördüncü tedavi yöntemi olarak bu alanda yerini almıştır. Bu yazıda; tedavide yenilikler, immünoterapi ve tedavide multidisipliner yaklaşım çerçevesinde akciğer kanseri ele alınmıştır. Küçük hücreli dışı akciğer kanseri (KHDAK) en sık görülen ve özellikleri nedeniyle İKNİ tedavisinden ideal olarak yararlanabilecek akciğer kanseri türü olmasından dolayı yazının odak noktasını oluşturmuştur.
ETYOLOJİ ve EPİDEMİYOLOJİ
Akciğer kanseri dünya genelinde -sigara bırakma kampanyaları ve tedavideki gelişmelere rağmen- kanserle ilişkili ölümlerin başlıca nedeni olmaya devam etmektedir. Akciğer kanseri için dünya genelinde tüm yaş ve cinsiyet gruplarında 2018 yılında 2.1 milyon yeni olgu ve 1.8 milyon ölüm görüldüğü bildirilmektedir (2). Akciğer kanserinden ölümlerin 2035 yılı itibariyle 3 milyona ulaşacağı tahmin edilmektedir (3). Akciğer kanseri ülkemizde de en sık görülen kanser türüdür. Tüm yaş ve cinsiyet grupları dikkate alındığında kanserlerin %16.5’inden sorumludur ve 2018 yılında 34.703 yeni olgu görüldüğü bildirilmiştir (4).
Akciğer kanserinin etyolojisinde başta sigara/tütün kullanımı ve pasif maruziyeti olmak üzere akciğerin inflamatuvar/infeksiyon hastalıkları (fibrozis, kronik obstrüktif akciğer hastalığı, pnömoni, tüberküloz vb.), insan immünyetmezlik virüsü (HIV) infeksiyonu, çevresel ve mesleki ajanlara (kirli hava, radon, asbest, kömür vb.) maruziyet gibi çeşitli risk faktörleri rol oynamaktadır ((3),(5),(6)).
Akciğer kanseri erkeklerde daha sık görülmektedir. Bununla birlikte, nedeni hakkında farklı görüşler öne sürülse de bir gerçeklik olarak son yıllarda kadınlarda akciğer kanseri insidansında önemli bir artış olduğu rapor edilmektedir (5). En yüksek insidans hızının görüldüğü bölgeler erkekler için Orta ve Doğu Avrupa ve Doğu Asya iken kadınlar için Kuzey Amerika, Kuzey Avrupa, Avustralya/Yeni Zelanda ve kısmen Doğu Asya olarak bildirilmektedir. Orta ve Batı Afrika, erkek ve kadınlar için en düşük insidansın olduğu bölgelerdir (3).
Sigarayı bırakmak ve erken tanı ile cerrahi rezeksiyon akciğer kanseri mortalitesini azaltmada başlıca etkenlerdir (5). Tanı erken konulduğunda hastalarda sağkalım önemli oranda artmaktadır, bu nedenle bilgisayarlı tomografi (BT) ile akciğer kanseri için taramalar yapmanın yararlı olduğu önerilmektedir (3).
TANI ve SINIFLANDIRMA
Akciğer kanserinde en sık görülen semptomlar öksürük, nefes darlığı, hemoptizi ve sistemik (kilo kaybı ve anoreksi gibi) semptomlardır. Bu semptomlarla gelen yüksek riskli hastalarda göğüs radyografisi çekilmelidir. Alternatif bir tanı konulmayan durumlarda BT ve pozitron emisyon tomografisi uygulanmalı, akciğer kanseri şüphesi olanlarda tanısal değerlendirme yapılmalıdır. Eş zamanlı olarak doku incelemesi ile tanı, evrelendirme ve fonksiyonel değerlendirme yapılması hem tedaviyi planlamak hem de prognozu belirlemek için gereklidir. Akciğer kanserli bir hastanın tanısal değerlendirilmesi ve tedavisi göğüs hastalıkları, göğüs cerrahisi, tıbbi onkoloji, radyasyon onkolojisi, patoloji ve radyoloji uzmanlık dallarının dahil olduğu bir ekibin işbirliğini gerektirir (6). Aile hekimleri akciğer kanserinin erken tanınmasında ve ayrıca hastaların her başvurusunda tütün bırakmayı teşvik ederek kanserin önlenmesinde önemli rol oynayabilirler. Kanserin erken tanısı için yüksek riskli kişilerde düşük doz BT ile tarama yapılması önerilmektedir (6).
Akciğer kanseri histolojik olarak iki temel grupta sınıflandırılmaktadır ((7),(8)):
* Küçük hücreli dışı akciğer kanseri (KHDAK) olguların %85’ini oluşturur. KHDAK üç tip kanser içerir: adenokarsinomlar, skuamöz hücreli karsinomlar ve büyük hücreli karsinomlar.
Küçük hücreli akciğer kanseri (KHAK) olguların %15’ini oluşturur.
KHDAK için beş yıllık sağkalım hızı %18, metastatik veya ilerlemiş olanlar için %4 olarak oldukça düşük oranlarda bildirilmektedir (7). Tedavi edilmemiş metastatik KHDAK olan hastaların ortalama ömrü dört ila beş aydır (9). Dahası akciğer kanserli hastaların çoğu (yaklaşık %75’i) tanı aldıkları sırada ilerlemiş (Evre III/IV) hastalığa sahiptir. Erken evrede tanı konulabilirse KHDAK hastalarında iyi bir prognoz görülebilmektedir, küçük lokalize tümörlerde (Evre I) cerrahi rezeksiyon ile beş yıllık sağkalımlar %70’lere ulaşabilmektedir (10). Bu bilgiler, akciğer kanserinin erken tanı ve tedavisinin önemini bir kez daha vurgulamaktadır.
KHDAK hastalarından alınan örnekler çeşitli mutasyonlar için test edilmelidir. Bu mutasyonların saptanması tedavinin planlanması için gereklidir (6). Akciğer kanserinin moleküler özellikleri hakkındaki bilgilerin artması hedeflenmiş tedavilerin gelişimine olanak sağlamıştır. Akciğer adenokanserlerinde en sık görülen genetik değişiklikler EGFR (epidermal büyüme faktörü reseptörü) ve KRAS (Kirsten rat sarkoma viral onkogen homolog) mutasyonlarıdır. Daha az sıklıkta ALK (anaplastik lenfoma kinaz) gen yeniden düzenlemeleri, ROS1 (c-ros onkogen 1) translokasyonları, HER2 (human epidermal büyüme faktörü reseptör 2) mutasyonları, BRAF (B-Raf proto-onkogen) mutasyonları ve RET (Ret proto-onkogen) translokasyonları görülür (5). İmmün sistem ve kanser arasındaki karmaşık ilişkilerin daha iyi anlaşılması sonucu, bu alanda yapılan araştırmalarla spesifik hedefler belirlenmiştir. Bu hedeflere yönelik ilaçlar “immün kontrol noktası (checkpoint) inhibitörleri” (İKNİ) olarak bilinmektedir (11). Bu ilaçlar metastatik melanom ve böbrek kanserinde etkili bulunduktan sonra KHDAK tedavisinde de başarıyla uygulanmaya başlanmıştır. İKNİ, KHDAK’ta ilk seçenek veya ilk seçenek kemoterapi rejiminden sonra ikinci seçenek olarak klinik uygulamaya dahil edilmiştir (12). Standart kemoterapi ile ilk seçenek olarak karşılaştırıldıkları randomize çalışmalardan olumlu sonuçlar geldiği bildirilmiştir. Bununla birlikte yanıtlar seçilmemiş hastalarda daha az oranlarda olduğundan, etkinliği öngördüren faktörlerin belirlenmesine ihtiyaç olduğu düşünülmektedir (11).
AKCİĞER KANSERİ ve İMMÜN SİSTEM
İmmün sistem üç aşamada tümörle etkileşime girmektedir: i) yeni gelişen kanser hücreleri doğal ve adaptif bağışıklık mekanizmaları ile elimine edilir; ii) bu immün ataktan kaçan bazı hücreler eylemsiz bir duruma girer; iii) sonuç olarak bu hücreler immün kontrolden kaçabilir, çoğalabilir ve klinik olarak bir hastalığa yol açabilir. Başka bir deyişle, tümör, bazı immün kontrol noktalarından yararlanarak T hücrelerinin saldırısından kaçar (11). İmmün sistemin aktivasyonunda veya önlenmesinde rol oynayan stimülatör ve inhibitör sinyallerin tümüne birden “kontrol noktaları” denmektedir (13). İyi tanımlanmış kontrol noktaları arasında programlanmış hücre ölümü-1 (PD-1) reseptörü, ilgili ligandı (PD-L1) ve sitotoksik T-lenfosit antijen-4 (CTL4-A) yer almaktadır ((11),(13)). İmmün kontrol noktaları, T hücreleri için negatif bir sinyal üretir ve bu sinyal, proliferasyon, sitokin salınımı ve sitotoksik granüllerin salgılanması dahil olmak üzere T hücre fonksiyonunu azaltır. Böylece tümör büyür ve ilerler (7). Bu immün kontrol noktalarına yönelik etkili terapötik ajanlar olarak İKNİ kullanıma sunulmuş durumdadır. CTLA-4 sinyallemesini bloke eden monoklonal immünglobulin (Ig) G1 antikoru olan ipilimumab, malign melanomun tedavisi için onay almıştır. Pembrolizumab ve nivolumab (IgG4 monoklonal anti-PD-1 antikorları) ve atezolizumab (IgG1 monoklonal anti-PD-L1 antikoru), KHDAK için standart tedavi olarak ortaya çıkmıştır. Ek olarak, durvalumab ve avelumab, klinik çalışmalarda aktif olarak araştırılan anti-PD-L1 ajanlardır (7).
KHDAK, kanser genomundaki somatik mutasyonların göreceli olarak yüksek prevalansı nedeniyle İKNİ tedavisinden ideal olarak yararlanabilecek bir kanser türüdür. Tümör mutasyon yükü (tumor mutational burden, TMB), İKNİ’ye cevabın bir prediktörüdür ve KHDAK’ta diğer malignansilere göre TMB düzeyi daha yüksektir (13).
AKCİĞER KANSERİ TEDAVİSİNDE YENİLİKLER
Akciğer kanseri tedavi prensipleri dünyanın her yerinde aynı olmakla beraber epidemiyolojik özellikler, genetik varyasyonlar ve tedavi olanaklarına erişim farklılıkları hastalarda farklı sonuçlara neden olabilmektedir (3).
Platin bazlı kemoterapi ve hedefe yönelik tedavi dahil olmak üzere sistemik tedavi, evre IV KHDAK hastalarında standart tedavi olarak uygulanmaktadır. EGFR mutasyonu veya ALK gen yeniden düzenlemesi olan KHDAK hastalarında, epidermal EGFR-tirozin kinaz inhibitörleri (TKİ) ve ALK inhibitörleri gibi hedefe yönelik tedaviler, etkililik ve tolere edilebilirlikte dramatik iyileşmeler sağlamıştır. KHDAK moleküler yolaklarının daha iyi anlaşılması sonucu İKNİ kullanımı, KHDAK dahil çeşitli solid tümörlerde kalıcı yanıt oranları göstermiştir ve tedavide yeni bir dönem başlatmıştır (7).
İMMÜNOTERAPİ
İKNİ, son yıllarda solid tümörlerin yönetiminde en ümit verici tedavilerden biri olarak kullanıma girmiştir. KHDAK tedavisinde İKNİ kullanımına ilişkin son birkaç yılda dikkat çeken klinik çalışma sonuçları yayınlanmaktadır. PD-1 ve PD-L1 inhibitörlerinden nivolumab, pembrolizumab ve atezolizumabın KHDAK hastalarında genel sağkalım (overall survival, OS) üzerine olumlu etkileri gösterilmiş ve bu sonuçlar üzerine bu üç ilaç KHDAK tedavisinde kullanılmak üzere onay almıştır (14). Ancak, çalışmalarda hastaların uygunluk kriterlerindeki farklılık nedeniyle, onay koşulları da farklı olmuştur. Pembrolizumab onayı PD-L1 > %1 olan hastalarla sınırlı iken, nivolumab ve atezolizumab onayı PD-L1 durumundan bağımsız olarak verilmiştir. PD-L1 dışında EGFR ve sigara içme durumu da bu ajanların sağkalıma faydası üzerine etkide bulunabilecek faktörler olarak öne sürülmüştür (14). EGFR mutasyonlu KHDAK hastaları i3lk seçenek olarak TKİ ile tedaviden yarar görmektedir. Progresyon olduğunda seçenek kemoterapi veya İKNİ olabilir, ancak EGFR mutasyonunun immünoterapideki rolünün tam açıklığa kavuşmadığı ve bu hastalarda kemoterapi ile sağkalımın daha iyi göründüğü bildirilmiştir (15). İKNİ tedavisi ile ilgili halen sürdürülen birçok klinik çalışma bulunmaktadır. Bu çalışmaların uzun dönem sonuçları alındıkça hasta seçimi ve fayda-zarar durumları hakkında daha fazla bilgi sahibi olunacaktır. İKNİ tedavisinden yararlanma olasılığı yüksek olan hastaları seçmek için bazı biyobelirteçlerden yararlanılmaktadır. Bu biyobelirteçler hakkında aşağıda kısaca bilgi verilmiştir.
İMMÜNOTERAPİDE BİYOBELİRTEÇLER
PD-L1 ekspresyonu ve TMB; İKNİ tedavisinden yararlanma olasılığı yüksek olan hastaları seçmek için biyobelirteçler olarak kabul edilmektedir ((7),(16)-(18)). PD-L1 ekspresyon düzeyi en yaygın kabul görmüş biyobelirteçtir ((16),(17)). PD-L1 ekspresyonu yüksek olan hastalarda, düşük ekspresyon gösterenlere kıyasla immünoterapinin yararının anlamlı olarak daha yüksek olduğu bildirilmektedir. Bununla birlikte bazı hastalar PD-L1 ekspresyonu negatif olduğu halde İKNİ tedavisinden fayda görmektedir. Bu nedenle immünoterapinin etkisini öngörmede PD-L1 ekspresyonunun bağımsız bir biyobelirteç olarak kullanılması konusunda dikkatli olunması önerilmiştir (16). Kullanılan test ve sonuçların raporlanma ve yorumlanma şekli tedavi kararını etkileyebilir. PD-L1 ekspresyon düzeyini belirlemek için daha az hassas bir test kullanılması durumunda hastalar yanlış sınıflandırılabilir ve bu potansiyel olarak tedaviye uygunlukta farklılıklara neden olur (19).
Tümör mutasyon yükü yüksek olan hastalarda da İKNİ tedavisine yüksek cevap oranları görülmektedir. Bazı hastalarda TMB ile PD-L1 ekspresyon durumu arasında bir uyum olmadığı, TMB’nin tedaviye cevap için daha iyi bir prediktör olduğu öne sürülmüştür. Bununla birlikte yüksek maliyetli ve uzun süre alan bir test olması klinikte kullanımını sınırlamaktadır (16).
İmmünoterapinin etkisini öngörmede kullanılabilecek ancak henüz yeterince kanıt olmayan ve daha fazla çalışma verisine ihtiyaç duyulan başka belirteçler de bulunmaktadır. Bunlar arasında; MMR (mismatch-repair) eksikliği ve MSI (mikrosatellit-instabilite), EGFR/ALK, KRAS, TP53, tümör mikroçevresi, intestinal mikroflora, dolaşımdaki lenfosit sayısı, nötrofil/lenfosit oranı, laktat dehidrogenaz düzeyi vb. yer almaktadır ((16),(17)).
KLİNİK ÇALIŞMALAR
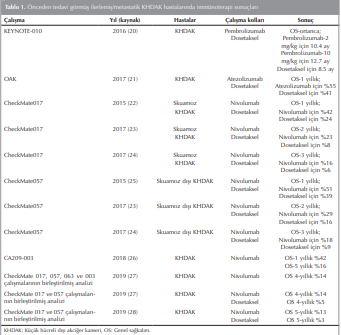
Önceden tedavi görmüş ilerlemiş/metastatik KHDAK hastalarında ikinci/üçüncü seride İKNİ tedavisinin kalıcı yanıt açısından etkileri birçok klinik çalışmada gösterilmiştir (13). Bu çalışmalardan bazı örnekler (Tablo 1)‘de özetlenmiştir. Uzun süreli sağkalımı araştırmak için randomize çalışmaların toplu analizine odaklanıldığında bu hasta popülasyonunda en uzun süreli OS verisi olan 4 yıllık OS nivolumab (ikinci basamak metastatik hastalıkta) için %14 ve dosetaksel için %5 bulunmuştur (27). Aynı hasta popülasyonunun beş yıllık takip verilerine göre ise nivolumab için beş yıllık OS oranı %13 ve dosetaksel için %3 bulunmuştur (28).
KHDAK tedavisinde kemoterapi-immünoterapi kombinasyonları ilk seçenek olarak da denenmeye başlanmıştır ((7),(14),(29)). Önceden tedavi almamış metastatik KHDAK hastalarında immünoterapinin kemoterapi olmaksızın ilk seçenek olarak kullanılması da söz konusudur (30). Erken evre rezeke edilebilir KHDAK hastalarında immünoterapi kullanımı ile ilgili çalışmalar sürmektedir (31). Devam eden birçok klinik çalışma bulunmaktadır ve bunların uzun dönem sonuçları ortaya çıktıkça İKNİ tedavisinin en uygun kullanımı hakkında daha fazla bilgi sahibi olunacaktır (32).
İKNİ tedavisi KHAK hastalarında da denenmektedir ((33),(34)). Amerikan Gıda ve İlaç Dairesi (FDA) Ağustos 2018’de nivolumab için platin bazlı kemoterapi ve en az bir diğer tedavi sonrası ilerlemiş metastatik KHAK’lı hastalarda kullanılmak üzere hızlandırılmış onay vermiştir ((35),(36)). Bununla birlikte FDA, Mart 2019’da atezolizumab için yaygın evre KHAK’lı erişkin hastaların birinci basamak tedavisinde karboplatin ve etoposit ile kombinasyon halinde kullanılmak üzere onay vermiş olup Haziran 2019’da ise pembrolizumab için platin bazlı kemoterapi ve önceki en az bir diğer tedavi sırasında veya sonrasında hastalığı ilerlemiş metastatik KHAK’lı hastaların tedavisinde kullanılmak üzere hızlandırılmış onay vermiştir ((37)-(40)).
İMMÜNOTERAPİDE GÜVENLİLİK
İKNİ tedavisinin kendine özgü etki mekanizması, yeni bazı advers olay grubunun ortaya çıkmasına neden olmuştur. Bu advers olay sınıfı vücuttaki hemen hemen her organı içerebilir. İKNİ ile tedaviler iyi tolere edilebilmekle beraber hayatı tehdit edici ciddi ve/veya geri dönüşümsüz advers olaylar da görülebilir. Hafif düzeyde immün-ilişkili advers olay varlığında yakın monitörizasyon ile tedavi sürdürülebilir. Ancak orta/ciddi düzey advers olaylar organ fonksiyonlarında ve yaşam kalitesinde ciddi azalmalara neden olabilir ve fatal sonuçlanabilir. Ciddi advers olaylar erken tanı ve tedavi gerektirir (41).
Akciğer kanserli hastalar arasında İKNİ ile tedavi sırasında özellikle ilgi çekici olan bir advers olay “pnömonitis”tir. Pnömonitis kliniği, hastalığın progresyonu ile ortaya çıkan klinik tablo ile karıştırılabilir. Nadir görülen bir advers olay olmakla beraber pnömonit sıklıkla ciddi seyredebilir ((14),(42)). Pnömonitis akciğerlerin inflamasyonunu ifade eden genel bir terimdir. İnfeksiyon sonucu oluşan inflamasyon pnömoni olarak ifade edilirken pnömonitis terimi infeksiyon dışı bir hastalık, radyasyon tedavisi, allerji, kimyasal irritasyon veya kanser tedavisinde kullanılan ilaçlar nedeniyle oluşan inflamasyon için kullanılmaktadır. İlaçla ilişkili pnömonitis doğrudan sitotoksik etki, oksidatif stres veya immün aracılı hasar sonucu ortaya çıkabilir (42).
Pnömonitis KHDAK hastalarında, diğer kanser türlerine (melanom, ürothelyal karsinom, baş ve boyun skuamöz hücreli kanser) kıyasla daha sık görülmektedir. KHDAK hastalarında (İKNİ ve kontrol kolundaki hastalar birlikte değerlendirildiğinde) ve diğer kanserler türlerinde insidans sırasıyla tüm grade pnömonitisler için %3.1 ve %2, yüksek grade pnömonitler için %1.4 ve %0.6 olarak bildirilmektedir. Ayrıca PD-1/PD-L1’i hedefleyen İKNİ tedavisi alan hastalarda kontrol kolundaki hastalara kıyasla pnömonitis gelişme riskinin herhangi bir grade için de (RR= 4.7) yüksek grade için de (RR= 3.3) anlamlı olarak daha fazla olduğu gösterilmiştir (43).
İKNİ ile tedavi sırasında görülebilecek advers olay ve toksisitelere yaklaşım açısından gerekli durumlarda konuya ilişkin algoritmaların yer aldığı kılavuzlara başvurulmalıdır. Brahmer ve arkadaşları İKNİ tedavisi alan hastalarda immün-ilişkili advers olaylar hakkında farkındalığı artırmak ve yönetimi konusunda rehberlik sağlamak amacıyla tıbbi onkoloji, dermatoloji, gastroenteroloji, romatoloji, pulmonoloji, endokrinoloji, üroloji, nöroloji, hematoloji, acil tıp, hemşirelik ve avukatlık konularında uzman kişilerin bir araya gelmesi ile klinik uygulama kılavuzu oluşturmak üzere multidisipliner bir çalışma yapmışlardır (41). Çalışmada, İKNİ ile tedavi sırasında ortaya çıkabilecek advers olay ve toksisitelerin spesifik organ/sistem temelinde tanısı ve yönetimi için öneriler sunulmuştur (41). Yönetim, etkilenen organ sistemine göre değişmekle birlikte, genel olarak grade 1 toksisiteler için (bazı nörolojik, hematolojik ve kardiyak toksisiteler hariç) yakın izleme ile İKNİ tedavisine devam edilmesi önerilmektedir. Grade 2 toksisitelerin çoğunda İKNİ tedavisi askıya alınabilir ve semptomların derecesi düştüğünde devam edilebilir, kortikosteroidler uygulanabilir. Grade 3 toksisiteler, genellikle İKNİ tedavisinin askıya alınmasını ve yüksek doz kortikosteroidlerin başlatılmasını gerektirir. Bazı dirençli olgular infliksimab veya başka bir immünsüpresif tedavi gerektirebilir. Grade 4 toksisitelerde, hormon replasmanı ile kontrol edilen endokrinopatiler hariç, genellikle İKNİ tedavisinin kalıcı olarak kesilmesi önerilir (41). İKNİ tedavisi sırasındaki olası advers olay/toksisiteler özet olarak Tablo 2’de gösterilmiştir. İKNİ ile tedavi edilmekte olan hastalarda özellikle advers olay/toksisite varlığında multidisipliner bir yaklaşımın gerekliliği aşikardır.
İKNİ ve dosetaksel tedavisinin karşılaştırıldığı klinik çalışmalarda Grade 3 veya 4 advers olay görülme sıklığının İKNİ alanlarda daha düşük oranlarda olduğu gösterilmiştir.
Xu ve arkadaşları ilerlemiş KHDAK hastalarında nivolumab ve dosetakseli karşılaştıran yayınları gözden geçirdikleri sistematik derleme ve meta-analiz çalışmalarında, progresyonsuz sağkalım (progression‐free survival, PFS), OS, objektif yanıt oranı, toplam advers olaylar ve grade 3-5 advers olaylar açısından nivolumabın dosetaksele göre daha iyi etkinlik ve güvenlilik gösterdiğini bildirmişlerdir (44). PFS ve OS açısından etkinlik PD‐L1 ekspresyon düzeyi ile pozitif olarak korele bulunmuştur. Nivolumab tedavi kolunda en fazla rapor edilen 10 advers olay, yorgunluk (%15.7), bulantı (%10.8), iştahsızlık (%10.3), asteni (%9.8), ishal (%7.5), döküntü (%7.5), artralji (%5.4), kusma (%4.4), kabızlık (%3.5) ve pireksi (%3.3) olarak bildirilmiştir. Zhao ve arkadaşları sistematik literatür taraması sonucu nivolumab tedavisinin ciddi ve fatal advers olay insidansını sırasıyla %11.2 ve %0.3 olarak bulmuşlardır (45). Konvansiyonel tedavi ile karşılaştırıldığında nivolumabın ciddi/fatal advers olayları artırmadığı bildirilmiştir. En sık görülen ciddi advers olayların solunum (%21.4), gastrointestinal (%7.7) ve hepatik sistemlerde (%6.6) meydana geldiği ve en sık görülen ciddi advers olayın pnömonit (%8.2), interstisyel akciğer hastalığı (%5.6) ve kolit (%3.6) olduğu bildirilmiştir.
MULTİDİSİPLİNER YAKLAŞIM
Akciğer kanserinin önlenmesi, erken tanısı ve tedavisinde göğüs hastalıkları uzmanları anahtar rol oynamaktadır. Göğüs hastalıkları, göğüs cerrahisi, palyatif bakım, radyasyon onkolojisi, tıbbi onkoloji, patoloji, radyoloji uzmanları arasında akciğer kanserinin tanı ve tedavisi için yakın işbirliği olmalıdır ((46),(47)). Bunun dışında yukarıda advers olay/toksisite yönetiminde gerektiğinde hemen her uzmanlık dalı ile konsültasyon gerekebileceğine değinilmiştir.
KHDAK hastalarında hastanın özellikleri, histolojik özellikler, genetik durum göz önünde bulundurularak tedavinin kişi bazında planlanması özellikle immünoterapinin kullanıma girmesiyle daha da önem kazanmıştır (47). Histolojik tanı için yeterli tümör dokusu örneğinin elde edilmesi, genomik profilin çıkarılması en iyi tedavi stratejisini oluşturmak için şarttır. Tanı için yapılan girişimlerden son tedavi aşamasına kadar olan süreçlerde yer alan tüm uzmanlar arasında işbirliği olması iyi sonuçlar almak açısından önem taşımaktadır (47).
SONUÇ ve ÖNERİLER
• Kanserle ilişkili ölümlerin başlıca nedeni olan
akciğer kanserine bağlı mortaliteyi azaltmada
erken tanı ve tedavi büyük önem taşımaktadır.
Kanserin erken tanısı için yüksek riskli kişilerde
düşük doz BT uygulaması için öncelikle ülkemiz
verilerini değerlendirmek üzere pilot çalışmalar
yapılmalıdır.
• İmmünoterapi kanser tedavisinde yeni bir dönem
başlatmıştır. KHDAK en sık görülen ve özellikleri
nedeniyle İKNİ tedavisinden ideal olarak yararlanabilecek akciğer kanseri türüdür.
• Hastaların özellikleri, histolojik özellikler, genetik durum göz önünde bulundurularak tedavi kişi
bazında planlanmalıdır. Akciğer kanserli bir
hastanın tanısal değerlendirilmesi ve en uygun
şekilde tedavisi için göğüs hastalıkları, göğüs
cerrahisi, tıbbi onkoloji, radyasyon onkolojisi,
patoloji ve radyoloji uzmanlık dalları arasında
işbirliği sağlanmalıdır.
• İKNİ tedavisinin kendine özgü etki mekanizması,
yeni bazı advers olay grubunun ortaya çıkmasına
neden olmuştur. Bunlar arasında pnömonitis
olabileceğinden göğüs hastalıkları uzmanlarının
farkındalığı artırılmalıdır. Advers olaylar konusunda dikkatli olunmalı gerektiğinde hasta ilgili
uzmanlık dalları ile konsülte edilmelidir. Advers
olay farkındalığını artırmak, hastanın herhangi
bir advers olay durumunda ilgili kişilere konsülte
edilmesini sağlamak ve advers olay yönetiminin
hızlı ve kolay uygulanabilmesi için hastalara
kullandıkları ilaçlarla ilgili olarak kimlik kartına
benzer hasta kartları sağlanmalı ve bu kartları
hastanın yanında taşıması gerekliliği konusunda
hastalar bilgilendirilmelidir. Hasta kartı örneği
(Tablo 3)’te sunulmuştur.
• Aile hekimleri akciğer kanserinin erken tanınmasında ve ayrıca hastaların her başvurusunda
tütün bırakmayı teşvik ederek kanserin önlenmesinde önemli rol oynayabilirler.
• Toplumda farkındalık yaratmak ve erken tanı için
akciğer kanseri yönünden tarama çalışmaları
yapmak hedeflenmelidir.
• Kanser Araştırmaları Enstitüsü (Cancer Research
Institute), yeni bir inisiyatif olarak, immünoterapinin hayat kurtarıcı potansiyeli hakkında farkındalık yaratmaya yardımcı olmaları için insanları
her yıl 14 Haziran’da kansere bağışık bir gelecek
için beyaz giymeye davet etmektedir (48).. Biz de
her yıl 14 Haziran’da hep beraber beyaz giyerek
Kanser Araştırmaları Enstitüsü’nün belirttiği gibi
bilimin ve immün tabanlı tedavi araştırmalarının
simgesi olabilir ve farkındalık yaratabiliriz.
TEŞEKKÜR
Omega Araştırma (Ankara, Türkiye) ve Ülke Medikal Direktörü Uzm. Dr. Devrim Emel Alıcı’ya (Bristol–Myers Squibb, İstanbul, Türkiye) makalenin yazımında bulunan katkılarından dolayı teşekkür ederiz.
KAYNAKLAR
- Naran K, Nundalall T, Chetty S, Barth S. Principles of immunotherapy: implications for treatment strategies in cancer and infectious diseases. Front Microbiol 2018;9:3158.
- Global Cancer Observatory (GCO). Cancer Today. Cancer Fact Sheet. Erişim tarihi: 13 Mart 2019. Available from: http://gco.iarc.fr/today/data/factsheets/cancers/15-Lung-fact-sheet.pdf.
- McIntyre A, Ganti AK. Lung cancer-A global perspective. J Surg Oncol 2017;115:550-4.
- Global Cancer Observatory (GCO). Cancer Today. Turkey Fact Sheet. Erişim tarihi: 13 Mart 2019. Available from: http://gco.iarc.fr/today/data/factsheets/populations/792-turkey-fact-sheets.pdf.
- Barta JA, Powell CA, Wisnivesky JP. Global epidemiology of lung cancer. Ann Glob Health 2019;85:pii: 8.
- Latimer KM, Mott TF. Lung cancer: Diagnosis, treatment principles, and screening. Am Fam Physician 2015;91:250-6.
- Lim SW, Ahn MJ. Current status of immune checkpoint inhibitors in treatment of non-small cell lung cancer. Korean J Intern Med 2019;34:50-9.
- Travis WD, Brambilla E, Nicholson AG, Yatabe Y, Austin JHM, Beasley MB, et al. The 2015 World Health Organization Classification of lung tumors: Impact of genetic, clinical and radiologic advances since the 2004 classification. J Thorac Oncol 2015;10:1243-60.
- Kanwal B, Biswas S, Seminara RS, Jeet C. Immunotherapy in advanced non-small cell lung cancer patients: ushering chemotherapy through the checkpoint inhibitors? Cureus 2018;10:e3254.
- Blandin Knight S, Crosbie PA, Balata H, Chudziak J, Hussell T, Dive C. Progress and prospects of early detection in lung cancer. Open Biol 2017;7:170070.
- Sánchez de Cos Escuín J. New immunotherapy and lung cancer. Arch Bronconeumol 2017;53:682-7.
- Wojas-Krawczyk K, Kalinka E, Grenda A, Krawczyk P, Milanowski J. Beyond PD-L1 markers for lung cancer immunotherapy. Int J Mol Sci 2019;20(8). pii: E1915.
- Barnet MB, Cooper WA, Boyer MJ, Kao S. Immunotherapy in non-small cell lung cancer: Shifting prognostic paradigms. J Clin Med 2018;7:E151.
- Abdel-Rahman O, Morris D. Immune checkpoint inhibitors and non-small-cell lung cancer management: 2018 update. Immunotherapy 2019;11:149-53.
- Cavanna L, Citterio C, Orlandi E. Immune checkpoint inhibitors in EGFR-mutation positive TKI-treated patients with advanced non-small-cell lung cancer network meta-analysis. Oncotarget 2019;10:209-15.
- Dong J, Li B, Zhou Q, Huang D. Advances in evidence-based medicine for immunotherapy of non-small cell lung cancer. J Evid Based Med 2018;11:278-87.
- Prelaj A, Tay R, Ferrara R, Chaput N, Besse B, Califano R. Predictive biomarkers of response for immune checkpoint inhibitors in non-small-cell lung cancer. Eur J Cancer 2019;106:144-59.
- Remon J, Hendriks LE, Cabrera C, Reguart N, Besse B. Immunotherapy for oncogenic-driven advanced non-small cell lung cancers: Is the time ripe for a change? Cancer Treat Rev 2018;71:47-58.
- Hirsch FR, McElhinny A, Stanforth D, Ranger-Moore J, Jansson M, Kulangara K, et al. PD-L1 Immunohistochemistry Assays for Lung Cancer: Results from Phase 1 of the Blueprint PD-L1 IHC Assay Comparison Project. J Thorac Oncol 2017;12:208-22.
- Herbst RS, Baas P, Kim DW, Felip E, Pérez-Gracia JL, Han JY, et al. Pembrolizumab versus docetaxel for previously treated, PD-L1-positive, advanced non-small-cell lung cancer (KEYNOTE-010): A randomised controlled trial. Lancet 2016;387:1540-50.
- Rittmeyer A, Barlesi F, Waterkamp D, Park K, Ciardiello F, von Pawel J, et al. Atezolizumab versus docetaxel in patients with previously treated non-small-cell lung cancer (OAK): A phase 3, open-label, multicentre randomised controlled trial. Lancet 2017;389:255-65.
- Brahmer J, Reckamp KL, Baas P, Crinò L, Eberhardt WE, Poddubskaya E, et al. Nivolumab versus Docetaxel in advanced squamous-cell non-small-cell lung cancer. N Engl J Med 2015;373:123-35.
- Horn L, Spigel DR, Vokes EE, Holgado E, Ready N, Steins M, et al. Nivolumab versus Docetaxel in previously treated patients with advanced non-small-cell lung cancer: Two-Year outcomes from two randomized, open-label, phase III trials (CheckMate 017 and CheckMate 057). J Clin Oncol 2017;35:3924-33.
- Felip Font E, Gettinger SN, Burgio MA, Antonia SJ, Holgado E, Spigel DR, et al. Three-year follow-up from CheckMate 017/057: Nivolumab versus docetaxel in patients with previously treated advanced non-small cell lung cancer (NSCLC). Ann Oncol 2017;28(Suppl 5).
- Borghaei H, Paz-Ares L, Horn L, Spigel DR, Steins M, Ready NE, et al. Nivolumab versus Docetaxel in advanced nonsquamous non-small-cell lung cancer. N Engl J Med 2015;373:1627-39.
- Gettinger S, Horn L, Jackman D, Spigel D, Antonia S, Hellmann M, et al. Five-year follow-up of Nivolumab in previously treated advanced non-small-cell lung cancer: Results from the CA209-003 study. J Clin Oncol 2018;36:1675-84.
- Brahmer J, Borghaei H, Ramalingam SS, Horn L, Holgado E, Pluzanski A, et al. Long-term survival outcomes with nivolumab (NIVO) in pts with previously treated advanced non-small cell lung cancer (NSCLC): Impact of early disease control and response [abstract]. Proceedings of the 110th Annual Meeting of the American Association for Cancer Research; 2019 Mar 29-Apr 3; Atlanta, GA, USA. Philadelphia (PA): AACR; 2019. Abstract 19-LB-7988-AACR.
- Gettinger S, Borghaei H, Brahmer J, Chow LQM, Burgio MA, de Castro Carpeno J, et al. Pooled analysis of checkmate 017 and 057: 5-year outcomes with nivolumab vs docetaxel in previously treated NSCLC. Presented at: IASLC 2019 World Conference on Lung Cancer hosted by the International Association for the Study of Lung Cancer; September 7-10, 2019; Barcelona, Spain. Abstract OA14.04.
- Shafique M, Tanvetyanon T. Immunotherapy alone or chemo-immunotherapy as front-line treatment for advanced non-small cell lung cancer. Expert Opin Biol Ther 2019;19:225-32.
- Martinez P, Peters S, Stammers T, Soria JC. Immunotherapy for the first-line treatment of patients with metastatic non-small cell lung cancer. Clin Cancer Res 2019;25:2691-8.
- Ghysen K, Vansteenkiste J. Immunotherapy in patients with early stage resectable nonsmall cell lung cancer. Curr Opin Oncol 2019;31:13-7.
- Nadal E, Massuti B, Dómine M, García-Campelo R, Cobo M, Felip E. Immunotherapy with checkpoint inhibitors in non-small cell lung cancer: Insights from long-term survivors. Cancer Immunol Immunother 2019;68:341-52.
- Calles A, Aguado G, Sandoval C, Álvarez R. The role of immunotherapy in small cell lung cancer. Clin Transl Oncol 2019;21:961-76
- Lehman JM, Gwin ME, Massion PP. Immunotherapy and targeted therapy for small cell lung cancer: There is hope. Curr Oncol Rep 2017;19:49.
- U.S. Food and Drug Administration. Erişim tarihi: 16.07.2019. Available from: https://www.fda.gov/drugs/resources-information-approved-drugs/fda-grants-nivolumab-accelerated-approval-third-line-treatment-metastatic-small-cell-lung-cancer.
- Antonia SJ, López-Martin JA, Bendell J, Ott PA, Taylor M, Eder JP, et al. Nivolumab alone and nivolumab plus ipilimumab in recurrent small-cell lung cancer (CheckMate 032): a multicentre, open-label, phase 1/2 trial. Lancet Oncol 2016;17:883-95.
- U.S. Food and Drug Administration. Erişim tarihi: 16.07.2019. Available from: https://www.fda.gov/drugs/drug-approvals-and-databases/fda-approves-atezolizumab-extensive-stage-small-cell-lung-cancer
- Horn L, Mansfield AS, Szczesna A, Havel L, Krzakowski M, Hochmair MJ, et al. First-line atezolizumab plus chemotherapy in extensive-stage small-cell lung cancer. N Engl J Med 2018;379:2220-9.
- U.S. Food and Drug Administration. Erişim tarihi: 16.07.2019. Available from: https://www.fda.gov/drugs/resources-information-approved-drugs/fda-approves-pembrolizumab-metastatic-small-cell-lung-cancer
- Ott PA, Elez E, Hiret S, Kim DW, Morosky A, Saraf S, et al. Pembrolizumab in patients with extensive-stage small-cell lung cancer: results from the Phase Ib KEYNOTE-028 Study. J Clin Oncol 2017;35:3823-9.
- Brahmer JR, Lacchetti C, Schneider BJ, Atkins MB, Brassil KJ, Caterino JM, et al. Management of immune-related adverse events in patients treated with immune checkpoint inhibitor therapy: American Society of Clinical Oncology Clinical Practice Guideline. J Clin Oncol 2018;36:1714-68.
- Nishino M, Hatabu H, Hodi FS, Ramaiya NH. Drug-related pneumonitis in the era of precision cancer therapy. Precis Oncol 2017. Epub 2017 May 26.
- Ma K, Lu Y, Jiang S, Tang J, Li X, Zhang Y. The relative risk and incidence of immune checkpoint inhibitors related pneumonitis in patients with advanced cancer: A meta-analysis. Front Pharmacol 2018;9:1430.
- Xu Z, Yi F, Yu D, Xu J, Wei Y, Zhang W. Nivolumab provides improved effectiveness and safety compared with docetaxel as a second-line treatment for advanced non-small cell lung cancer: A systematic review and meta-analysis. Cancer Med 2019;8:629-42.
- Zhao B, Zhao H, Zhao J. Serious adverse events and fatal adverse events associated with nivolumab treatment in cancer patients: Nivolumab-related serious/fatal adverse events. J Immunother Cancer 2018;6:101.
- Gaga M, Powell CA, Schraufnagel DE, Schönfeld N, Rabe K, Hill NS, et al. An official American Thoracic Society/European Respiratory Society statement: The role of the pulmonologist in the diagnosis and management of lung cancer. Am J Respir Crit Care Med 2013;188:503-7.
- De Marinis F, Barberis M, Barbieri V, Marchianò A, Gasparini S, Migliorino MR, et al. Diagnosis and first-line treatment of non-small cell lung cancer in the era of novel immunotherapy: Recommendations for clinical practice. Expert Rev Respir Med 2019;13:217-28.
- Cancer Research Institute. Erişim tarihi: 27.06.2019. Available from: https://www.cancerresearch.org/join-the-cause/cancer-immunotherapy-month/wear-white-day).
Yazışma Adresi (Address for Correspondence)
Dr. Nuri KARADURMUŞ
Sağlık Bilimleri Üniversitesi Gülhane Eğitim ve Araştırma Hastanesi,
Tıbbi Onkoloji Bölümü,
ANKARA - TÜRKİYE
E-mail: drnkaradurmus@yahoo.com