REVIEW
Doi: 10.5578/tt.50748
Tuberk Toraks 2017;65(2):117-130

T?rk Toraks Derneği ulusal spirometri ve laboratuvar standartları
Gaye ULUBAY1, Nurdan K?KT?RK2, Aslı G?REK DİLEKTAŞLI3, Elif ŞEN4, Fatma ?İFTCİ4, Tun?alp DEMİR5, ?znur YILDIZ4, Bilun GEMİCİOĞLU5, Sevgi SARYAL4
1 Başkent ?niversitesi Tıp Fak?ltesi, G?ğ?s Hastalıkları Anabilim Dalı, Ankara, T?rkiye
1 Department of Chest Diseases, Faculty of Medicine, Baskent University, Ankara, Turkey
2 Gazi ?niversitesi Tıp Fak?ltesi, G?ğ?s Hastalıkları Anabilim Dalı, Ankara, T?rkiye
2 Department of Chest Diseases, Faculty of Medicine, Gazi University,?? Ankara, Turkey
3 Uludağ ?niversitesi Tıp Fak?ltesi, G?ğ?s Hastalıkları Anabilim Dalı, Bursa, T?rkiye
3 Department of Chest Diseases, Faculty of Medicine, Uludag University, Bursa, Turkey
4 Ankara ?niversitesi Tıp Fak?ltesi, G?ğ?s Hastalıkları Anabilim Dalı, Ankara, T?rkiye
4 Department of Chest Diseases, Faculty of Medicine, Ankara University,?? Ankara, Turkey
5 İstanbul ?niversitesi Cerrahpaşa Tıp Fak?ltesi, G?ğ?s Hastalıkları Anabilim Dalı, İstanbul
5 Department of Chest Diseases, Cerrahpasa Faculty of Medicine, Istanbul University, Istanbul, Turkey
?ZET
T?rk Toraks Derneği ulusal spirometri ve laboratuvar standartları
Solunum fonksiyon testlerinin (SFT) uygulanma kalitesi verilen sağlık hizmetlerinin kalitesini etkilemesi nedeni ile b?y?k ?nem taşır. 2013 yılında yayınlanan "T?rkiye Kronik Hastalıklar ve Risk Fakt?rleri ?alışması" ?lkemizde ikinci basamak sağlık kurumlarında yapılan SFT'lerin sadece %22.6'sının kriterlere uygun olduğunu g?stermiştir. Bu sonu? ?lkemizdeki spirometre uygulamalarında yaşanan standardizasyon sorununu ortaya koymaktadır. G?n?m?zde spirometre ?l??mlerinin uygulama ve yorumlama nitelik g?vencesi "American Thoracic Society(ATS)/European Respiratory Society (ERS)"? standartları ile belirlenmiştir. D?nyada olduğu gibi ?lkemizde de bir?ok laboratuvar bu standartları kullanmaktadır. Ancak g?n?m?ze dek ?lkemiz koşullarına uygun olarak d?zenlenmiş ulusal laboratuvar standartları hen?z tanımlanmamıştır. Bu rapor, ?lkemizde en yaygın kullanılan solunum fonksiyon testi y?ntemi olan spirometrenin en uygun koşullarda yapılmasını sağlamak ve laboratuvar i?i-laboratuvarlar arası farklılıkları, hataları en aza indirgemek ve standardize edebilmek amacı ile hazırlanmıştır. Raporda laboratuvar koşulları, cihaz ve teknisyen ?zellikleri, test uygulanışı ve test kalitesinin değerlendirilmesi, infeksiyon kontrol? ve referans değerlere y?nelik standartlar ?zerinde durulmuştur.
Anahtar kelimeler: Spirometre, laboratuvarlar, kılavuz
SUMMARY
Turkish Thoracic Society national spirometry and laboratory standards
The application quality of pulmonary function tests (PFT) carries high importance since it affects the quality of health services. "Chronic Diseases and Risk Factors in Turkey Study," which was published in 2013 showed that only 22.6% of PFTs performed in the secondary care institutions in our country were compatible with the standards. This finding reveals the standardization problem in spirometry applications in our country.? Currently, the criteria for the application and evaluation of spirometer measurements were defined by American and European Respiratory Societies standards. Several laboratories use these standards in our country as in the world. But, national laboratory standards that are suitable for the conditions in our country have not been defined yet. This report was prepared to ensure the application of spirometry in optimal conditions, to minimize intra-laboratory and inter-laboratory differences and mistakes, and to standardize in our country. In this report, we focused on the standards concerning laboratory conditions, equipment, and technician specifications, test application, evaluation of test quality, infection control, and reference values.
Key words: Spirometry,? laboratories, guideline
Geliş Tarihi/Received: 20.02.2017 - Kabul Ediliş Tarihi/Accepted: 27.02.2017
LABORATUVARIN FİZİKİ KOŞULLARI
Rahat, geniş (havalandırılabilen, g?n ışığı alan, sessiz bir ortam), nem ve ısı a?ısından aşağıda tanımlanan standartlara uygun bir oda olmalıdır.
Ortam ısısı 17-40?C, tercihen 20-24?C, nem ise %40-60 arasında olmalı, barometrik basın? g?nl?k ?l??l?p kaydedilmelidir. G?n?m?zde bu basamaklar bir?ok cihaz tarafından otomatik kaydedilmektedir (1,2).
BTPS: ?l??m sonu?larının v?cut ısısı, atmosfer basıncı ve hava yolundaki doymuş su buharına ayarlanmasıdır. B?t?n spirometrik ?l??mler BTPS şartlarında raporlanmalıdır. Ekspire edilen havanın akım sens?r?nden ge?erken soğuması, kullanılan bakteri filtreleri ve akım sens?r ?zerinde biriken nem, BTPS d?zeltme fakt?r?nde %10 yanılmaya sebep olabilir, bu nedenle bu d?zeltmelerin yapılması tercih edilir. G?n?m?zde bu d?zeltmeler bir?ok cihaz tarafından otomatik olarak yapılmaktadır (3).
CİHAZ STANDARTLARI
Solunum fonksiyon testi (SFT) laboratuvarı farklı testlerin yapıldığı bir laboratuvardır. Bu testler; arter kan gazları ?l??m?, spirometri, akciğer vol?mlerinin gazlı testlerle ?l??m?, pletismografi, dif?zyon kapasitesi ?l??m?, egzersiz testi (kardiyopulmoner egzersiz testi-KPET) ve alan testleridir. Her solunum fonksiyon laboratuvarında en azından bir spirometre cihazı gereklidir. Hazırlanan bu raporda ?lkemizde en yaygın kullanılan spirometrik incelemeye y?nelik gerekli standartların ?ncelikli olarak hazırlanması ama?lanmıştır.
Spirometreler
SFT laboratuvarındaki olmazsa olmaz cihazlardan olan spirometrelerin pek ?ok tipi bulunduğundan se?im yaparken doğru olanı bulmak ?nemlidir. "European Respiratory Society (ERS)" ve "American Thoracic Society (ATS)" kriterlerine uygun olan spirometreler tercih edilmelidir. Bu cihazlarla ?l??len değerlerin g?venle kullanılabilmesi i?in doğruluk, tekrarlanabilirlik, ?retilebilirlik, ?l??m aralığı ve rezol?syon gibi ?zellikler tanımlanmıştır (3,4).
Doğruluk: Cihazın ?l?t?ğ? değer ile ger?ek değer arasında uyum olmasıdır. ?rneğin; bir hastada 3 L olan vital kapasitenin aynı hastada her ?l??mde 3 L olarak ?l??lmesidir. ?evre koşulları, sistemin doğrusallığı ve kalibrasyon gibi değişkenlerden etkilenir.
Tekrarlanabilirlik, kesinlik (repeatability, presicion): Cihazın her tekrar ?l??mde aynı değeri, hatalı bile olsa vermesidir. Belli bir zaman diliminde teknisyen, ?l??m y?ntemi ve fiziki ortam gibi koşulların değişmediği durumda bu ?zellik ge?erlidir.? ?rneğin; cihazın 3 L'lik zorlu vital kapasite (FVC)'yi her ?l??mde 2.7 L ?l?mesidir. Tekrarlanabilirlik ve kesinlik PEF metre gibi tanısal değil takip ama?lı kullanılan cihazlar i?in ge?erlidir.
?l??mler arasında vol?m (hacim) en ?ok %3 veya 0.05 L değişmeli, 8 L'den fazla ?l?ebilmelidir. ?l??mler arasında akım en ?ok %5 veya 0.20 L/saniye değişmeli, akım 14 L/saniye ?l?ebilmelidir.
?retilebilirlik (reproducibility): Cihazın farklı koşullarda ?değişik teknisyen, farklı laboratuvar ortamı gibi? biri birine yakın, kabul edilir sınırlar i?inde sonu? vermesidir. ?rneğin bir hastaya ?ok kez ve aynı cihazla farklı teknisyen ile ya da farklı mekanda (?rn. aynı spirometre ile birinci testte laboratuvarda, bir başka g?n ise yatak başı) test uygulandığında veya belki bir ilacın etkisini belli zaman araları ile takip ederken aynı cihazla ama farklı zamanlarda ?alışan teknisyenlerle test yapılması gerektiğinde bu ?zellik ?nemlidir.
?l??m aralığı: ?retici firmanın belirlediği ilgili parametredeki değişikliğin ?l??lebileceği en alt ve en ?st sınırdır.
Rezol?syon: Parametrede ?l??lebilen en k???k değişikliktir. Rezol?syon standartları: akım 5 mm/L/saniye, vol?m 10 mm/L, zaman 20 mm/saniye şeklindedir.
Cihazlarda bu tanımların teknik ?zellikler ?retici/satıcı firmalarca net bir şekilde belirtilmiş olmadır. Bir solunum fonksiyonu laboratuvarı sonu?larının tutarlı olması i?in cihazların kalite kontrol ve kalibrasyonu cihazların kullanım kılavuzlarında belirtilen ve ATS/ERS raporlarında ?ng?r?len aralıklarla d?zenli olarak yapılmalıdır. Koordinat?r hekim ve laboratuvar sorumlusu teknisyen bu ?zelliklerin cihazın kullanım ?mr? s?resince g?venilir sınırlar i?inde tutulmasından sorumludurlar.
Spirometre Tipleri (5,6):
1. Vol?m Duyarlı Spirometreler; doğrudan vol?m ?l?erler.
2. Akım Duyarlı Spirometreler (Pn?motakometreler); akım ve zaman ?arpımı ile vol?m? elde eden bilgisayarlı sistemlerdir. En az 7 L kapasiteli olup 0-12 L/saniye arasındaki akım hızlarını ?l?ebilirler.
G?n?m?zde vol?m duyarlı spirometreler kullanılmamaktadır. Bu nedenle bu b?l?mde akım duyarlı spirometrelerin ?zelliklerinden bahsedilecektir.
Bilgisayar cihazlarının ve ilgili yazılımların gelişmesi, bu grup cihazların k???k ve taşınabilir olmaları akım spirometrelerin daha ?ok yaygınlaşmasını sağlamıştır. Akımı doğrudan ?l?en bu cihazlar i?lerinden ge?en hava akımının zaman ile ?arpımından havanın hacmini hesaplarlar. En ?ok kullanılan akım duyarlı spirometreler şunlardır (5-7);
1. Pn?motakograf: Venturi etkisi prensibine g?re ?l??m yaparlar. Fleisch ve Lilly olmak ?zere 2 tipi vardır, Fleisch tip pn?motakograflar daha g?venilir kabul edilir. Ancak her iki tip pn?motakografların zayıf y?nleri, ısı, nem ve atmosferik basınca duyarlı olmaları ve bu nedenle sık (en az g?nl?k ve her yer değişikliğinde sonra) kalibrasyon gerektirmeleridir.
2. Turbin spirometre: İ?inde bir turbinin bulunduğu t?p i?erine hızla ?flenmesi ve turbinin d?nd?r?lmesi ile ?l??m yaparlar. G?venilirlik ve tekrarlanabilirliği y?ksektir. Karbon ya da kevlar i?erikli turbinlerin kullanıldığı cihazlarda kalibrasyon ve termostat kullanımına ihtiya? olmaması avantajdır. Turbinin zaman zaman temizlenmesi gereklidir. G?n?m?zde en ?ok kullanılan spirometre ?eşididir.
3. Isıya duyarlı (tel) akım spirometreler (anemometre): Platinden yapılmış ısıya duyarlı ince bir telin bulunduğu t?p i?inden ge?en havanın tel ?zerinde yarattığı ısı farkına g?re ?l??m yapar. ?flenen havanın yarattığı havanın akımına (inspiryum, ekspiryum) duyarlı değildir. Elektrik enerjisi ile belli bir ısıda tutulan bu telin epey kırılgan olması, cihaz hareket ettirildiğinde kolaylıkla arızalanması kullanımını zorlaştırır. G?venilirliği az, sık kalibrasyon gerektiren cihazlardır.
4. Ultrason spirometreler: G?n?m?zde en modern teknoloji ile ?retilmiş spirometrelerdir. Kalibrasyon ve termostat kullanımına ihtiya? olmaması avantajdır. G?venilirlik ve kesinliği y?ksektir.
SOLUNUM FONKSİYON TESTİ LABORATUVARI DİREKT?R, SORUMLU ve TEKNİSYEN ?ZELLİKLERİ
SFT laboratuvarı bir "tıbbi direkt?r" tarafından y?netilir. Bu tıbbi direkt?r g?ğ?s hastalıkları uzmanı olmalıdır. Tıbbi direkt?r SFT laboratuvar personelinin eğitimi, cihazların kalite ve fonksiyonel durumunun denetlenmesi ve testlerin raporlanmasından sorumlu kişidir (8).
SFT laboratuvarlarında bir de SFT sorumlusu olmalıdır ve SFT sorumlusu, tercihen biyomedikal b?l?m? mezunu, SFT laboratuvarın da en az iki yıl bilfiil g?rev yapmış, laboratuvarın diğer teknisyenlerine kılavuzluk edebilecek, laboratuvarda gelişebilecek sorunların ??z?lmesinde rol ve sorumluluk ?stelenebilecek deneyim ve donanımda olmalıdır.
SFT laboratuvarında ?alışabilecek teknik elemanın sertifiye bir laboratuvarda altı aylık pratik eğitim almış olması ?nerilir. Konuya y?nelik teorik ve pratik eğitim T?rk Toraks Derneği (TTD) tarafından d?zenlenecek programlar ile olmalıdır. SFT laboratuvarı teknik elemanlarının bu programlara katılmış ve katılım belgesi almış olması ?nerilir (9).
?neriler, mevcut laboratuvarın imkanlarına g?re değişecektir. Eğer teknik personel bir hemşirelik programından mezun ise, matematik, fizik, biyolojik bilimlerde y?ksekokul d?zeyinde bir eğitimi varsa, hem eğitim s?resi hem de sorun ??zme becerisinin kazanılması i?in ?ng?r?len pratik eğitim s?resi daha kısalabilir.
SFT teknisyeninin genel dikkat edilmesi gereken ?zellikleri şunlardır;
1. En az lise mezunu, tercihen Sağlık Bilimleri alanında eğitim almış,
2. Konuya y?nelik teorik eğitim almış,
3. Uygulanan teknikleri bilen,
4. Pratik olarak uygulayabilen,
5. Kullanılan teknoloji, ?l??mler, kalibrasyon, hijyen, kalite kontrol?n?n teorik ve pratik y?nleri hakkında bilgi sahibi kişilerden se?ilmelidir (10).
Teknisyenlerin eğitimlerinin en az beş yılda bir tekrarlanması, teknisyenlerin ?alıştıkları ortamda da eğitimlerin s?reklilik g?stermesi yararlı olacaktır.? Teknisyenlerin bilgi g?ncelleme-danışma kaynakları olarak, TTD Solunum Fonksiyon Testleri (2012) kitabının kullanılması ?nerilir (11).
SFT teknisyenlerinin se?iminde testlerden sağlığı olumsuz etkilenebilecek astım, bronş aşırı duyarlılığı gibi sağlık sorunları olmamasına dikkat edilmelidir (9,10).
KALİTE KONTROL ve KALİBRASYON
Kalibrasyon, bir cihazın ?l?t?ğ? akım veya hacmin değerleri ile ger?ek akım ve hacim değerleri arasındaki ilişkinin bir referans cihazla karşılaştırarak doğrulanmasıdır.
SFT laboratuvarlarında g?nl?k uygulama cihazın rutin kalibrasyonu ile başlar. Cihazların d?zenli bakımı yapılmalıdır. Cihazların temizliği, aşırı sıcak veya soğuğa maruz bırakılmaması, gereken par?aların d?zenli değiştirilmesi, ara bağlantıların g?nl?k kontrol? gereklidir. Yıllık kalibrasyonlar ise sorumlu firma tarafından yapılır.
Kalibrasyon i?in standart, 3 L'lik ve ?nerilecek koşullarda muhafaza edilecek "kalibrasyon şırıngası" kullanılır. Kalibrasyon şırıngasının sağlamlığı ka?ağı ?nlemek a?ısından her yıl kontrol edilmelidir. Şırınga, spirometre ile aynı ?evre koşullarında tutulmalıdır. Direk g?neş ışığından ve sıcak cisimlerden uzak kalmalıdır. Uygun olmayan hasarlı bir şırınga kalibrasyon yazılımının hatalı sonu?ları kabul etmesine yol a?ar.
Kalibrasyon Denetimi
Kalibrasyon denetimi-kontrol? ise g?nl?k uygulamada kullanılan ve ?l??len değerlerin kabul edilen (? %3 veya 5) sınırlar i?inde olup olmadığının denetlenmesidir. Ortamda 30 dakika i?inde > 3?C değişiklik oluşursa veya ?ok sayıda gruplar halinde test yapmak gerekirse kalibrasyonlar tekrarlanmalıdır. Bu ?zellikle saha taramalarında mekan değişikliğine bağlı fizik koşulların değiştiği ?l??mler i?in gereklidir.
Akım spirometrelerinde hacim kalibrasyon denetimi g?nl?k yapılmalıdır: Yavaş 6 saniye (0.5 L/saniye), orta 1-2 saniye (1.5-3.0 L/saniye) ve haftalık olarak da hızlı 0.5 saniye (6.0 L/saniye) manevra yaptırılır. Linearite ise 3 yavaş, 3 orta, 3 hızlı akımda manevra yaptırılarak değerlendirilir. ?l??len vol?mde en fazla? ? %3.5 değişim kabul edilebilir.
Biyolojik Kontrol
Bilinen sağlıklı bir denek ile (tercihen sağlıklı laboratuvar ?alışanlarından biri) aylık test ?l??m? yapılarak, ?nceki ?l??mlerle farklılık olup olmadığı g?zetilmelidir. Farklılık saptandığı takdirde kalibrasyonlar tekrarlanmalıdır.
Kalibrasyon şırıngası vol?m ve akımın doğruluğunu ?l?erken biyolojik kontrol ile sistem i?i (spirometre, gaz analiz?rler, yazılım) kontrol edilmiş olur.
KAYIT SİSTEMİ ve BELGELER (2,12)
Cihazların bakımı, kontrol?, kalibrasyonları, yazılım ve donanım yenilemeleri, onarımları yapıldığında d?zenli aralarla kayıt altına alınarak laboratuvarda arşivlenmelidir.
Yazılı olarak testle ilgili bazı belgelerin laboratuvar duvarında asılı olmasında zorunlu olmamakla birlikte fayda vardır, bunlar;
?retici tavsiyesine g?re test ?ncesi yapılacak??? kalibrasyon listesi,
Testin basamakları,
Hastanın teste hazırlanma basamakları,
Testin kalite kontrol (kabul ve tekrar edilebilirlik),
G?venlik uyarıları (infeksiyon kontrol?),
Sonu?ların değerlendirilmesinde kullanılacak beklenen değer tablo ve form?lleri.
Her laboratuvarın kalite protokol dosyası bulunmalıdır. Bu dosyada bulunması ?nerilenler:
Kalibrasyon raporları,
Y?ntemlerin genel tarifi ve ?zel bir durum varsa a?ıklanması,
Hastanın teste hazırlanması,
İlgili g?venlik uyarıları (panik, acil durumlar, infeksiyon uyarısı gibi),
Referans değer tablo ve form?lleri,
Hekim ve sorumlu teknisyen imzaları.
Cihazın ?retici-aracı firma tarafından verilen kullanım kılavuzu da ayrıca her laboratuvarda muhafaza edilmelidir.
Ayrıca her laboratuvarın acil durum eylem planı tercihen yazılı ve duvarda asılı olmalıdır. Acil ila?ları, oksijen bulunmalı ve defibrilat?r yakında olmalıdır. Solunum yolu m?dahale aparatları ve diğer gerekebilecekleri i?eren acil malzeme arabasının aynı ortamda bulunmasında fayda vardır.
İNFEKSİYON KONTROL? ve DEZENFEKSİYON STANDARTLARI
Her sağlık kuruluşunun kendi infeksiyon kontrol politikası olması zorunludur. İnfeksiyon kontrol?, sterilizasyon, kişisel korunma ekipmanlarının kullanımı ve teknisyen eğitimini kapsar.
ATS laboratuvar ortamındaki nazokomiyal infeksiyonlardan korunulması i?in "National Committee for Clinical Laboratory Standards (NCCLS)" ve "Centers for Disease Control and Prevention (CDC)" tarafından hazırlanan rehberi tavsiye eder. Bu rehberin t?m SFT laboratuvarlarında olması ve ?nerilerinin izlenmesi tavsiye edilir. Sağlık ?alışanları da bu g?venlik ?nlemleri ve rehberler hakkında eğitilmelidir (2).
Hijyen ve İnfeksiyon Kontrol?
İnfeksiyon kontrol?nde ama? infeksiyonun test yapılan hastalar arasında ve teknisyen ile hasta arasında karşılıklı ge?işini ?nlemektir.
SFT sırasında infeksiyon ge?işi olduğu g?sterilen olgu sayısı ?ok azdır ancak olma potansiyeli vardır. İnfeksiyon kontrol? spirometri, dif?zyon kapasitesi ve akciğer vol?mlerini ?l?en cihazlarda kullanılan ekipmanları hedef almaktadır. Organizmalar ayrıca pulse oksimetre probları ve bronkodilat?r verilen nebulizat?r ve inhaler hazneleri yoluyla da ge?ebilir (13,14).
İNFEKSİYONUN YAYILMA YOLLARI
İnfeksiyon doğrudan veya dolaylı temas ile yayılabilir.
Doğrudan Temas
?st solunum yolu infeksiyonları, enterik infeksiyonlar, kan yoluyla ge?en infeksiyonların etkenlerinin doğrudan temas ile yayılma riski vardır. Doğrudan temas cilt temasıyla, t?k?r?k ve diğer v?cut sıvılarıyla kontaminasyon yoluyla olur. Hepatit ve insan imm?nyetmezlik vir?s? (HIV)'n?n t?k?r?k ile ge?işi d?ş?k ihtimal olsa da oral mukozadaki a?ık yaralar veya kanayan diş etleri bu riski artırır (15). Temasın en riskli olduğu yerler ağızlıklar, kapakların ve set borularının proksimal y?zeyleridir.
Dolaylı Temas
T?berk?loz, viral infeksiyonlar, fırsat?ı infeksiyonlar ve nozokomiyal pn?moniler havada asılı damlacıklar yoluyla bulaşabilir. Temasın en riskli olduğu yerler yine ağızlıklar, kapakların ve setlerin temaslı y?zeyleridir.
İnfeksiyon ge?işini kolaylaştıran etkenlerden biri organizmanın vir?lansıdır. Organizmaların vir?lansı ?ok sayıda fakt?rle ilişkilidir. Bu fakt?rler arasında patojenin kaynağı, inok?lasyon oranı, viabilitesi, ısı-ışık duyarlılığı, etkeni taşıyan aerosol?n b?y?kl?ğ? sayılabilir. Konak?ı fakt?rleri de infeksiyon ge?işinde anlamlı rol oynar.
Doğrudan Temas ile İnfeksiyonun Ge?iş Yolları Damlacık Yoluyla Bulaş
SFT laboratuvarında infeksiyon ge?işinin en fazla olduğu yoldur. ?st hava yolundan salınan infekte damlacıklar vir?s, mikobakteri ve diğer bakteriler gibi ?ok ?eşitli mikroorganizmaları barındırır. Bu mikroorganizmalar ile influenza, kızamık, kızamık?ık, pn?moni ve t?berk?loz infeksiyonu gelişir. T?k?r?k ve balgam SFT laboratuvarında ana infeksiyon kaynağıdır. İnfekte kişinin kullandığı ekipman ?zerinde kalan damlacıklar iyi temizlenmediğinde arkasından teste alınan hastada ?apraz infeksiyon gelişmesine sebep olur. SFT laboratuvarında bulaşta en ?nemli ve ciddi infeksiyon t?berk?lozdur. Ancak t?berk?loz bulaşı riski hakkında elimizde yeterli veri bulunmamaktadır. SFT sonrası Mycobacterium tuberculosis ile infeksiyon gelişimine dair bir olgu sunumu yayınlanmıştır (16). Bir araştırmada ise spirometre par?alarından alınan s?r?nt? ve yıkamalarında t?berk?loz k?lt?r? pozitif bulunmuştur. Ayrıca SFT sonrası bulaş yoluyla t?berk?loz deri testi pozitifleşen bir olgu bildirilmiştir (17).
T?berk?loz infeksiyonu ge?işi damlacık i?indeki aktif mikroorganizma ile olur. İnfekte kişinin ?ks?rmesi veya zorlu ekspiratuvar manevralar ile bu damlacıklar ortama salınır. Bu damlacıklar oda sıcaklığında dokuz saat canlılığını s?rd?r?r. ?oklu ila? direnci olan olgular ?zellikle ?nemlidir. Damlacık yoluyla bulaşan t?berk?loz da ?evresel m?hendislik kontrolleri ?rneğin ventilasyon, hava filtrasyonu ve ultraviyole dekontaminasyon kullanılmalıdır.
Cilt Teması ile Bulaş
Doğrudan cilt teması Rhinovir?s ve Burkholderia cepacia infeksiyonu bulaşında ana yoldur. B. cepacia, bağışıklığı normal kişilerde patojenik değilken, ?zellikle kistik fibrozis olgularında infeksiyona yol a?ar. Tek merkezli bir araştırmada kontamine SFT donanımı ile kistik fibrozis olgularında B. cepacia infeksiyonlarında artış olduğu g?r?lm?şt?r.
Bağışıklığı baskılanmış olgularda ?st hava yollarının normal florasında bulunan Haemophilus influenza, Branhamella catarrhalis ve Streptococcus pneumonia ile infeksiyon riski y?ksektir.
Tablo 1'de SFT laboratuvarlarındaki potansiyel infeksiyon etkenleri, riskli durumlar ve gerekli ?nlemler ?zetlenmiştir.
Hava yoluyla bulaş i?in ?nlemler
Kişisel korunma ekipmanlarının kullanılması,
Maske kullanılması (N95),
İnfekte hastalarda ayrı cihazların kullanılması. Testten sonra derhal dezenfekte edilmesi,
Testin ayrı odada ve m?mk?nse negatif basın?lı odada yapılması,
Infeksiyonu/riski olduğu bilinen hastaların testlerinin g?n?n sonunda yapılması.
Temas yoluyla bulaş i?in ?nlemler
Sağlık ?alışanları her testten sonra ellerini yıkamalı, m?mk?nse her test sırasında tek kullanımlık tıbbi eldiven kullanmalı,
Ağızlıklar her testten sonra değiştirilmeli,
Hastalar testten ?nce ve sonra ellerini yıkamalı veya dezenfektan ile temizlemeli,
Ağızlığın sens?rden uzaklaştırılması cihazın kontaminasyon riskini azaltır,
Aktif infeksiyonları olan sağlık ?alışanlarının hastalıkları s?resince labaratuvarda ?alışmamaları,
M?mk?nse sadece aşılı personelin infekte hastayla temas etmesi.
Damlacık yoluyla bulaş i?in ?nlemler
Kişisel koruyucu ekipmanların kullanılması,
İki test arasında damlacıkların ??kmesine yetecek kadar s?re bırakılması,
Her testten sonra y?zeylerin temizlenmesi gereklidir.
DONANIM-EKİPMAN
İnfeksiyon ge?işinde ?zellikle hasta ve SFT arasındaki bağlantı aparatları (setler, rebreathing kapakları ve ağızlık) her hastada değiştirilmeli veya ?ok kullanımlık olanlar dezenfekte edilmelidir.
SFT laboratuvarında ortaya ?ıkan tek kullanımlık atıklar ?rneğin ağızlık, kağıt pe?ete vb. mikroorganizmalar i?in depo g?revi g?rerek ?apraz infeksiyon riskini artırır. Bu atıklar derhal uygun ??p kutularına atılmalı ve ortamdan uzaklaştırılmalıdır (18).
?NLEMLER
Teknisyene İnfeksiyon Bulaşının ?nlenmesi
Kontamine spirometre y?zeyinden teknisyene infeksiyon bulaşının ?nlenmesinde en etkin y?ntemler el yıkama ve bariyer materyallerin ?rneğin uygun eldivenlerin kullanılmasıdır (18,19).
Teknisyenin elinde kesik veya yara var ise potansiyel kontamine donanıma dokunmadan ?nce mutlaka eldiven giymelidir. Her hastadan sonra el yıkanmalıdır. Lodofor, klorhekzidin, glukonat, triklosan, bifenilol ve kloroksilenol ile hazırlanan deterjanlar el sterilizasyonunda kullanılabilir. Sabun i?eren yumuşatıcı ve kremlerde cildi kurutmadan dezenfeksiyon sağlayabilir. El yıkanan lavabolar dirsek veya bilek hizasında ve otomatik olarak dokunmadan kullanılabilmelidir.
?apraz-Kontaminasyonun ?nlenmesi
?apraz-kontaminasyonu ?nlemek i?in ?ok kullanımlık ağızlıklar, setler, kapaklar, burun klipsleri ve manifoldlar d?zenli olarak dezenfekte ve sterilize edilmelidir. Set, kapak veya manifoldların dezinfeksiyon ve sterilizasyon sıklığı i?in optimal bir s?re belirlenmemiştir. ?reticinin ?zel bir ?nerisi yok ise y?zeyi dışarı verilen soluğa bağlı olarak yoğunlaşan par?a derhal dezenfekte edilmelidir.
Sterilizasyonda sıcak y?ntemler ?nerilmez. Cihazların bazı par?alarına soğuk sterilize edici kimyasal ajanlar da zararlı olabilir. Bu sebeple teknisyenler ?reticilerin tavsiyelerine uymalıdır. ?reticiler, cihazın kılavuzunda ekipmanın her par?asının temizleme ve sterilizasyonu i?in gerekli işlemleri, kimyasalları ve konsantrasyonlarını belirtmelidir.
Hastane infeksiyon kontrol komitesinin ?nerileri de izlenmeli ancak iki ?neride ?elişen koşullar varsa tartışılarak karar verilmelidir.
Hastaların G?zlemlenmesi
SFT laboratuvarında soğuk algınlığı gibi d?ş?k riskli infeksiyonlardan t?berk?loz gibi y?ksek riskli infeksiyonlara kadar geniş bir yelpazede infeksiyon riski olabilir. Sağlık ?alışanlarına y?ksek riskli hastalıkların tanısından ş?phelenerek ve gerekli ?nlemleri alabilmeleri i?in eğitim verilmelidir. ?zellikle t?berk?loz belirtileri olan hastaları tanıyabilmeleri i?in gerekli sorular i?in eğitilmelidir. Ayrıca imm?nyetmezlikler ve kızamık konusunda da eğitilmeleri ?nerilir.
İnfekte teknisyen ve hastaların korunma ?nlemlerinin artırılması ?apraz infeksiyon riskini azaltır.
Bağışıklığı baskılanmış hastaların testleri g?n?n ilk saatlerinde diğer hastalardan ?nce yapılmalı, infekte hastaların testleri ise g?n?n ya da haftanın sonunda gerekli ?nlemler alındıktan sonra yapılmalıdır.
İnfekte hastaların laboratuvar i?inde cerrahi maske giymesi sağlanmalıdır.? Eğer ortam şartları uygunsa ayrı bir bekleme odasında bekletilmelidir. Aynı anda ?oklu test uygulanıyorsa hastaların en az bir metre aralıklı olmaları infeksiyon kontrol?ne yardım eder. Bekleme odasında da hastaların teması minimuma indirilmelidir.
Cerrahi maskeler, havlular, ??p kovaları, alkol bazlı temizleyiciler hastaların kolayca ulaşabileceği yerde olmalıdır.
Mycobacterium tuberculosis veya Staphylococcus aureus ile infeksiyon riski olan olguların zorunlu değil ise teste alınmaması ?nerilir. Sterilizasyon işindeki personel Hepatit B vir?se karşı aşılanmalıdır.
SFT laboratuvarında ?alışan personelin, influenza (influenza vir?s?ne karşı) ve pn?moni (S. pneumoniae'ye karşı) aşılarının ve t?berk?loz a?ısından yıllık kontrollerinin yapılması ?nerilir.
Spirometre
Spirometreler SFT laboratuvarında en sık kullanılan cihazlardır. ?eşitli bileşenleri i?inde ağızlıklar bakteriyel kontaminasyon i?in en y?ksek riski taşır (%92), ikinci sırada temaslı setler gelir (%50). Ancak şimdiye kadar yapılan araştırmalarda cihazın i?inden alınan ?rneklerde kontaminasyon bildirilmemiştir.
Ultrasonik sistemlerde ise hasta sadece ağızlığa temas ettiği i?in infeksiyon riski daha d?ş?kt?r.
İnfekte bir hastada ?l??m yapılacaksa akım sens?rl? s?k?lebilir pn?motakometresi olan spirometreler ?ok daha faydalı olacaktır.
A?ık devre sisteminde ise rebreathing olan kısımlar her hastada temizlenmeli ya da tek kullanımlık olanlar kullanılmalıdır.
A?ık devre tekniğinde (hacim veya akım spirometresi) inspirasyon olmadığında sadece ağızlığın değişmesi yeterlidir. Ancak hastanın cihazdan inhale etmediğine emin olmak zordur. D?ş?k diren?li tek y?nl? kapak inhalasyonu engellemek i?in kullanılabilir.
Cihaz ayrılıp birleştirildiğinde, temizlendiğinde ve sens?r yerleştirildiğinde spirometre yeniden kalibre edilmelidir.
Testler arasında en az beş dakika mola olması da yer?ekimsel ??kme ile mikroorganizmaların azalmasını sağlar.
Tek Kullanımlık Bakteri Filtreleri
Donanım kontaminasyonunu ?nlemek i?in en etkin ve en ucuz y?ntemdir. Piyasadaki filtrelerin FVC ve FEV1 ?l??m değerleri ?zerindeki etkileri tam olarak bilinmemektedir. D?ş?k impedanslı filtrelerin FEV1 ve FVC ?zerinde etkisi yoktur. ?nerilen bu filtreler kullanılsa dahi cihaz ve par?alarına gerekli sterilizasyon uygulanmalıdır (20,21).
İnfekte olduğu bilinen hastalarda cihazın kontaminasyonunu ?nlemek i?in bakteri filtreleri kullanılabilir. Cihazın kalibrasyonları filtre takılıyken yapılmalıdır.
Donanım Dizaynı
?reticiler kolayca temizlenebilen cihazlar ?retimi konusunda bilgilendirilmelidir. T?keticiler cihazı almadan ?nce araştırarak kolayca temizlenebilen, sensitizasyon ekipmanları ve kimyasalları hakkında kılavuzunda a?ık ve anlaşılır bilgi verilen cihazları se?melidir.
Tek merkezli bir araştırmada kontamine solunum fonksiyon testi donanımı ile kistik fibrozis olgularında B. cepacia infeksiyonlarında artış izlenmiştir. Pn?motakometre sistemlerinin infeksiyonlara karşı sulu spirometrelerden daha az yatkın olduğuna dair kanıtlar vardır.
Su şebekesi de infeksiyon kaynağı olabilir. Ortak su şebekesinden Mycobacterium avium kompleks, Mycobacterium kansasii, Mycobacterium chelonae, Mycobacterium fortuitum, Mycobacterium xenopi ve Pseudomonas aeruginosa mikroorganizmalarıyla kontaminasyon bildirilmiştir (18,22,23).
Etkin Ortam Temizliği
Kirli ortam, bakteri ve mantarların b?y?mesi i?in uygun bir k?lt?r vasatıdır. Bu sebeple laboratuvarın genel temizliği infeksiyon kontrol?nde ?nemli bir adımdır. Y?ksek kalitede temizlik mikroorganizmaların %90'ını yok eder.
Ortamda ortaya ?ıkan biyolojik atıklar uygun şekilde yok edilmelidir (24,25). İnfekte olan ve olmayan atıkların ayrılması da infeksiyon kontrol?ne yardım eder. Sıvı ve katı tıbbi atıkların ayrılması, sızdırmayan kutularda ve iyi havalanan bir yerde muhafaza edilmesi ?nerilir.
Nebulizat?r ve İnhaler Hazneler
Nebulizat?r ve inhalerlerde ara par?a olarak atomizer ve inhaler hazneler kullanılır. Bu cihaz ve aletlerin iyi temizlenmemesine bağlı infeksiyon ge?işi olabilir (26-30). Etkin temizlenmediğinde P. aeroginosa, S. aureus, Bacillus cereus, ve B. cepacia ile kontaminasyon olma ihtimali y?ksektir. Ayrıca cihazlar ?zerinde bakteri kolonizasyonu olabilir.?
Bu kolonizasyonlar cihazları evde tedavi i?in kullanan hastalarda daha yaygındır.? Tanısal ama?lı kullanılan nebulizat?r ile ?apraz infeksiyon bildirilmemiştir.
Laboratuvar Alt Yapısı
Laboratuvar alt yapısı da infeksiyon ge?işinde ?nemli rol oynar. Y?zey alanları, d?zen, yer d?şemesi, havalandırma, ısı ve nem dengesi ?apraz infeksiyonda ?nemli etkenlerdir. Ortam tozlu, dağınık olmamalı, yer d?şemesinde kalın t?yl? halı kullanılmamalıdır. Havalandırma sistemleri ve filtreleri sık sık temizlenmelidir. Legionella pneumophilia ile infekte aerosollerin inhalasyonu ile bulaşan infeksiyonlar y?n?nden hastane su şebekesi denetlenmeli ve sonu?lar takip edilmelidir. Laboratuvar hastanenin sakin bir yerinde, g?n ışığı alan, aydınlık ve a?ık hava ile havalandırılabilen bir yer olmalıdır (5).
Y?NTEM STANDARDİZASYONU
Klasik olarak spirometrik incelemede yapılan FVC manevrasıdır. FVC; maksimal bir inspirasyondan sonra yapılan zorlu maksimal ekspirasyon manevrası ile ?ıkarılan hava hacmidir (Şekil 1).
Genel ?neriler
?Testten ?nce hasta mutlaka en az 15 dakika dinlendirilmelidir. Hastaya bu esnada testin nasıl yapılacağı ayrıntılı olarak anlatılmalıdır. ?zellikle ağızlığı nasıl kullanacağı, ne zaman nefes alıp vereceği ve maksimal efor yapması gerektiği vurgulanmalıdır. Daha ?nce hi? test yapmamış hastaya teknisyen tarafından testin g?sterilmesi olduk?a yararlıdır (2).
V?cut pozisyonu: Akciğer vol?mleri v?cut pozisyonundan etkilenmektedir. En y?ksek değer ayakta elde edilirken, oturur pozisyona ge?işle vital kapasitede yaklaşık 70 mL azalma olur. Bu azalma gen?lerde belirgin olmayabilir. Yatar pozisyonda ise en d?ş?k değerler elde edilir. Diyafram paralizisi olan olgularda ise yatar pozisyona ge?işle vital kapasitede dramatik d?şme g?zlenir. Bu nedenle diyafram paralizisinden ş?phelenilen olgularda oturur ve yatar pozisyonda iki ayrı ?l??m yapılması tanı koydurucu olabilir.
Zorlu solunum manevraları sırasında hastalarda baş d?nmesi olabileceğinden dolayı testin oturur durumda yapılması daha uygun olur. Her laboratuvarda standart pozisyon uygulanmalı ya da testin hangi pozisyonda yapıldığı kaydedilmelidir.
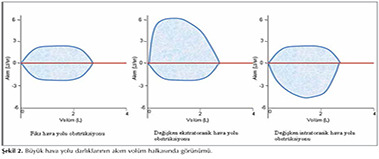
ATS/ERS kılavuzu başta olmak ?zere kılavuzlarda sadece zorlu ekspirasyon manevrası ?nerilmekle birlikte b?y?k hava yolu darlıklarının atlanması a?ısından akım-vol?m halkasında inspiratuvar akımlarında kaydedilmesi uygun olacaktır (Şekil 2).
Testin Uygulanması
Test kapalı devre manevrası şeklinde uygulanmalıdır.?nce hastaya doğru pozisyon verdirilir. Daha sonra burun mandalı takılıp, ağızlık yerleştirilir ve dudakların kapalı olmasına dikkat edilir. Hızlı ve derin inspirasyonun ardından total akciğer vol?m? (TLC) d?zeyinde maksimal ekspirasyon manevrası akciğerler boşalana kadar s?rd?r?l?r (Şekil 1).
Kabul edilebilirlik (VC ya da FVC manevrası i?in) kriterleri (4)
İyi bir başlangı? yapılması ve ekstrapole edilen vol?m?n FVC'nin %5'inden ya da 150 mL'den az olması gerekir.
Manevra sırasında hasta ?ks?rmemelidir. Birinci saniye i?indeki ?ks?r?kler FEV1'in de (FVC manevrasının ilk bir saniyesinde ?ıkarılan hava hacmidir)? yanlış ?ıkmasına yol a?ar.
Ekspirasyonun en az altı saniye s?rmesi ve sonunda (en az bir saniyelik) plato ?izmesi gerekir. (Erken bitirilmemeli) Obstr?ksiyonu olan hastalarda platoya ulaşmak i?in genelde daha uzun s?reye gereksinim vardır. Ancak bu olgularda da genelde altı saniyelik ekspirasyon s?resi yeterli g?r?l?r.
Test sırasında Valsalva manevrası yapılmamalıdır. Glottisin kapanması akımda kesintilere yol a?ar. Ayrıca eforda da değişkenlik olmamalı.
Sistemde ka?ak olmamalı. En sık g?r?len hatalarda biri hastanın ağızlığı iyice kavramamasıdır.
Ağızlık hastanın dili ya da dişleri ile kapatılmamalıdır.
Ayrıca teknisyen tarafından, hastanın maksimal inspirasyon yaptığı, ekspirasyon manevrasına iyi bir şekilde başladığı ve maksimal eforla ekspirasyonu kesintisiz s?rd?rd?ğ? g?zlenmelidir.
Test Sayısı
Her hastaya en az ?? test yaptırılmalıdır. Eğer sekiz kez tekrarlanmasına karşın halen ge?erli manevra elde edilemiyorsa ya da hasta yorulursa test sonlandırılmalıdır. Daha fazla test yapılması bazı hastalarda bronkokonstr?ksiyona yol a?abilir.
Tekrarlanabilirlik [VC (vital kapasite) ya da FVC manevrası i?in] kriterleri (4)
Kabul edilebilirlik kriterlerine uyan en az ?? manevradan en iyi ikisindeki FVC ve FEV1 değerleri arasında 150 mL'den fazla fark olmaması gerekir. FVC'nin bir litreden az olduğu olgularda bu sınır 100 mL olarak alınmalıdır.
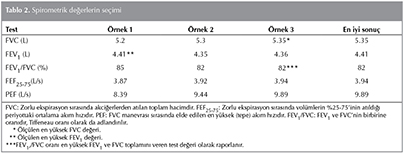
?rneklerden değerlerin se?ilmesi
Kabul edilebilirlik kriterlerine uyan testlerden en iyi FVC ve FEV1 değerleri se?ilir. Bu iki değerin aynı eğri ?zerinde olması gerekmez. FEV1/FVC değeri bu en iyi iki değerin birbirine b?l?m? ile elde edilir. Ekspiratuvar akımlar ise FEV1 ve FVC toplamının en b?y?k olduğu eğriden se?ilir (Tablo 2).
Reversibilite
Obstr?ksiyonun saptandığı olgularda bu obstr?ksiyonun ne kadarının geri d?nd?r?lebilir olduğunun incelenmesidir. Spirometrik incelemenin yapılıp obstr?ksiyon saptanan olgularda hastaya hızlı ve kısa etkili bir bronkodilat?r (?rn. salbutamol, terbutalin, ipratropium vb.) verilip belli bir s?re sonra test tekrarlanarak,? FEV1 ve FVC'deki değişim incelenir (4,31).
TTD Astım Kılavuzunda 200-400 ?g salbutamol uygulamasından 15-20 dakika sonra testin yapılması ?nerilmekte ve FEV1'de %12 ve 200 mL artış pozitif olarak değerlendirilmektedir (32).
TTD KOAH Kılavuzu ise 400 ?g salbutamol, 160 ?g ipratropium ya da her ikisinin birlikte kullanılmasını ?nermekte, test yapılma zamanını ise eğer ipratropium kullanılacaksa 30-45 dakika olarak belirtmektedir (33).
Postbronkodilat?r uygulama ise reversibiliteden farklı olarak hastaya hi? test yapmadan, yukarıdaki sayılan bronkodilat?rlerden birinin verilip daha sonra spirometrik incelemenin yapılmasıdır. KOAH Kılavuzlarında spirometrik incelemenin postbronkodilat?r olarak yapılması ?nerilmektedir.
TESTLERİN BEKLENEN DEĞERLERİNİN TANIMLANMASI ve STANDARDİZASYONU
SFT'ler genellikle aynı bireyde zaman i?erisinde tekrarlanması gerekli ?l??mler olduğu i?in, testin değerlendirilmesinde kullanılacak referans değerlerin se?imi sağlıklı bir değerlendirme i?in olduk?a ?nemlidir. Se?ilen referans değerler beklenen değer olarak kabul edilerek, ?l??len solunum fonksiyon parametresi, beklenenin y?zdesi olarak ifade edilmektedir (34). Bu yaklaşım, o birey i?in beklenen normal referans aralık hakkında bilgi vermemektedir. 1991 yılında ATS, sağlıklı sigara i?meyen referans bir pop?lasyonda elde edilen t?m değerlerden 5. persentili normalin alt sınırı (lower limits of normal) olarak değerlendirmeyi ?nermiştir. SFT'lerde referans değerler, akciğer hastalığı ?yk?s? bulunmayan, sigara veya ?evresel hava kirleticiler gibi risk fakt?rlerine maruziyeti bulunmayan veya ?ok d?ş?k d?zeyde maruziyeti olan sağlıklı bireylerden oluşan b?y?k araştırma gruplarından elde edilen ?l??mlerin istatistiksel analizine dayanmaktadır (35). T?m solunum fonksiyon ?l??mleri, sağlıklı bireyler arasında değişkenlik g?stermektedir. Yaş, cinsiyet, boy, ırk veya etnik k?ken, v?cut ağırlığı, v?cut y?zey alanı gibi fiziksel ?zellikler, SFT'lerde ?l??len parametreler ?zerine belirgin etkisi olan değişkenlerdir. Genellikle yaş ve boy, SFT'lerde ?l??len pek ?ok parametre ile doğrusal bir ilişki g?stermektedir (36). Bu bilgilerden hareketle, bir bireyin yaş, boy gibi fiziksel ?l??mlerinden solunum fonksiyonları i?in beklenen değerlerin tahmin edilebileceği doğrusal regresyon denklemleri geliştirilmiştir (36). Ancak adolesanlarda ?zellikle hızlı b?y?me d?neminde ve ileri yaşlılarda, solunum fonksiyonları ile fiziksel karakteristikler arasındaki ilişki artık doğrusal değildir. Bu nedenle, bu yaş gruplarında s?z konusu doğrusal regresyon modelleri, beklenen solunum fonksiyon parametrelerini tahmin etmede yetersiz kalmaktadır (35). Bir diğer yandan ?rneklem yapılan pop?lasyondaki normal bireylerin, beslenme, eğitim d?zeyleri ve yaşadıkları ortamdaki ?evresel fakt?rler de solunum fonksiyonlarını etkilemektedir. T?m bu fakt?rler bir arada "kohort etkisi" olarak değerlendirilmekte olup, beklenen değerlerin hesaplanması i?in se?ilecek referans değerlerin k?ken aldığı ?rneklem grubunun, ?l??m yapılacak gruba benzerliği bu bakımdan da olduk?a ?nemlidir (37).
Irk ve etnik k?ken, v?cut ?l??mlerini etkileyen bir diğer ?nemli değişkendir. Solunum fonksiyonları, ?zellikle de akciğer hacimleri ırklar arasında ?nemli ?l??de farklılık g?stermektedir. Bazı SFT yazılımları, farklı ırklar i?in beyaz ırkın referans alındığı d?zeltme fakt?rlerini ekleyerek, beklenen solunum fonksiyon testlerini raporlamaktadır. Ancak tanımlanan d?zeltme fakt?rlerinin ırk-spesifik beklenen değer denklemleri kadar başarılı sonu? vermediği saptanmıştır. Bu nedenle, beklenen solunum fonksiyon testlerinin tayini i?in ırk-spesifik referans değerlerin kullanılması ?nerilmektedir. ?rneğin, Hankinson tarafından 1999 yılında Amerika Birleşik Devletleri (ABD)'nde Ulusal Sağlık ve Beslenme Değerlendirme Araştırması (NHANES III) pop?lasyonunda referans denklemler, beyaz, Afrikan-Amerikan ve Hispanik Amerikan gibi ırklar i?in ayrı ayrı tanımlanmıştır (36). ATS ve ERS 2005 yılında yayımladıkları ortak uzlaşı raporunda, ABD i?in 8-80 yaş arası bireyleri temsil eden Hankinson normlarının;? 8 yaş altındaki ?ocuklar i?in, ?zellikle ?ocukların değerlendirildiği Wang tarafından tanımlanan referans denklemlerin kullanılmasını ?nermiştir (36,38). Bu uzlaşı, Avrupa'da ise erişkinlerde Avrupa K?m?r ve ?elik Birliği (ECSC)/ERS tarafından 1993 yılında yayımlanan referans denklemlerini, ?ocuklarda ise Quanjer'in tanımladığı pediatrik normların kullanılmasını ?nermiştir (39). ?lkemiz i?in de (ECSC)/ERS tarafından 1993 yılında yayımlanan referans denklemlerinin kullanılması g?n?m?ze dek ?nerilmiştir ve yaygın olarak bu normlar kullanılmaktadır. Ancak, ATS/ERS 2005 yılı ortak uzlaşı raporunda t?m Avrupa'yı temsil eden daha g?ncel referans normların tanımlanmasına gereksinim olduğu da belirtilmiştir (31).
Beklenen değerlerin tanımlanmasında genel yaklaşım, ?ok sayıda sağlıklı bireyde SFT'lerin ?l??lmesi, daha sonra her parametre i?in o grup i?indeki değişkenliğin saptanmasıdır. Bu pop?lasyonda aynı parametre i?in ?l??len t?m değerlerden 5. persentilin normalin alt sınırı (lower limits of normal) iken; 5. persentil altında yer alan t?m ?l??mler ise anormal kabul edilmektedir (31).
1971 yılından g?n?m?ze pek ?ok farklı sayıda referans denklem tanımlanmıştır. Quanjer ve arkadaşları, otuz farklı yazar tarafından tanımlanan denklemleri aynı cins, boy ve yaştaki bir hasta i?in uyarlandığında, hesaplanan beklenen FEV1 değerinin, se?ilen form?le g?re bir diğerinden yaklaşık 1 Litre farklılık g?sterebileceğini saptamıştır (40). Bu endişe verici analiz neticesinde, 2010 yılında ERS altı b?y?k uluslararası solunum derneğinin de desteği ile Global Solunum Fonksiyon İnisiyatifi (GLI)'ni kurmuştur (31,41).
GLI kapsamında, toplam 33 ?lke (Cezayir, Avusturya, Avustralya, Brezilya, Kanada, Şili, ?in, Meksika, Fransa, Almanya, İzlanda, Hindistan, İran, İsrail, İtalya, Portekiz, G?ney Afrika, G?ney Kore, İsve?, İsvi?re, Tayvan, Tayland, Tunus, ABD, İngiltere, Uruguay ve Venezuela) ve 72 merkezden, 2.5-95 yaş arasında 97.759 sigara i?meyen sağlıklı bireyin SFT'leri değerlendirilerek FEV1, FVC, FEV1/FVC i?in yeni LLN normları ve beklenen değerler tanımlanmıştır.
Bu yeni yaklaşım, SFT sonu?larının raporlanması aşamasına da yenilikler getirmektedir. Hastanın mutlak ?l??mleri korunurken, bir diğer yandan da FEV1, FVC, FEV1/FVC değerlerinin z-skorları, beklenen normal referans değer aralığının da belirli olduğu bir piktogram ?zerinde işaretlenmektedir. Burada FEV1, FVC, FEV1/FVC değerleri i?in z-skorunun -1.64'ten d?ş?k olmasının (< 5. persentil) normalin alt sınırı olarak tanımlanmasını ?nermektedir. B?ylece test sonu?larının kolayca g?rsel olarak da değerlendirilmesi m?mk?n olmaktadır (Şekil 3). S?z konusu değerlendirme bronkodilat?rl? test uygulandığında, bronkodilat?r ?ncesi ve sonrası z-skorlarını da piktogram ?zerinde işaretlemektedir.
Solunum fonksiyon testleri tarama amacıyla uygulandığında beklenen alt değerin 2.5 sentil olarak alınması yani z-skorunun -1.96'nın altında olmasının anormal olarak değerlendirilmesi ?nerilirken; daha ?nceden bilinen akciğer hastalığı bulunan, solunumsal yakınmaları olan bireylerde normalin alt sınırının 5. persentil, yani z-skorunun -1.64'?n altında olmasının patolojik olarak değerlendirilmesi ?nerilmektedir. ?lkemiz koşullarında laboratuvarlarımızda kullanılan yazılım programları uygun olduğu takdirde, dinamik ?l??mle elde edilen parametreler i?in beklenen değer olarak 2012 GLI referans normlarının yukarıda belirtildiği şekilde kullanılması ?nerilir. Ancak, yenilenmemiş yazılımların olduğu cihazların kullanıldığı laboratuvarlarda (ECSC)/ERS tarafından 1993 yılında yayımlanan referans denklemlerinin kullanılması doğru olacaktır.
Sonu? olarak 2012 GLI normları ile, 40'tan fazla ?lkenin katılımıyla 3 ila 95 yaş arasında global olarak kullanılabilecek spirometrik beklenen değerler tanımlanmıştır. Bu yeni yaklaşım, SFT sonu?larının raporlanmasında FEV1, FVC, FEV1/FVC değerlerinin z-skorları, beklenen normal referans değer aralığının da belirli olduğu bir piktogram ?zerinde işaretlenmekte, g?rsel değerlendirme kolaylığı sağlanmaktadır. Standardize z-skorları aracılığıyla farklı farklı merkezlerde yapılan ?l??mler arasında bir standardizasyon sağlanabileceği ?ng?r?lmektedir. Pek ?ok ?lkede 2012 GLI normlarının ge?erliliği test edilmiştir. 2012 GLI normlarının, kendi pop?lasyonunda beklenen SFT referans değerleri ?alışılmamış olan ?lkemiz i?in de g?venli bir değerlendirme y?ntemi olabileceği inancındayız.
KAYNAKLAR
- Wanger J. ATS Pulmonary Function Laboratory Management and Procedure Manual 3rd Edition. https://store.thoracic.org 6 june 2016.
- Crapo RO. Pulmonary-function testing. N Eng J Med 1994;331:25.
- Redlich CA, Tarlo SM, Hankinson JL, Townsend MC, Eschenbacher WL, Von Essen SG, et al. American Thoracic Society Committee on Spirometry in the Occupational Setting. Official American Thoracic Society technical standards: spirometry in the occupational setting. Am J Respir Crit Care Med 2014:15;189:983-93.
- Miller MR, Crapo R, Hankinson J, Brusasco V, Burgos F, Casaburi R, et al. General considerations for lung function testing ATS/ERS Task Force: Standardisation of Lung Function Testing. Eur Respir J 2005;26:153-61.
- Pulmonary Function Testing and Equipment. In Manuel of Pulmonary Function Testing. Ninth edition. Ruppel GL (ed).China: Mosby Elsevier, 2009:327-83.
- American Thoracic Society, Committee on Proficiency Standarts for Clinical Pulmonary Laboratories: Computer Guidilines for Pulmonary Laboratories. Am Rev Respir Dis 1986;134:628-32.
- Basic Equipment and Measurement Techniques. Lung Function: Physiology, Measurement and Application in Medicine. JE Cotes, DJ Chinn, MR Miller. 6th ed. India: Blackwell Publishing, 2009:59-81.
- Gardner RM, Clausen JL, Epler G, Hankinson JL, Permutt S, Plummer AL. Pulmonary function laboratory personnel qualifications American Thoracic Society. Am Rev Respir Dis 1986;134:623-4.
- Miller MR, Hankinson J, Brusasco V, Burgos F, Casaburi R, Coates A, et al. ATS/ERS Task Force: Standardisation of spirometry. Eur Respir J 2005;26:319-38.
- Haynes JM. Quality assurance of the pulmonary function technologist. Respir Care 2012;57:114-26.
- Saryal SB, Ulubay G. Solunum fonksiyon testleri. Toraks Kitapları. İstanbul: Aves Yayıncılık, 2012:16.
- Ruppel GL. Quality assurance in the pulmonary function laboratory. In: Manuel of pulmonary function testing. 9th ed. China: Mosby Elsevier, 2009:384-411.
- Botman MJ, de Krieger RA. Contamination of small volume medication nebulizers and its association with oropharyngeal colonization. J Hosp Infect 1987;10:204-8.
- Dautzenberg B. Prevention of nosocomial infection during nebulization and spirometry. Rev Pneumol Clin 2001;57:91-8.
- Denison DM, Cramer DS, Hanson PJV. Lung function testing and AIDS. Respir Med 1989;83:133-8.
- Johns DP, Ingram C, Booth H, Williams TJ, Walters EH. Effect of microaerosol barrier fitler on the measurement of lung function. Chest 1995;107:1045-8.
- Hazaleus RE, Cole J, Berdischewsk M. Tuberculin skin test conversion from exposure to contaminated pulmonary function testing apparatus. Respir Care 1981;26:53-5.
- Burgos F, Torres A, Gonzalez J, Puig de la Bellacasa J, Rodriguez-Roisin R, Roca J. Bacterial colonization as a potential source of nosocomial respiratory infections in two types of spirometer. Eur Respir J 1996;9:2612-7.
- Tabalan OC, Williams WW, Martone MJ. Infection control in pulmonary function laboratories. Infect Control 1985;6:442-4.
- Kirk YL, Kenday K, Ashworth HA, Hunter PR. Labortaory evaluation of a filter fort he control of cross-infection during pulmonary function testing. J Hosp Infect 1992;20:193-8.
- Rutala DR, Rutala WA, Weber DJ, Thomann CA. Infection risks associated with spirometry. Infect Control Hosp Epidemiol 1991;12:89-92.
- Isles A, Maclusky I, Corey M, Gold R, Prober C, Fleming P, et al. Pseudomonas cepacia in cystic fibrosis: an emerging problem. J Pediatr 1984;104:206-10.
- Du moulin GC, Stottmeier KD, Pelletier PA, Tsang AY, Hedley-White J. Concentration of Mycobacterium avium by hospital hot water systems. JAMA 1988;260:1599-601.
- Kendrick AH, Johns DP, Leeming JP. Infection control of lung function equipment: A practical approach. Respir Med 2003;97:1163-79.
- Clausen JL. Lung volume equipment and infection control. ERS/ATS Workshop Report Series. European Respiratory Society/American Thoracic Society. Eur Respir J 1997;10: 1928-32.
- Ducel G, Fabry J, Nicolle L. Epidemiology of nosocomial infections. Prevention of hospital-acquired infections. A practical guide. 2 nd ed., Ch. 1. World Health Organization, 2002;12:6-7.
- Unstead M, Stearnb MD, Cramer D, Chadwick MV, Wilson R. An audit into the efficacy of single use bacterial/viral ?lters for the prevention of equipment contamination during lung function assessment. Respir Med 2006;100: 946-50.
- Rasam SA, Apte KK, Salvi SS. Infection control in the pulmonary function test laboratory. Lung India 2015; 32:359-66.
- Matlow A. Infection Control in the Physician's Office. The College of Physicians and Surgeons of Ontario; Ontario. 2004;4:17-20.
- Singh V, Arya A, Mathur US. Bacteriology of spirometer tubing and evaluation of methodology to prevent transmission of infection. J Assoc Physicians India 1993;41: 193-4.
- Ulubay G. Solunum fonksiyon testleri. In: Dalar L, S?erdem M, ?zt?rk C, Saygı A (eds). G?ğ?s hastalıkları kitabı. T?rkiye Solunum Araştırmaları Derneği. İstanbul: İstanbul Tıp Yayınevi, 2015:141-52.
- T?rk Toraks Derneği Astım Tanı ve Tedavi Rehberi. Turk Thorac J 2016;17(Suppl 1):S1-108.
- Kronik Obstr?ktif Akciğer Hastalığı (KOAH) Koruma, Tanı ve Tedavi Raporu. Turk Thorac J 2014;15(Suppl 2):1-85.
- Ruppel GL, Enright PL. Pulmonary function testing. Respiratory Care 2012:57:165-75.
- Ruppel GL. Reference values. In: Manuel of pulmonary function testing. 9th ed. China: Mosby Elsevier, 2009:423-34.
- Hankinson JL, Odencrantz JR, Fedan KB. Spirometric reference values from a sample of the general US population. Am J Respir Crit Care Med 1999:159:179-87.
- Pellegrino R, Viegi G, Brusasco V, Crapo R, Burgos F, Casaburi R, et al. Interpretative strategies for lung function tests. Eur Respir J 2005:26:948-68.
- Wang X, Dockery DW, Wypij D, Fay ME, Ferris BG. Pulmonary function between 6 and 18 years of age. Pediatr Pulmonol 1993:15:75-88.
- Quanjer PH, Tammeling G, Cotes J, Pedersen O, Peslin R, Yernault J. Lung volumes and forced ventilatory flows. Eur Respir J 1993:6(Suppl 16):S5-40.
- Quanjer PH, Brazzale DJ, Boros PW, Pretto JJ. Implications of adopting the Global Lungs Initiative 2012 all-age reference equations for spirometry. Eur Respir J 2013: 42:1046-54.
- Quanjer PH, Stanojevic S, Cole TJ, Baur X, Hall GL, Culver BH, et al. Multi-ethnic reference values for spirometry for the 3-95-yr age range: the global lung function 2012 equations. Eur Respir J 2012:40:1324-43.
Yazışma Adresi (Address for Correspondence)
Dr. Gaye ULUBAY
Başkent ?niversitesi Tıp Fak?ltesi,
G?ğ?s Hastalıkları Anabilim Dalı,
Ankara, T?rkiye
e-mail: gayeulubay@yahoo.com