RESEARCH ARTICLE
Doi: 10.5578/tt.8452
Tuberk Toraks 2014;62(4):286-290

Ankara Numune E?itim Ara?t?rma Hastanesi G???s Hastal?klar? Klini?inde
son 8 y?lda (2006-2013) TNF-alfa? blokeri kullanan hastalara verilen
latent t?berk?loz tedavisi sonu?lar?
Sema DEM?R1, Filiz SAD? AYKAN1, Derya ?ZTUNA2
1 Ankara Numune E?itim ve Ara?t?rma Hastanesi, G???s Hastal?klar? Klini?i, Ankara, T?rkiye
1 Clinic of Chest Diseases, Ankara Numune Training and Research Hospital, Ankara, Turkey
2 Ankara ?niversitesi T?p Fak?ltesi, Biyoistatistik Anabilim Dal?, Ankara, T?rkiye
2 Department of Biostatistic, Faculty of Medicine, Ankara University, Ankara, Turkey
?ZET
Ankara Numune E?itim Ara?t?rma Hastanesi G???s Hastal?klar? Klini?inde son 8 y?lda (2006-2013) Tnf-alfa blokeri kullanan? hastalara verilen latent t?berk?loz tedavisi sonu?lar?
Giri?: Bu ?al??mada amac?m?z, t?m?r nekroz fakt?r?-alfa (TNF-a) bloker tedavisi almakta olan hastalarda t?berk?loz kemoprofilaksisine ra?men t?berk?loz geli?me s?kl???n? belirlemektir.
Materyal ve Metod: Ankara Numune E?itim ve Ara?t?rma Hastanesi, G???s Hastal?klar? Klini?ine, 2006-2013 y?llar? aras?nda ba?vuran, TNF-α bloker tedavisi halen alan, t?berk?loz kemoprofilaksisi alm?? hastalar, t?berk?loz geli?me s?kl??? a??s?ndan retrospektif olarak de?erlendirildi. TNF-α bloker tedavi endikasyonu alan, romatolojik ve dermatolojik hastal?k tan?s? olan; 18-80 ya? aral???nda, 134 hasta de?erlendirildi. Ya?, cinsiyet, sigara i?me durumu, BCG a??s?, akci?er grafisi, hastal?k tan?s?, ek hastal?k varl???, t?berk?loz hikayesi, PPD de?eri, kemoprofilaksi alma durumu, hangi antit?berk?loz ajan? ald??? ve ald??? s?re, TNF-α bloker tedavisi ald??? s?re, ba?ka imm?ns?presif al?m? olup olmad???na bak?ld?.
Bulgular: ?o?u romatolojik hastal?k tan?s? olan ve anti-TNF tedavi alan hastalarda (n= 134), izoniyazid ile t?berk?loz kemoprofilaksi uygulamas? (profilaksi endikasyonu olan %73.9 hasta) sonras?nda, pulmoner veya ekstrapulmoner t?berk?loz hastal??? geli?memi?tir.
Sonu?: Anti-TNF tedavi verilecek hastalarda, TCT veya Quantiferon ile taramada latent t?berk?loz infeksiyonu tan?s? konulmu?sa, anti-TNF ?ncesi en az bir ay kemoprofilaksi almal?, 9 ay INH veya 4 ay RIF ile t?berk?loz profilaksisi tamamlanmal?d?r. Ayl?k serum karaci?er enzimleri, bilirubin ?l??mleri; 3 ayda bir fizik muayene ve akci?er radyografisi takipleri yap?lmal?d?r.
Anahtar kelimeler: T?m?r nekroz fakt?r?-alfa blokeri; t?berk?loz; profilaksi;
SUMMARY
Latent tuberculosis treatment results in patients that taken Tnf-alpha blockers at Ankara Numune Training and Research Hospital Chest Diseases Clinic for last 8 years (2006-2013)
Introduction: Tuberculosis occurrence was evaluated in patients that applied tuberculosis chemoprophylaxis and currently receiving tumor necrosis factor-alpha (TNF-a) blocker.
Materials and Methods: Incidence of tuberculosis were retrospectively evaluated in patients that currently receiving TNF-α-blocking therapy and received tuberculosis chemoprophylaxis at Ankara Numune Education and Research Hospital, Lung Disease Department, between 2006-2013 years. 134 patients that were diagnosed with rheumatologic and dermatologic diseases, were evaluated. Patients were in the age range 18-80 years. Age, gender, smoking status, BCG vaccination, chest radiography, diagnose of disease, presence of concomitant disease, tuberculosis story, PPD value, chemoprophylaxis acquisition, which anti-tuberculosis agents received, duration of chemoprophylaxis, duration of TNF-α blocker, other immunosuppressive using were measured.
Results: Rheumatologic diseases were often. Prophylaxis has given at 73.9% of patients. Patients with received anti-TNF-α therapy (n= 134) have not developed pulmonary or extra-pulmonary tuberculosis disease.
Conclusion: Patients with received anti-TNF-α therapy, are scanned with TST or Quantiferon. If latent tuberculosis infection are diagnosed, tuberculosis prophylaxis should be started pre-anti-TNF-α therapy at least one month and INH chemoprophylaxis should be completed on 9 months or RIF should be completed on 4 months. Serum liver enzymes and bilirubin measurements monthly; follow-up physical examination and chest radiography should be performed for 3 months.
Key words: Tumor necrosis factor-alpha bloker; tuberculosis; prophylaxis
G?R??
T?m?r nekroz fakt?r?-alfa (TNF-α), polipeptid yap?da, otokrin ve parakrin ?zellikleri olan bir sitokindir. Ba?l?ca monositler ve makrofajlar taraf?ndan ?retilmektedir (1). TNF-α sal?nd??? makrofajlar? ve ?evresindeki di?er imm?n sistem h?crelerini aktive etmekte, di?er sitokinlerin (IL-1, IL-6, IL-8) ve gran?losit-monosit koloni uyar?c? fakt?r?n (GM-CSF) olu?umunu sa?lamaktad?r (2,3). TNF-α, makrofajlardaki nitrik oksit sentetaz? aktive ederek, nitrik oksit yap?m?n? uyar?p makrofajlar?n antibakteriyel etkinli?ini art?rmaktad?r.
TNF-α, immat?r dendritik h?creleri uyar?p, mat?r hale getirir. Bu yolla basillere ait epitoplar?n Th1 h?crelerine sunumlar?na ve h?cresel imm?n yan?t?n olu?mas?na katk?da bulunurlar. Bu nedenle, Mycobacterium tuberculosis'e kar?? olu?turulan h?cresel imm?n yan?tta ?ok ?nemli rol oynamaktad?r. TNF-α, makrofajlar?n apoptozuna yol a?arak t?berk?loz basilinin ortama yay?lmadan yok edilmesini sa?lar. Ayr?ca sitokin ve kemokinin sal?n?m?n? art?rarak, lenfosit proliferasyonu ve inflamasyon b?lgesine lenfositlerin migrasyonuna neden olur. Bunun sonucu olarak, gran?lom olu?ur, yok edilemeyen basiller bu yap? i?inde hapsolarak ?o?almalar? ve yay?lmalar? engellenir (4-6). Gran?lom i?indeki aktive makrofajlar, TNF-α etkisi ile epiteloid h?crelere farkl?la??r, epiteloid h?crelerin f?zyon yaparak dev h?cre olu?turmalar?n? sa?lar. Gran?lomlar?n devaml?l??? da TNF-α'ya ba?l?d?r. TNF-α, t?berk?loz infeksiyonunun kontrol?, gran?lom olu?umu ve devam?n?n sa?lanmas? i?in gereklidir. ?te yandan, TNF-α, y?ksek konsantrasyonlarda eksprese edildi?inde, artm?? mezenkimal h?cre proliferasyonu ve doku matriks metalloproteinazlar?n sal?verilmesiyle sistemik inflamatuvar s?reci tetikler (7). Kronik inflamatuvar yan?t?n devam etmesi sonucunda; romatolojik hastal?klar ba?ta olmak ?zere, otoimm?n, sistemik inflamatuvar hastal?klar olu?ur. Juvenil romatoid artrit, romatoid artrit, ps?riyatik artrit, ankilozan spondilit, ps?riyazis, Crohn ve ?lseratif kolit gibi sistemik inflamatuvar hastal?klar geli?mektedir. Bu nedenle, bu hastal?klar?n tedavisinde, biyolojik ila?lar?n kullan?m? yayg?nd?r. Bunlar i?inde, TNF-α inhibit?r? ila?lar da yayg?n olarak kullan?lmaktad?r. Ba?l?ca anti-TNF ila?lar: Etanersept, infliksimab, adalimumab, golimumab ve sertolizumabd?r. Son 10 y?lda TNF blokeri ila? kullan?m? artm??t?r (8). TNF-α aktivitesinin engellenmesi, gran?lomat?z inflamasyonu bask?lar (9). Bu durumda anti-TNF-α ila?lar bu mekanizmay? bozarak t?berk?loz ba?ta olmak ?zere, f?rsat?? infeksiyonlar?n geli?me riskini art?rmaktad?rlar (8,10).
Anti-TNF-a kullanan hastalarda t?berk?loz geli?me s?kl??? genel pop?lasyona g?re artm??t?r (11-14). T?berk?loz hastal???n?n ?nlenmesi kapsam?nda, anti-TNF-α tedavisi kullan?lacak hastalarda, tedavi ?ncesinde latent t?berk?loz infeksiyonunun belirlenmesi ve kemoprofilaksi karar? a??s?ndan de?erlendirilmelidir (8). Anti-TNF tedavi alan hastalar?n t?berk?loz riski a??s?ndan dikkatli sorgulanmas?, tedavi ?ncesi t?berk?lin cilt testlerinin veya Quantiferon testlerinin yap?lmas?, PPD ≥ 5 mm olan veya Quantiferon pozitif hastalarda kemoprofilaksinin ba?lanmas? ve ard?ndan bir ay sonra anti-TNF tedaviye ba?lanmas? ?nerilir. ?zoniyazidle 9 ay veya rifampisinle 4 ay s?reyle profilaksi ?nerilir (10,15,16). Anti-TNF tedavi s?resince kemoprofilaksi alan hastalara ayl?k kontrollerle yan etki sorgulamas?, karaci?er enzimleri ile bilirubin de?erleri ?l??mleri ve muayeneleri ?nerilmektedir (15).
Bu ?al??man?n amac?, anti-TNF verilen hastalarda t?berk?loz kemoprofilaksi oranlar? ve kemoprofilaksisine ra?men pulmoner veya ekstrapulmoner t?berk?loz geli?me s?kl???n? ara?t?rmakt?r.
MATERYAL ve Metod
G???s hastal?klar? poliklini?ine, Ocak 2006-Aral?k 2013 tarihleri aras?nda ba?vuran, halen anti-TNF alan ve antit?berk?loz profilaksisi alm?? hastalar, t?berk?loz geli?me s?kl??? a??s?ndan retrospektif olarak de?erlendirildi.
Anti-TNF tedavi endikasyonu alan, romatolojik ve dermatolojik hastal?k tan?s? olan; 18-80 ya? aral???nda, 134 hasta ?al??maya al?nd?. T?berk?loz kemoprofilaksi endikasyonu konulanlardan, tedavisi tamamlananlar ?al??maya dahil edildi. Ya?, cinsiyet, sigara i?me durumu, BCG a??s?, akci?er grafisi, anti-TNF endikasyonu olu?turan hastal?k tan?s?, ek hastal?k varl???, ge?irilmi? t?berk?loz hastal???, ailede t?berk?loz hikayesi, PPD de?eri, kemoprofilaksi alma durumu, kemoprofilaksi ba?land??? tarih ve ald??? toplam s?re, anti-TNF ajan ba?land??? tarih, anti-TNF tedavi ald??? s?re, ba?ka imm?ns?presif al?m? olup olmad???na bak?ld?. ?? ayda bir kontrol ama?l? ?ekilen akci?er grafileri de?erlendirildi.
?statistiksel Analiz
Verilerin analizi SPSS 11.5 paket program?nda ger?ekle?tirilmi?tir. Say?mla elde edilen de?i?kenlerde frekans (y?zde), ?l??mle elde edilen de?i?kenlerde ortalama ? standart sapma (SS) [ortanca (minimum-maksimum)] tan?mlay?c? ?l?? olarak verilmi?tir. p< 0.05 istatistiksel olarak anlaml? kabul edilmi?tir.
BULGULAR
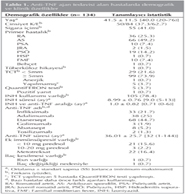
Anti-TNF ajan tedavisi alan 134 hastada ya? ortalamas? 41.5 olup, erkek hasta say?s? belirgin olarak fazlayd?. Primer hastal?k tan?s?nda birinci s?kl?kta %49.2 ile ankilozan spondilit (AS), ikinci s?kl?kta ise %25.3 ile romatoid artrit (RA) g?r?lmekteydi. Ps?riyatik artrit (PSA), juvenil RA (JRA), ps?riyazis, hidradenitis supurativa (HSP), FMF ve Beh?et hastal??? g?r?len di?er hastal?klard?. T?m hastalara ?ocuklukta BCG a??lar? yap?lm??t?. T?berk?loz hikayesi bir ki?ide vard?, daha ?nceden yeterli s?re tedavi alm??t?. TCT, 99 (%73.9) hastada ≥ 5 mm olarak saptand?. T?berk?loz profilaksisinde sadece izoniyazid (INH) kullan?lm??t?. 105 (%78.4) hasta INH alm??t?. Alt? hasta endikasyon d???nda profilaksi alm??t?. Ancak kemoprofilaksi alma nedenleri hakk?nda bilgiye ula??lamad?. INH s?resi ortalama 8.9 ayd?. INH ba?lang?c?ndan 1.0 ? 0.8 ay sonra anti-TNF ajan ba?lanm??t?. Bir hastada ise anti-TNF ba?land?ktan d?rt ay sonra INH ba?lanm??t?. En s?k kullan?lan anti-TNF etanerseptti. Ortalama anti-TNF s?resi 36 ayd?. Hastalar?n %24.6's?nda ek imm?ns?presif ila? kullan?m? mevcuttu. Bu hastalar ek tedavi olarak metotreksat, < 10 mg prednol, baz?lar?nda ise ikisi de kullan?l?yordu. Bir hasta ila? reaksiyonuna ba?l? olarak, bir hastada ise fayda g?rmedi?i i?in ila? de?i?ikli?i yap?lm??t?. T?m hastalara, ?? ayl?k kontrollerinde t?berk?loz semptomlar? a??s?ndan sorgulama, fizik muayene yap?lm??, akci?er grafilerine bak?lm??t?.
Anti-TNF ajan alan ve TCT pozitif saptanan hastalarda t?berk?loz kemoprofilaksisi verilmi?, anti-TNF ald??? s?rece pulmoner ya da ekstrapulmoner t?berk?loz hastal???na rastlanmam??t? (Tablo 1).
Tart??ma
TNF-α, T h?creleri ve makrofajlardan sal?nan, t?berk?loz infeksiyonunun kontrol?, gran?lom olu?umu ve devam?n?n sa?lanmas? i?in gerekli olan bir sitokindir (7). Son 10 y?ld?r, romatolojik hastal?klar ba?ta olmak ?zere yayg?n olarak kullan?lan anti-TNF ila?lar, TNF-α aktivitesini engellemesi sonucunda, gran?lomat?z inflamasyon bask?lan?r (9). Bu durumda t?berk?loz ba?ta olmak ?zere, f?rsat?? infeksiyonlar?n geli?me riskini art?rmaktad?rlar (10).
Anti-TNF ajan kullanan hastalarda pulmoner ve ekstrapulmoner t?berk?loz geli?me s?kl??? genel pop?lasyona g?re artm??t?r (11-14). T?berk?loz hastal???, yayg?nl???ndaki art?? nedeniyle son 20 y?ld?r tekrar g?ndeme gelmi?tir. G?n?m?zde d?nya ?zerinde 2 milyardan fazla birey M. tuberculosis basili ile infektedir. ?nfekte olan bireylerin %10'unda aktif t?berk?loz ortaya ??kmaktad?r (15). D?nya Sa?l?k ?rg?t? (DS?) 2012 raporuna g?re, 2011 y?l?nda 8.7 milyon (%13'? HIV ile birlikte) yeni t?berk?loz hastas? ortaya ??km?? ve buna ba?l? 1.4 milyon hasta ?lm??t?r.
?lkemizde yap?lm?? bir ?al??mada, anti-TNF-α tedavisi kullanan hastalarda t?berk?loz hastal?k s?kl??? %1.1 bulunmu?tur ve genel pop?lasyonla k?yasland???nda yakla??k 23 kat daha y?ksektir (17). Hanta ve arkada?lar?n?n 192 hasta ile yapt??? bir ?al??mada, %67'si kemoprofilaksi alm??, profilaksi almayan 3 ki?i (ppd: 0,14,0 mm) aktif t?berk?loz hastal???na yakalanm??t?r (18). ?nceki ?al??malarda; LTBI taramas? i?in yap?lan, Quantiferon ve TCT testi sonu?lar?ndaki uyum ve farkl?l?klar, kemoprofilaksi endikasyon parametrelerindeki farkl?l?klar ve kemoprofilaksi s?relerinin farkl? olmas?na ba?l? olarak, anti-TNF alan hastalarda t?berk?loz hastal?k s?kl??? artm?? olabilmektedir.
?a?atay ve arkada?lar?n?n 702 hasta ile yapt??? bir ?al??mada, LTBI taramas? TCT ile pozitif olan 583 olguya 9 ayl?k izoniyazid kemoprofilaksisi verilmi?, 6 ki?ide (4 pulmoner, 2 ekstrapulmoner olmak ?zere) t?berk?loz hastal??? geli?mi?tir. Ancak t?berk?loz geli?en t?m hastalarda ?nceden di?er imm?ns?presif tedavi uygulamas? vard?r. Bir hasta kemoprofilaksi almam??, bir di?erinin de ge?mi?te t?berk?loz hikayesi olup, 6 ay INH kemoprofilaksisi alm??t?r (19). Sichletidis ve arkada?lar?n?n yapt??? retrospektif bir ?al??ma da, 6 ay izoniyazid (INH) veya 3 ay INH + Rifampisin (RIF) kemoprofilaksisi alan, anti-TNF tedavi verilen 36 hastan?n 7'sinde t?berk?loz hastal??? geli?ti?i saptanm??t?r. ?? hastada RA, 2 hastada AS, 1 hastada Beh?et ve 1 hastada ps?riyatik artrit vard?r. Be? hastaya infliksimab, 2 hastaya adalimumab tedavisi verilmi?tir (20). Jauregui-Amezaga ve arkada?lar?n?n yapt??? bir ?al??mada da inflamatuvar ba??rsak hastal??? olan ve anti-TNF alan 423 hastadan 30'una 6 ay INH (11 hasta) veya 3-4 ay INH + RIF (19 hasta) olarak LTBI profilaksisi verilmi?tir. Profilaksi verilen hastalardan birinde anti-TNF tedavinin 4. ay?nda ekstrapulmoner t?berk?loz, 6 hastada ise LTBI taramas?nda (tct ve Quantiferon testleri) negatif olmas?na ra?men, anti-TNF al?rken t?berk?loz geli?mi?tir (21). Hastalar?n mevcut hastal?k tan?lar?, hangi anti-TNF ajan ile tedavi verildi?i ve beraberindeki di?er imm?ns?presif tedavilerin varl???, kemoprofilaksiye ra?men t?berk?loz geli?imini etkilemi? olabilir. Ancak T?rkiye'den Kurt ve arkada?lar?n?n yapt??? prospektif ?al??ma da, kemoprofilaksi alanlarda t?berk?loz geli?imi izlenmemi?tir. ?al??mada, romatolojik hastal??? olan 86 hastadan %60.3'? AS, %24.7'si RA, %9.6's? J. RA, %4.1'i PSA idi. 3-36 y?ld?r hastal?k s?releri vard?. %41 hasta (n= 86) ek imm?ns?presif tedavi almaktayd?. ?nfliksimab ve adalimumab %39.7, etanersept %30.1 hastada kullan?lm??t?. LTBI tan?mlanan (tct ≥ 5 mm) 58 hastaya, t?berk?loz kemoprofilaksisi (INH 56 ve RIF 2 hastaya) 9 ay boyunca verilmi?ti. ?ki ayl?k takipler yap?lm??, sonu?ta hi?bir hastada t?berk?loz hastal??? geli?memi?ti (22).
Yapt???m?z ?al??mada ise anti-TNF ajan alan ve TCT pozitif saptanan hastalarda t?berk?loz kemoprofilaksisi verilmi?ti, anti-TNF ald??? s?rece, yap?lm?? di?er bir?ok ?al??man?n aksine, pulmoner ya da ekstrapulmoner t?berk?loz hastal???na rastlanmam??t?. ?al??mam?zda hastalar?n %24.6's?nda ek imm?ns?presif ila? kullan?m? mevcuttu. T?m hastalara ?ocuklukta BCG a??lar? yap?lm??t?. T?berk?loz profilaksisinde sadece izoniyazid (INH) kullan?lm??t?. INH s?resi ortalama 8.9 ayd?. INH ba?lang?c?ndan 1.0 ? 0.8 ay sonra anti-TNF ajan ba?lanm??t?. En s?k kullan?lan anti-TNF etanerseptti. T?berk?loz profilaksi s?resinin ?nerilen s?reye tamamlanmas?, TNF-alfa blokeri tedavisinden bir ay ?ncesinde profilaksiye ba?lanmas?, ek imm?ns?presif tedavi kullan?m? s?kl???n?n az olmas?, en s?k etanersept kullan?lm?? olmas?, di?er ?al??malarda elde edilen sonu?lar?n aksine t?berk?loz hastal??? geli?me s?kl???n? ?nemli ?l??de azaltm??, ortadan kald?rm?? olabilir. Hastalar?n anti-tnf tedavi ?ncesi de?erlendirilmeleri ve sonraki takiplerinin ilgili b?l?m ve g???s hastal?klar? birimleri ile beraber, d?zenli yap?lmas?, rol al?yor olabilir.
Bu alanda daha fazla prospektif, ?ok merkezli ?al??malara ihtiya? vard?r. Belki gelecekte, ?u anda faz ?al??malar? devam eden t?berk?lozdan koruyucu a??larla, LTBI a??s?ndan da korunma sa?lanabilir. DS? 2020 y?l?nda en az bir yeni a?? i?in ?al??malar?n tamamlan?p, lisans al?nabilece?ini ?ng?rmektedir (23).
Sonu? olarak, anti-TNF tedavi verilecek hastalarda, quantiferon veya TCT ile taramada latent t?berk?loz infeksiyonu tan?s? konulmu?sa, anti-TNF ?ncesi en az bir ay kemoprofilaksi almas?, dokuz ay INH veya 4 ay RIF ile t?berk?loz profilaksisinin tamamlanmas?, ayl?k karaci?er enzim ve bilirubin kontrolleri ve ?? ayda bir fizik muayene, akci?er radyografisi takipleri yap?lmal?d?r.
?IKAR ?ATI?MASI
Bildirilmemi?tir.
KAYNAKLAR
- Camussi G, Albano E, Tetta C, Bussolino F. The moleculer action of tumor necrosis factor-alpha. Eur J Biochem 1991;202:3-14.
- Haworth C, Berennan FM, Chantry D, Turner M, Maini RN, Feldmann M. Expression of granulocyte-macrophage colony stimulating factor in rheumatoid arthritis: regulation by tumor necrosis factor-a. Eur J Immunol 1991;21:2575-9.
- Butler DM, Maini RN, Feldmann M, Brennan FM. Modulation of proinflammatory cytokine release in rheumatoid synovial membrane cell cultures: comparison of monoclonal anti-TNF-antibody with interleukin-1 receptor antagonist. Eur Cytokine Netw 1995;6:225-30.
- Gardam MA, Keystone EC, Menzies R, Manners S, Skamene E, Long R,? et al. Anti-tumour necrosis factor agents and tuberculosis risk: mechanisms of action and clinical management. Lancet Infect Dis 2003;3(3):148-55.
- Keane J, Gershon S, Wise RP, Mirabile-Levens E, Kasznica J, Schwieterman WD,? et al.? Tuberculosis associated with infliximab, a tumor necrosis factor alpha-neutralizing agent. N Engl J Med? 2001;345(15):1098-104.
- Stenger S, Modlin RL. Control of Mycobacterium tuberculosis through mammalian Toll-like receptors. Curr Opin Immunol 2002;14:452-7.
- Shingu M, Nagai Y, Isayama T, Naono T, Nobunaga M, Nagai Y. The effects of cytokines on metalloproteinase inhibitors (TIMP) and collagenase production by human chondrocytes and TIMP production by synovial cells and endothelial cells. Clin Exp Immunol 1993;94:145-9.
- Nordgaard-Lassen I, Dahlerup JF, Belard E, Gerstoft J, Kjeldsen J, Kragballe K, et al. Danish Society for Gastroenterology. Guidelines for screening, prophylaxis and critical information prior to initiating anti-TNF-alpha treatment. Dan Med J 2012;59(7):C4480.
- Male D, Brostoff J, Roth DB, Roitt I. Immunology. 7. Bask?. ?eviri: Turgut ?mir, Ankara: Palme Yay?nc?l?k, 2008:129-130,485-7.
- John H, Buckley C, Koh L, Obrenovic K, Erb N, Rowe IF. West Midlands Rheumatology Service and Training Committee. Regional survey of tuberculosis risk assessment in rheumatology outpatients commencing anti-TNF-alpha treatment in relation to British Thoracic Society guidelines. Clin Med 2009;9(3):225-30.
- Brassard P, Kezouh A, Suissa S. Antirheumatic drugs and the risk of tuberculosis. Clin Infect Dis 2006;43(6):717-22.
- Tubach F, Salmon D, Ravaud P, Allanore Y, Goupille P, Br?ban M,? et al.; Research Axed on Tolerance of Biotherapies Group.
- Abreu C, Magro F, Santos-Antunes J, Pil?o A, Rodrigues-Pinto E, Bernardes J, et al. Tuberculosis in anti-TNF-α treated patients remains a problem in countries with an intermediate incidence: Analysis of 25 patients matched with a control population. J Crohns Colitis 2013;7(10).
- Hazlewood GS, Naimark D, Gardam M, Bykerk V, Bombardier C. Prophylaxis for latent tuberculosis infection prior to anti-TNF therapy in low-risk elderly patients with rheumatoid arthritis: A decision analysis. Arthritis Care Res (Hoboken). 2013.
- ?zkara ?, Bilgi? H, Karada? M. T?berk?lozda koruyucu tedavi. T?berk?loz Kitab?. 2010:592-3.
- ?zkara ?, Akta? Z, ?zkan S, Ecevit H. T?rkiye'de T?berk?lozun Kontrol? ??in Ba?vuru Kitab?. 2003
- Do?an C, K?ral N, ?ener C?mert S, Fidan A, ?a?layan B, Salep?i B. Tuberculosis frequency in patients taking TNF-alpha blokers. 2012;13(3):93-8.
- Hanta I, Ozbek S, Kuleci S, Kocabas A. The evaluation of latent tuberculosis in rheumatologic diseases for anti-TNF therapy: experience with 192 patients. Clin Rheumatol 2008;27:1083-6.
- Cagatay T, Aydin M, Sunmez S, Cagatay P, Gulbaran Z, Gul A, et al. Follow-up results of 702 patients receiving tumor necrosis factor-α antagonists and evaluation of risk of tuberculosis. Rheumatol Int 2010;30(11):1459-63.
- Sichletidis L, Settas L, Spyratos D, Chloros D, Patakas D, Tuberculosis in patients receiving anti-TNF agents despite chemoprophylaxis. Int J Tuberc Lung Dis 2006;10(10):1127-32.
- Jauregui-Amezaga A, Turon F, Ord?s I, Gallego M, Feu F, Ricart E, et al. Risk of developing tuberculosis under anti-TNF treatment despite latent infection screening. J Crohns Colitis 2013;7(3):208-12.
- Kurt OK, Kurt B, Talay F, Tug T, Soy M, Bes C, et al. Intermediate to long-term follow-up results of INH chemoprophylaxis prior to anti-TNF-alpha therapy in a high-risk area for tuberculosis. Wien Klin Wochenschr 2013;125(19-20):616-20.
- Global Tuberculosis Report: Tuberculosis-Epidemiology. WHO report 2012.
Yaz??ma Adresi (Address for Correspondence)
Dr. Sema DEM?R
Ankara Numune E?itim ve Ara?t?rma Hastanesi,?
G???s Hastal?klar? Klini?i,
ANKARA - TURKEY
e-mail: drsemad@yahoo.com