REVIEW
Doi: 10.5578/tt.7425
Tuberk Toraks 2014;62(3):236-242

Warfarin doz? ayarlanmas?nda genetik varyasyonlar?n etkisi
G?lbahar DARILMAZ Y?CE1
1 D??kap? Y?ld?r?m Beyaz?t E?itim ve Ara?t?rma Hastanesi, G???s Hastal?klar? Klini?i, Ankara, T?rkiye
1 Clinic of Chest Diseases, Diskapi Yildirim Beyazit Training and Research Hospital, Ankara, Turkey
?ZET
Warfarin doz ayarlanmas?nda genetik varyasyonlar?n etkisi
Warfarin en yayg?n kullan?lan oral antikoag?land?r. Dar bir terap?tik indekse sahiptir, bu nedenle, warfarin alan hastalarda antikoag?lan yan?t s?k kontrol gerektirir. Ya?, cinsiyet, komorbiditeler, birlikte al?nan ila?lar?n yan? s?ra farmakokinetik ve farmakogenetik genlerdeki varyasyonlar da warfarin dozunu etkilemektedir. VKORC1 ve CYP2C9 warfarin metabolizmas?ndan sorumlu iki gendir. G?n?m?zde warfarin metabolizmas?ndaki ?nemleri ve klini?e yans?malar? yeterince bilinmemektedir. Bu genlerdeki polimorfizmler warfarine yan?tta duyarl?l??a ve a??r? antikoag?lasyona hatta hemorajik komplikasyonlara neden olmaktad?r. Genetik polimorfizm ara?t?rmas? ?zellikle uluslararas? normalle?tirilmi? oran (INR) d?zeyi ayarlanamayan hastalarda faydal? olmaktad?r. Farkl? ?rklarda ve toplumlarda bu iki genin s?kl??? da farkl?d?r. Bu durum warfarine yan?tta ?e?itlili?e neden olmaktad?r. G?n?m?zde warfarin dozu ayarlan?rken halen geneti?in rol? g?z ard? edilmektedir. Bu polimorfizmler i?in genetik analiz yapman?n hasta takibi ve maliyete sa?layaca?? katk?lar halen tart??mal?d?r. Bu konuyla ilgili Amerika ve Avrupa'da yap?lmakta olan ?ok merkezli ?al??malar devam etmektedir.
Anahtar kelimeler: Genetik varyasyon, warfarin, CYP2C9, VKORC1
SUMMARY
Effect of genetic variations on adjusting of warfarin dose
Warfarin is the most widely used oral anticoagulant. Since it has a limited therapeutics index, anticoagulant reaction is mostly needed to be controlled in patients taking warfarin. Besides age, gender, medicines taken with comorbidities, the variations in pharmacokinetics and pharmacogenetic genes also affect the dose of warfarin. VKORC1 and CYP2C9 are two genes responsible for warfarin metabolism. Today the importance and clinical effects of warfarin in metabolism are not known sufficiently. The polymorphisms in these genes cause sensitivity and over anticoagulant even hemorrhagic complication in warfarin reaction. Genetic polymorphism research is beneficial especially in patients where international normalized ratio (INR) level cannot be adjusted. The frequency of these genes is also different in different races and populations. This condition causes variety in warfarin reaction. Today the role of genetics is still ignored in adjusting warfarin dose. The contributions of doing genetic analysis for polymorphisms to patient follow ups and expenditure are still contradictive. Multicentric studies about this subject are going on in the USA and Europe.
Key words: Genetic variations, warfarin, CYP2C9, VKORC1
G?R??
Wisconsin Mezunlar? Ara?t?rma Vakf? taraf?ndan ke?fedilen warfarin, 1950'li y?lllarda piyasaya s?r?ld???nden beri yayg?n olarak kullan?lan oral antikoag?land?r (1,2). G?n?m?zde geli?mi? d?nya n?fusunun %1-2'si bu oral antikoag?lan? d?zenli olarak almaktad?r (1). Derin ven trombozu, pulmoner embolizm, mekanik kapak replasman?, atriyal fibrilasyon ve inme profilaksisinde kullan?lmaktad?r (3).
Warfarin kullanan hastalar terap?tik doza ula?abilmek i?in 10 mg ile 100 mg/hafta gibi geni? bir doz aral???nda ila? kullanmak zorundad?r (4). Dar bir terap?tik indekse sahip olan warfarin subterap?tik dozda p?ht? olu?umu ve supraterap?tik dozda kanama olu?umuna neden olur (1). Bu nedenle, warfarin alan hastalar?n yak?n izlemi gerekir. Bu durum sa?l?k sistemleri i?in pahal? bir yat?r?m, hastalar i?in de rahats?zl?k yarat?r. 2006 y?l?nda Amerika Birle?ik Devletleri (ABD)'nde acil servise warfarin kullan?m?na ba?l? yan etkiler nedeniyle 36.000 ki?i ba?vurmu?tur (5). Hemorajik olay g?r?lme oran? %12'dir ve bunlar?n %2'si mortal seyreder (6). Warfarin tedavisinin ilk ay?ndaki kanama riski, ilk y?ldan sonraki riske g?re 10 kat daha fazlad?r. Kanamalar s?kl?kla gastrointestinal sistem, yumu?ak doku ve ?riner sistemden olmaktad?r (7). Warfarin tedavisi s?ras?nda maj?r kanama olaylar?n?n insidans? RE-LY (Uzun S?reli Antikoag?lasyon Tedavisinin Randomize De?erlendirmesi) ?al??mas?na g?re, hasta ba??na y?lda ortalama %3.36'd?r (8). ?leri ya?, kad?n cinsiyet, kontrols?z hasta, y?ksek dozda antikoag?lan kullan?m?, ek hastal?klar ve e? zamanl? ila?lar?n hemorajik komplikasyonlar? art?rd???, d???k beden kitle indeksi (BK?) olanlarda daha d???k doz gerekti?i bilinmektedir (3,9). Diyet de warfarin metabolizmas?n? etkilemektedir (10). Ayr?ca, karaci?er hastal???, hipertiroidizm ve kalp yetmezli?inin de ilaca hassasiyeti art?rd??? tespit edilmi?tir (1). Tedavi etkinli?i ve warfarinin g?venli kullan?m? protrombin zaman? ve uluslararas? normalle?tirilmi? oran (INR) ile takip edilir (3,11). Terap?tik seviyeleri a?an INR de?erleri kanama riskinin artmas?na neden olmaktad?r. INR de?erleri terap?tik seviyenin alt?nda ise, tromboembolik olaylarda art?? olmaktad?r (12). Tedavi ba?lang?c?nda herhangi bir hasta i?in optimal doz belirsiz oldu?undan tedaviye genelde ampirik dozda ba?lan?r. Bu d?nemde a??r? antikoag?lasyon veya hemoraji geli?me riski y?ksektir (13).
Son 10 y?lda warfarin dozundaki ?e?itliliklerin warfarin metabolizmas? ve aktivitesinden sorumlu genlere ait varyasyonlardan dolay? meydana geldi?i ve ?e?itlili?in %40'?ndan sorumlu oldu?una ili?kin kan?tlar elde edilmi?tir (3). Farmakokinetik ve farmakogenetik genlerdeki varyasyonlar warfarin dozunu etkilemektedir (4).
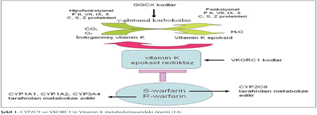
Warfarin, koag?lasyon fakt?rlerinden 2, 7, 9, 10'un gama-karboksilasyonunu engelleyerek aktivasyonlar?n? ?nlemektedir (7). Vitamin K'n?n inaktif formu olan Vitamin K epoksit, Vitamin K epoksit red?ktaz (VKOR) enzimi ile indirgenmi? Vitamin K'ya [Vitamin K (H2)] d?n??t?r?l?r. VitKH2 proton kayna?? sa?layarak, fakt?r 2, 7, 9, 10'un gama-glutamil karboksilaz enzimi ile gama-glutamil karboksilasyona u?ray?p fonksiyonel olmalar? i?in kataliz?r g?revi g?r?r. Warfarin taraf?ndan VKOR enzimi bloke edilerek Vitamin K'n?n indirgenmi? haline d?n???m? inhibe edilir (3,7) (?ekil 1).
Klinik olarak kullan?lan warfarin %50 R-warfarin ve %50 S-warfarinin rasemik bir kar???m?d?r. Sitokrom p450 2C9 S-warfarininin aktif metabolitleri olan 6-hidroksi-S-warfarin ve 7-hidroksi-S-warfarine d?n???m?n? katalize eder. R-warfarin metabolizmas?ndan sorumlu olan sitokrom P4501A2, 2C19 ve 3A4R-warfarininin aktif metabolitleri olan 6-hidroksi-R-warfarin ve 7-hidroksi-R-warfarine d?n???m?n? katalize eder. S-warfarinin metabolik eliminasyonu R-warfarinden ?? kat daha h?zl?d?r. R-warfarinle kar??la?t?r?ld???nda S-warfarin VKOR enzim inhibit?r? olarak be? kat daha aktiftir (3,7).
Sitokrom P450 (CYP) endojen steroidleri, yabanc? kimyasal madde ve ila?lar? metabolize eden bir enzim s?per ailesidir. Bu ailenin, bir ?yesi olan CYP2C9, warfarin metabolizmas?nda ?nemlidir (1). Hepatik CYP2C9 warfarinin daha aktif izomeri olan S-warfarinin metabolizmas?ndan sorumludur. CYP2C9'un aktivitesinde azalmaya sebep olan birka? CYP2C9 polimorfizmi saptanm??t?r. Bu azalm?? serum aktivitesi warfarin seviyelerinde artmaya neden olur. Bu da terap?tik INR'ye ula?mak i?in daha d???k dozlar?n yeterli olmas?n? sa?lar, b?yle hastalarda, di?er hastalarda normal olan dozlar kanamaya neden olabilir (7). CYP2C9 genindeki polimorfizm d???nda warfarin dozunu etkileyen di?er genetik varyasyon Vitamin K metabolizmas?ndan sorumlu VKORC1 genindeki polimorfizmlerdir. Warfarin doz ?e?itliliklerinin yakla??k olarak %30'u bu iki polimorfizmden dolay? olmaktad?r (4). Aithal ve arkada?lar? ilk olarak 1999 y?l?nda CYP2C9 gen varyantlar?n?n warfarin metabolizmas?nda de?i?ikliklere neden oldu?unu bulmu?lard?r (15). VKORC1 gen varyantlar? ise 2004 y?l?nda saptanm??t?r (16) (Tablo 1).
CYP2C9 geni 10. kromozomun q23.33 band?nda yerle?mi?tir. Klinik olarak ?nemli olan polimorfizmleri 430, 818 ve 1075 pozisyonlar?nda bulunur. *2 olarak bilinen 430. pozisyonda sitozin yerine timin gelmesiyle olu?an polimorfizm (430C > T, rs1799853) arjinin yerine sisteinin geldi?i bir protein kodlar, *3 olarak bilinen 1075. pozisyonda adenin yerine sitozin gelmesiyle olu?an polimorfizm (1075A > C, rs1057910) izol?sin yerine l?sinin geldi?i bir protein kodlar (1,7). Enzim aktivitesi *2 genotipi i?in, %30 azal?rken, *3 genotipi i?in %80 azal?r (1). Hem *2 hem de *3 allelleri S-warfarinin normal allele g?re s?ras?yla %12 ve %5 daha az olan bozulmu? hidroksilasyonuyla sonu?lan?r. Bu varyasyonlar warfarinin degradasyonu ve klerensini azalt?r. Bundan dolay? terap?tik INR elde etmek i?in d???k bir doz yeterli olur (3). *6 olarak bilinen 818. pozisyonda adenin delesyonuyla olu?an polimorfizm (818 delA, rs9332131) azalm?? enzim aktivitesiyle ili?kilidir. Ayr?ca, 19. kromozom q13.12 lokalizasyonunda yerle?mi? olan normal CYP4F2 varyant? (7253232 C > T rs2108622) olan polimorfizm de warfarin metabolizmas?n? etkiler (7).
VKOR enzimini kodlayan VKORC1 16. kromozom p 11.2'de bulunmaktad?r. VKORC1'in transkripsiyonu ba?l?ca karaci?erde, daha az olarak da kalp ve pankreasta yap?lmaktad?r (7). VKORC1 promoter b?lgesindeki polimorfizm 1639. pozisyondaki guanin yerine adenin gelmesiyle meydana gelir (17). 1639 A alleli VKORC1 mRNA'n?n azalm?? ?retimi ve VKOR enziminin azalm?? ekspresyonuyla sonu?lan?r (18). Bu hastalarda daha d???k warfarin dozlar?yla terap?tik INR'ye ula??l?r. Di?er hastalar i?in normal olan dozlar kanamaya neden olabilir.
Bir meta-analizde ?zellikle CYP2C9 varyantlar?n?n (*2 ve *3) belirgin olarak hemorajik komplikasyonlarla ili?kili oldu?u, CYP2C9 *2 ile kar??la?t?r?ld???nda *3'?n warfarinin hemorajik komplikasyonlar? i?in daha g??l? bir risk fakt?r? oldu?u belirtilmi?tir (2). ?inlilerde yap?lan bir ?al??mada; VKORC1 polimorfizmlerinin CYP2C9 polimorfizmlerine g?re, warfarine erken yan?t? daha ?ok etkiledi?i bulunmu?tur.VKORC1 mutant genotipleri antikoag?lasyonun erken d?nemlerinde warfarine daha duyarl?d?r, bu genotiplerde antikoag?lan tedavinin ilk a?amas? en zorlu ad?m olmaktad?r (19).
Kafkaslarda yap?lan bir ?al??mada genotip idame dozundaki de?i?kenlikten %19.8 sorumluyken, ya?, v?cut y?zey alan? ve erkek cinsiyet s?ras?yla %14.6, %7.5 ve %4.7, sorumlu olarak bulunmu?tur (20). Kuzey Amerikan toplumunda warfarin doz gereksinimi CYP2C9 *2 i?in %19, *3 i?in %30, ya??n her 10 y?l? i?in %8, v?cut y?zey alan?ndaki standart deviasyondaki azalma ba??na %13, amiodaron alan (warfarin metabolizmas?n? g??l? ?ekilde inhibe eder) hastalarda %29, simvastatin alan hastalarda %12, beyazlarda Afrika k?kenli Amerikal?larla kar??la?t?r?ld???nda %11 daha az olarak hesaplanm??t?r. Bu fakt?rler ve cinsiyetin dahil oldu?u verilerin analizi sonucunda warfarin idame dozunda varyans?n %39 oldu?u a??klanm??t?r (21). ABD'de poliklinikte yap?lan prospektif bir ?al??mada warfarin dozu hakim belirleyicisi olarak ya?, kilo ve cinsiyetin %12 oran?nda etkili olmas?na kar??n genotip %33 ile dominant fakt?r olarak belirtilmi?tir (22). Bu verilere g?re warfarin doz gereksiniminde genetik fakt?rler; ya?, BK?, cinsiyet ve e?lik eden ila?lardan daha ?nemlidir.
Warfarinin allel s?kl?klar?na g?re ortalama g?nl?k idame dozlar? Hintli bir pop?lasyonda VKORC1-1639 GG ve 1173 CC (wild-tip) i?in 4.72 mg/g?n, VKORC 1-1639 GA ve 1173 CT (heterozigot) allelleri i?in 3.74, VKORC1-1639 AA ve 1173 TT (homozigot) alleleri i?in 2.07, CYP2C9 *1/*1 (wild-tip) i?in 4.46, CYP2C9 *1/*2 (heterozigot) allel i?in 4.5, CYP2C9 *2/*2 (homozigot) allel i?in 2.85 bulunmu?tur (3). T?rk pop?lasyonunda VKORC1 -1639 GG (wild-tip) i?in 5.95 ? 2.12, VKORC 1-1639 GA i?in 3.29 ? 1.72 ve VKORC1-1639 AA i?in 2.49 ? 1.11, CYP2C9 *1/*1 (wild-tip) i?in 4.74 ? 2.49, CYP2C9 *1/*2 (heterozigot) allel i?in 3.71 ? 1.76, CYP2C9 *1*3/*2*3 allelleri i?in 3.32 ? 1.92 bulunmu?tur (11). Kafkaslarda CYP2C9 *1*1, *1*2, *1*3, *2*2, *2*3 ve *3*3 genotiplerinin ortalama idame dozlar? s?ras?yla 36.5, 29.1, 23.5, 28.0, 18.1 ve 5.5 mg/hafta olarak hesaplanm??t?r (20). Bu bulgular g?nl?k warfarin dozunun VKORC1 ve CYP2C9 normal allele sahip hastalarda en y?ksek, polimorfizmlerde ise; heterozigotlukta normal allelden daha az, homozigotlukta en az oldu?unu g?stermektedir.
Farkl? ?rklarda ve toplumlarda bu iki genin s?kl??? da de?i?mektedir. Son y?llarda warfarin yan?t?na farkl?l?kta etnik topluluklar?n temel genetik mod?lat?r oldu?u belirtilmektedir. Toplam 453 kafkas hastan?n CYP2C9 genotip s?kl???n?n incelendi?i ?al??mada *1*1, *1*2, *1*3, *2*2, *2*3 ve *3*3 genotiplerinin toplumda g?r?lme s?kl??? s?ras?yla %65, %19, %12, %1.6, %1.8 ve %0.4 bulunmu?tur (20). ?in pop?lasyonunda CYP2C9 *1*1 genotip s?kl??? %95, *1*3 %5 ve *3 *3 %0 olup, *2, *4 ve *5 varyantlar?n?n da olmad??? bildirilmi?tir (23). Kafkaslarda VKORC1 allelleri GG, AG, AA %39, %47 ve %14 mevcut iken, ?inli hastalarda ise %2.7, %17.6 ve %79.7 olup, anlaml? olarak farkl? oldu?u rapor edilmi?tir. ?inli hastalarda VKORC1 polimorfizminin daha yayg?n ve homozigotlu?un fazla g?zlenmesinden dolay? benzer derecede antikoag?lasyona eri?mek i?in ?inliler kafkaslardan daha d???k doz warfarin gerektirmektedir (17). Hintlilerde CYP2C9 *2 varyant allel n?fusun %5.4'?nde mevcut iken *3 varyant allel tamamen yok olarak bulunmu?tur (3). VKORC1 varyant alleli Hintlilerde n?fusun %14-19'unda mevcut olup, di?er Asyal?larda oldu?undan daha azd?r (24). CYP2C9 allel s?kl??? Avrupa k?kenli Amerikal?larda *2 ve *3 i?in s?ras?yla %11.24 ve %5.1, Afrika k?kenli Amerikal?larda %1.1 ve %1.8 olup, polimorfizm s?kl??? Avrupa k?kenlilerde Afrika k?kenlilere g?re fazlad?r, bu nedenle CYP2C9 polimorfizmi warfarin dozunu ?ng?rmede Avrupa k?kenlilerde ?nemliyken, Afrika k?kenlilerde ?nemsizdir (25). VKORC1 *2 allel s?kl??? Afrika k?kenli Amerikal?larda %14, Avrupal?larda %42'dir (26).
T?m Asyal?larda VKORC1 polimorfizmi %90-95 civar?nda g?r?lmektedir (27,28). Bu nedenle Asyal? hastalar warfarinle antikoag?lasyona kar?? daha duyarl?d?r (29). Asyal?lar aras?nda da, Hintliler; ?inliler, Japonlar ve Malaylardan daha y?ksek dozlar gerektirir (3). ?inliler de Kafkaslardan daha d???k doz gerektirmektedir (17). Afrikal? Amerikal?lar warfarine daha duyarl? olan Kafkas ve Asyal?lara g?re daha y?ksek dozlara gereksinim duyar (3). ?zet olarak, siyah pop?lasyonda warfarin doz gereksinimi en y?ksek, beyaz pop?lasyonda orta derece, Asyal?larda en d???k olmaktad?r (1).
T?rk n?fusu, Avrupa ve Asya k?kenli farkl? etnik gruplardan olu?maktad?r. T?rk toplumunda CYP2C9 ve VKORC1 allel s?kl??? ve gen polimorfizmlerinin warfarin doz gereksinimleri ?zerine etkileri hakk?nda yay?nlanan birka? ?al??ma vard?r (11,30-32). Toplam 100 stabil T?rk hastada yap?lan ?al??mada warfarin ortalama g?nl?k idame dozu 4.1 mg/g?n ve warfarin doz gereksinimi 1.16 ile 9.33 mg/g?n, aras?nda b?y?k farkl?l?klar g?stermi?tir. Polimorfizmler i?in varyant allel frekanslar? VKORC1 A %40, CYP2C9 *2 %13, *3 %15 olup, di?er bir T?rk pop?lasyonu ?al??mas?nda ayn? genotipler i?in s?kl?klar s?ras?yla %50, %13'e %10 bulunmu?tur (11,32). T?rkiye'den yap?lan ?al??malarda allel s?kl??? sonu?lar? birbiriyle uyumludur. Ayr?ca T?rk hastalar?n sonu?lar?, Asya ve Afrika k?kenli Amerikal?lardan farkl? olup, en ?ok Kafkas pop?lasyonuyla benzemektedir (11). T?rk hastalarda VKORC1 ve CYP2C9 polimorfizmlerinin haftal?k warfarin dozunda %40'l?k bir azalmaya neden olmas? dikkat ?ekicidir (32).
2007 A?ustos ay?nda, "Food and Drug Administration (FDA)" CYP2C9 ve VKORC1 polimorfizmleri olan belirlenmi? hastalarda warfarin i?in d???k ba?lang?? dozlar? kullan?lmas? gerekti?ini belirtmi?tir. FDA warfarin tedavisi ba?lanmadan ?nce bu genetik varyantlar i?in test yap?lmas?n? ve ?r?n etiketlerinde farmakogenetik bilgi verilmesi gerekti?ini ?nermektedir (19,33).
D??ER GENLERDEK? POL?MORF?ZMLER
CYP4F2'nin K vitamini ve warfarin metabolizmas?ndaki yola?? tam olarak bilinmemektedir. Warfarin dozu ?zerinde %1-2'lik k???k bir etkisi vard?r. TT homozigot allelde, CC homozigot allele g?re 1 mg/g?n daha fazla warfarin ihtiyac? olmaktad?r (34).
Apolipoprotein E (APOE) karaci?erde K vitamini bak?m?ndan zengin lipoproteinlerin resept?re spesifik al?m?na arac?l?k eden, lipidlerin ta??nmas?nda yer alan plazma lipoproteinlerinin ?nemli bir bile?enidir. APOE genindeki polimorfizmin de kumarinler i?in doz gereksinimini etkiledi?i g?sterilmi?tir. APOE'yi kodlayan ?? allel vard?r: ε2, ε3 ve ε4. Doz ayarlanmas?nda farkl? allelik varyantlar?n etkileri toplumdaki s?kl???na ba?l?d?r. ?rne?in; Ε4 genotipi warfarin doz gereksinimi i?in k???k bir katk?da bulunmaktad?r, bu durumda bu genotipin frekans? Asyal?larda beyazlar ve Afrikal? Amerikal?lardan daha d???k oldu?u i?in klinik olarak anlaml? de?ildir (35).
Gamma-glutamilkarboksilaz (GGCX) vitamin K d?ng?s?n?n ?nemli bir bile?eni oldu?u i?in, bu genin polimorfizmi de ?nemlidir. Avrupa pop?lasyonunda, pozisyon 12970'te tek gen polimorfizmi (rs11676382) warfarin dozunda toplam varyans?n %2'sini a??klarken s?ras?yla VKORC1 ve CYP2C9 ise varyans?n %21 ve %8'ini a??klamaktad?r (36).
Trans-hidrodioller i?in epoksitlerin hidrolizinden sorumlu olan ve vitamin K 2,3-epoksit ba?lanma b?lgesi gibi davranan mikrozomal epoksit hidrolaz, ayn? zamanda, iki polimorfizmi tespit edilmi? olan bir gen taraf?ndan kodlan?r (1).
Calumenin bir kalsiyum iyonu ba?lanma proteinidir. A??r? ekspresyonu oldu?u zaman, VKOR'a ba?lan?r ve inhibe eder. Bu, ayn? zamanda karboksilaz enzimine, vitamin K'n?n, indirgenmi? formunun transferini ?nler. Antikoag?lan kullanan bir pop?lasyonunda, warfarin doz gereksinimi mikrozomal epoksit hidrolaz ve calumenin genlerinin polimorfizminden etkilenmemi?tir (1).
Toplam 550.000 polimorfizmin test edildi?i retrospektif bir ?al??ma warfarin doz gereksiniminde en belirgin olarak VKORC1, orta derecede CYP2C9 *2 ve *3 polimorfizmlerinin etkili oldu?unu ortaya koymu?tur. Bu ?al??mada GGCX, ?e?itli farkl? p?ht?la?ma fakt?rleri, mikrozomal epoksit hidrolaz, di?er CYP2C9 sitokrom P450 izoformlar?, baz? glutatyon-S-transferaz izoformlar?, APOE ve protein C kodlayan di?er genlerin ?ok az ya da hi? katk?s?n?n olmad??? ortaya ??km??t?r (1).
Ampirik yakla??m?n savunucular? farmakogenetik k?lavuzlu?unda doz algoritmas?ndansa daha iyi hasta e?itimi ve daha yak?n takip ile dozlama do?rulu?unun art?r?labilece?ini savunmaktad?rlar. Toplam 1015 hastan?n tedavinin ilk d?rt haftas?nda incelendi?i bir ?al??mada warfarinin genotip tabanl? dozlamas?n?n yarar? g?sterilememi?tir (37).
D?rt k?ta (Asya, Avrupa, Kuzey Amerika ve G?ney Amerika) dokuz ?lke, 21 merkez bilim insanlar?ndan olu?an Uluslararas? Warfarin Farmakogenetik Konsorsiyumu (IWPC), 4043 hastadan gelen (klinik ve genetik) verilerle warfarin dozunun do?ru tahmin edilmesi i?in bir algoritma geli?tirmi?tir. Doz tahmininin do?rulu?u 1009 hastal?k bir do?rulama kohortu ile de?erlendirilmi?tir. Do?rulama kohortunda hedef INR'ye eri?mek i?in d???k ya da y?ksek doz gereken hastalar (haftal?k 21 mg ya da daha az, 49 mg ya da daha fazla) b?y?k oranda do?ru tan?mlanm??t?r. En b?y?k faydas? d???k ve y?ksek doz alan hastalarda g?zlenmi?tir (1).
Farmakogeneti?e dayal? dozlaman?n hasta sonu?lar?n? geli?tirip geli?tirmeyece?ini de?erlendirmek amac?yla halen iki b?y?k, prospektif, ?ok merkezli (ABD'de ve Avrupa'da), randomize, klinik ?al??ma s?rd?r?lmektedir. Genetik yoluyla optimal antikoag?lasyonun ayd?nlat?lmas? olarak adland?r?lan ABD deneyi (COAG), Ulusal Kalp Akci?er ve Kan Enstit?s? taraf?ndan finanse edilmektedir. On iki klinik alandan farkl? etnik k?ken ve ge?mi?ten olan 1200 hasta de?erlendirilecektir. Hastalar?n yar?s? tek ba??na klinik bilgilere g?re randomize olacak ve di?er yar?s? IWPC taraf?ndan geli?tirilen denkleme g?re dozlanacakt?r. T?m hastalar alt? ay boyunca izlenecektir. Avrupa deneyi Kumarin Tedavisine Farmakogenomik Yakla??m (EU-PACT), olarak adland?r?lm??t?r. Yedi ?lkeden 13 merkez bu ?al??mada yer almaktad?r. ?al??ma Avrupa Komisyonu FP7 program? taraf?ndan desteklenmektedir. Her bir coumarin kolu i?in 1000 hasta ?al???lacakt?r. EU-PACT deneyi CYP2C9 ve VKORC1 genotiplemesi i?in h?zl? ve ucuz bir nokta-bak?m testi kullanmaktad?r (HyBeacon? technology). Genotip-leme yeni tan?l? bir hastada 1 saat i?inde kullan?labilir hale getirilmi?tir (1).
Sonu? olarak, warfarin dozu ile CYP2C9 ve VKORC1 genleri aras?ndaki ili?ki ?ok say?da ?al??ma ile kan?tland??? gibi, art?k tart???lmazd?r. FDA taraf?ndan da bu genlerde varyasyonlar? olan hastalar i?in warfarine d???k dozlarda ba?lanmas? gerekti?i ?nerilmi?tir. Geneti?in hekimleri uyarmadaki yarar? ve FDA ?nerisine ra?men, warfarin doz do?rulu?unu d?zeltmek i?in genetik bilginin nas?l kullan?laca?? bilinmemektedir. ?deal doz algoritmas? hedefi a?madan ya da yetersiz antikoag?lasyon olmaks?z?n kanama ve tromboemboli komplikasyonlar?n? ?nlemeli, INR izleme s?kl???n? ve belirsizli?i azaltmal?d?r. Geneti?e dayal? dozlama tedaviye ba?lanmadan ?nce yap?l?r ise yararl? olarak ?nerilmektedir. G?n?m?zde farmakogenetik tabanl? warfarindoz algoritmas? hen?z rutinde kullan?lmamaktad?r. ABD ve Avrupa ?al??malar?n sonu?lar?n?n 3-4 y?l i?inde sonu?lanmas? bekleniyor. Tedaviye ili?kin komplikasyonlar? azalt?p, maliyet-etkinli?i ve pratiklik sa?larsa, gelecekte warfarin ba?lanmadan ?nce kullan?labilir.
?IKAR ?ATI?MASI
Bildirilmemi?tir.
KAYNAKLAR
- Kamali F, Wynne H. Pharmacogenetics of warfarin. Annu Rev Med 2010;61:63-75.
- Yang J, Chen Y, Li X, Wei X, Chen X, Zhang L, et al. Influence of CYP2C9 and VKORC1 genotypes on the risk of hemorrhagic complications in warfarin-treated patients: a systematic review and meta-analysis. Int J Cardiol 2013;168(4):4234-43.
- Natarajan S, Ponde CK, Rajani RM, Jijina F, Gursahani R, Dhairyawan PP, et al. Effect of CYP2C9 and VKORC1 genetic variations on warfarin dose requirements in Indian patients. Pharmacol Rep 2013;65(5):1375-82.
- Daneshjou R, Tatonetti NP, Karczewski KJ, Sagreiya H, Bourgeois S, Drozda K, et al. Pathway analysis of genome-wide data improves warfarin dose prediction. BMC Genomics 2013;14(3):11.
- Budnitz DS, Pollock DA, Weidenbach KN, Mendelsohn AB, Schroeder TJ, Annest JL. National surveillance of emergency department visits for outpatient adverse drug events. JAMA 2006;296(15):1858-66.
- Li T, Lange LA, Li X, Susswein L, Bryant B, Malone R, et al. Polymorphism in the VKORC1 gene is strongly associated with warfarin dosage requirements in patients receiving anticoagulation. J Med Genet 2006;43(9):740-4.
- Moyer TP, O'Kane DJ, Baudhuin LM, Wiley CL, Fortini A, Fisher PK, et al. Warfarin sensitivity genotyping: a review of the literature and summary of patient experience. Mayo Clin Proc 2009;84(12):1079-94.
- Connolly SJ, Ezekowitz MD, Yusuf S, Eikelboom J, Oldgren J, Parekh A, et al. Dabigatran versus warfarin in patients with atrial fibrillation. N Engl J Med 2009;361:1139-51.
- Rubboli A, Becattini C, Verheugt FW. Incidence, clinical impact and risk of bleeding during oral anticoagulation therapy. World J Cardiol 2011;3:351-8.
- Franco V, Polanczyk CA, Clausell N, Rohde LE. Role of dietary vitamin K intake in chronic oral anticoagulation: prospective evidence from observational and randomized protocols. Am J Med 2004;116:651-6.
- Ozer N, Cam N, Tangurek B, Ozer S, Uyarel H, Oz D, et al. The impact of CYP2C9 and VKORC1 genetic polymorphism and patient characteristics upon warfarin dose requirements in an adult Turkish population. Heart Vessels 2010;25(2):155-62.
- Cannegieter SC, Rosendaal FR, Wintzen AR, Van Der Meer FJ, Vandenbroucke JP, Briet E. Optimal oral anticoagulant therapy in patients with mechanical heart valves. N Engl J Med 1995;333:11-7.
- Schwarz UI, Ritchie MD, Bradford Y, Li C, Dudek SM, Frye-Anderson A, et al. Genetic determinants of response to warfarin during initial anticoagulation. N Engl J Med 2008;358:999-1008.
- Yin T, Miyata T. Warfarin dose and the pharmacogenomics of CYP2C9 and VKORC1 - rationale and perspectives.Thromb Res 2007;120(1):1-10.
- Aithal G, Day C, Kesteven P, Daly A. Association of polymorphisms in the cytochrome P450 CYP2C9 with warfarin dose requirement and risk of bleeding complications. Lancet 1999;353:717-9.
- Rost S, Fregin A, Ivaskevicius V, Conzelmann E, H?rtnagel K, Pelz HJ, et al. Mutations in VKORC1 cause warfarin resistance and multiple coagulation factor deficiency type 2. Nature 2004;427:537-41.
- Yuan HY, Chen JJ, Lee MT, Wung JC, Chen YF, Charng MJ, et al. A novel functional VKORC1 promoter polymorphism is associated with inter-individual and inter-ethnic differences in warfarin sensitivity. Hum Mol Genet 2005;14(13):1745-51.
- Wang D, Chen H, Momary KM, Cavallari LH, Johnson JA, Sad?e W. Regulatory polymorphism in vitamin K epoxide reductase complex subunit 1 (VKORC1) affects gene expression and warfarin dose requirement. Blood 2008;112(4):1013-21.
- Ye C, Jin H, Zhang R, Sun Y, Wang Z, Sun W, et al. Variability of warfarin dose response associated with CYP2C9 and VKORC1 gene polymorphisms in Chinese patients. J Int Med Res 2014;42(1):67-76.
- Hillman MA, Wilke RA, Caldwell MD, Berq RL, Glurich I, Burmester JK. Relative impact of covariates in prescribing warfarinaccording to CYP2C9 genotype. Pharmacogenetics 2004;14:539-47.
- Gage BF, Eby C, Milligan PE, Banet GA, Duncan JR, McLeod HL. Use of pharmacogenetics and clinical factors to predict the maintenance dose of warfarin. Thromb Haemost 2004;91:87-94.
- Carlquist JF, Horne BD, Muhlestein JB, Lappe DL, Whiting BM, Kolek MJ, et al. Genotypes of the cytochrome P450 isoform, CYP2C9 and the vitamin K epoxide reductase complex subunit 1 conjointly determine stable warfarin dose: a prospective study. J Thromb Thrombolysis 2006;22:191-97.
- Wang TL, Li HL, Tjong WY, Chen QS, Wu GS, Zhu HT, et al. Genetic factors contribute to patient-specific warfarin dose for Han Chinese. Clin Chim Acta 2008;396:76-9.
- Nahar R, Deb R, Saxena R, Puri RD, Verma IC. Variability in CYP2C9 allele frequency: a pilot study of its predicted impact on warfarin response among healthy South and North Indians. Pharmacol Rep 2013;65:187-94.
- Limdi NA, Goldstein JA, Blaisdell JA, Beasley TM, Rivers CA, Acton RT. Influence of CYP2C9 genotype on warfarin dose among African-Americans and European-Americans. Pers Med 2007;4:157-169.
- Geisen C, Watzka M, Sittinger K, Steffens M, Daugela L, Seifried E, et al. VKORC1 haplotypes and their impact on the interindividual and interethnical variability of oral anticoagulation. Thromb Haemost 2005;94:773-79.
- Takahashi H, Wilkinson GR, Nutescu EA, Morita T, Ritchie MD, Scordo MG, et al. Different contributions of polymorphisms in VKORC1 and CYP2C9 to intra- and inter-population differences in maintenance dose of warfarin in Japanese, Caucasians and African-Americans. Pharmacogenet Genomics 2006;16:101-10.
- Tham LS, Goh BC, Nafziger A, Guo JY, Wang LZ, Soong R,? et al. A warfarin-dosing model in Asians that uses single-nucleotide polymorphisms in vitamin K epoxide reductase complex and cytochrome P450 2C9. Clin Pharmacol Ther 2006;80:346-55.
- Cheng TO. Chinese patients require lower dosage of warfarin. Int J Cardiol 2010;139:1.
- Aynacioglu AS, Brockm?ller J, Bauer S, Sachse C, Guzelbey P, Ongen Z, et al. Frequency of cytochrome P450CYP2C9 variants in Turkish population and functional relevance for phenytoin. Br J Clin Pharmacol 1999;48:409-15.
- Dericioglu N, Babaoglu MO, Saygi S, Bozkurt A, Yasar U. Warfarin resistance with poor CYP2C9 activity and CYP2C9 *1*2 genotype. Ann Pharmacother 2004;38(5):899.
- Oner Ozgon G, Langaee TY, Feng H, Buyru N, Ulutin T, Hatemi AC, et al. VKORC1 and CYP2C9 polymorphisms are associated with warfarin dose requirements in Turkish patients. Eur J Clin Pharmacol 2008; 64:889-94.
- Wu AH. Genotype and phenotype concordance for pharmacogenetic tests through proficiency survey testing. Arch Pathol Lab Med 2013;137(9):1232-6.
- Caldwell MD, Awad T, Johnson JA, Gage BF, Falkowski M, Gardina P, et al. CYP4F2 genetic variant alters required warfarin dose. Blood 2008;111(8):4106-12.
- Lai S, Sandanaraj E, Jada SR, Kong MC, Lee LH, Goh BC, et al. Influence of APOE genotypes and VKORC1 haplotypes on warfarin dose requirements. Br J Clin Pharmacol 2008;65:260-64.
- Reider MJ, Reiner AP, Rettie AE. Gamma-glutamyl carboxylase (GGCX) tag SNPs have limited utility for predicting warfarin maintenance dose. J Thromb Haemost 2007;5:2227-34.
- Kimmel SE, French B, Kasner SE, Johnson JA, Anderson JL, Gage BF, et al. A pharmacogenetic versus a clinical algorithm for warfarin dosing. Engl J Med 2013;12;369(24):2283-93.
Yaz??ma Adresi (Address for Correspondence)
Dr. G?lbahar DARILMAZ Y?CE
D??kap? Y?ld?r?m Beyaz?t E?itim ve
Ara?t?rma Hastanesi,
G???s Hastal?klar? Klini?i,
ANKARA - TURKEY
e-mail: yucegulbahar@yahoo.com.tr