RESEARC ARTICLE
Doi: 10.5578/tt.7323
Tuberk Toraks 2014;62(2):122-130

Van y?resinde izole edilen Mycobacterium tuberculosis su?lar?n?n d?rt farkl?
y?ntemle
antimikobakteriyel ajanlara duyarl?l?k tespiti
Elif Sanem BAYKAL1, H?seyin G?D?C?O?LU2, G?rkem YAMAN3, Mustafa BERKTA?4
1 Sa?l?k M?d?rl???, Halk Sa?l???, Manisa, T?rkiye
1 Health Department, Public Health, Manisa, Turkey
2 Y?z?nc? Y?l ?niversitesi T?p Fak?ltesi, T?bbi Mikrobiyoloji Anabilim Dal?, Van, T?rkiye
2 Department of Medical Microbiology, Faculty of Medicine, University of Yuzuncu Yil, Van, Turkey
3 ?stanbul Maltepe ?niversitesi T?p Fak?ltesi, T?bbi Mikrobiyoloji Anabilim Dal?, ?stanbul, T?rkiye
3 Department of Medical Microbiology, Faculty of Medicine, Istanbul Maltepe University, Istanbul, Turkey
4 Lokman Hekim Hastanesi, T?bbi Mikrobiyoloji B?l?m?, Van, T?rkiye
4 Department of Medical Microbiology, Lokman Physician Hospital, Van, Turkey
* 24. Ankem Kongresi'nde poster olarak sunulmu?tur (Poster No: 89, 29 Nisan-3 May?s, ?l?deniz/Fethiye, 2009).
?ZET
Van y?resinde izole edilen Mycobacterium tuberculosis su?lar?n?n d?rt farkl? y?ntemle antimikobakteriyel ajanlara duyarl?l?k tespiti
Giri?: Bu ?al??mada; hastanemiz mikobakteriyoloji laboratuvar?na g?nderilen hasta ?rneklerinden soyutlanan, 58 Mycobacterium tuberculosis complex su?unun ?? farkl? sistem ve agar proporsiyon y?ntemiyle maj?r antit?berk?loz ila?lar olan streptomisin, izoniazid (INH), rifampisin (RIF) ve etambutol (ETM) duyarl?l?klar?n? tespit etmek ve bu ?? sistemin uygulanabilirli?ini, h?zlar?n?, ?zg?ll?k ve duyarl?l?klar?n? kar??la?t?rmak ama?lanm??t?r.
Materyal ve Metod: Bu ama?la; mikobakteriyoloji laboratuvar?na ba?vuran hastalardan izole edilen 60 su?tan, 58 (%96.6)'i klasik y?ntemlerle M. tuberculosis complex olarak adland?r?lm??t?r. Bu su?lara Manuel MGIT AST SIRE sistemi, BacT/ALERT 3D sistemi MB/BacT SIRE kiti, TK anti-TB kiti ve Middlebrook 7H10 besiyerinde agar proporsiyon y?ntemleri kullan?lm??t?r.
Bulgular: ?al??ma sonucunda; agar proporsiyon y?ntemi ile Van ilindeki diren? profili de?erlendirildi?inde, INH diren? oran?n?n %12 oldu?u, bunu %1.7 oran?yla INH + RIF ve %1.7 oran?yla INH + SM diren?lerinin izledi?i tespit edilmi?tir. ?al??maya al?nan sistemler diren? ve duyarl?l?k saptamada t?m ila?lar i?in %100 duyarl?l??a sahip bulunmu?lard?r. INH i?in ?zg?ll?kleri TK anti-TB sisteminde %98, MGIT sisteminde %96 ve MB/BacT sisteminde ise %95 olarak tespit edilmi?tir. ?? sistem de, ?oklu ila? direncinde %100 duyarl?l?k ve ?zg?ll??e sahiptir. MB/BacT sistemi 1 su?ta tek ba??na yanl?? RIF diren?i tespit etmi?tir. Diren? tespit s?relerine bak?ld???nda ise en h?zl? sistem MGIT sistemidir.
Sonu?: Sonu?lar ?lke genelinde yap?lan ?al??malara g?re de?erlendirildi?inde ortalama bir de?erdedir. Fakat t?berk?loz tedavisinde en tehlikeli diren? kal?b? olarak bilinen INH + RIF direncinin varl??? y?remizde yetersiz tedavi programlar?n?n uyguland???na i?aret etmektedir. Sonu?ta, ?? sistem de rutin mikobakteriyoloji laboratuvarlar? i?in, duyarl?l?k tespitinde kullan?labilecek h?zl? ve g?venilir y?ntemlerdir.
Anahtar kelimeler: Mycobacterium tuberculosis, agar proporsiyon, TK, MGIT, MB/BacT
SUMMARY
Mycobacterium tuberculosis strains isolated from Van region four different sensitivity detection method antimycobacterial agents
Introduction: The purpose of this study is detecting the susceptibility rates of 58 Mycobacterium tuberculosis complex strains which were isolated from patient specimens sent to our mycobacteriology laboratory, for major anti-tuberculosis drugs like streptomycin, isoniazid, rifampicin and ethambutol with three different systems and agar proportion method and compare the accessibility, speed, specificity and sensitivity of these three systems.
Materials and Methods: With this purpose, 58 (96.6%) strains out of 60 which were isolated from the patients attended to the mycobacteriology laboratory were identified as M. tuberculosis complex with conventional methods. These strains susceptibilities to four major anti-tuberculosis drugs were detected with Manuel MGIT AST SIRE system, BacT/ALERT 3D system MB/BacT SIRE, TK anti-TB system and compared with reference method in Middlebrook 7H10 media.
Results: As a result, INH resistance in Van province with agar proportion method was detected as 12%, followed by INH + RIF resistance of 1.7% and INH + SM resistance of 1.7%. These result compared with other studies conducted country wide are in median range. The systems included in our study were determined to have 100% sensitivity for all of the drugs for detecting resistance and sensitivity rates. Specificities for INH for TK anti-TB, MGIT and MB/BacT were detected as 98%, 96% and 95% respectively. Multidrug resistance rates were detected in 100% sensitivity and specificity with all of the three systems. Only MB/BacT system gave a false negative RIF resistance for 1 strain. Fastest system according to resistance determination times is found to be the MGIT system.
Conclusion: However, presence of INH + RIF resistance pattern, indicates inadequate treatment programs in our region. As a result these three systems are fast and reliable systems for antimicrobial susceptibility testing of Mycobacterium spp. to be used in routine mycobacteriology laboratories.
Key words: Mycobacterium tuberculosis, agar proportion, TK, MGIT, MB/BacT
G?R??
D?nya Sa?l?k ?rg?t? (DS?)'n?n verilerine g?re 2011 y?l?nda t?m d?nyada 8.7 milyon yeni tan? alm?? olgu bulunmaktad?r ve 1.4 milyon insan bu nedenle hayat?n? kaybetmi?tir (1). ?lkemizde ise 15.183'? yeni olgu olmak ?zere, 2010 y?l?nda toplam 16.551 kay?tl? t?berk?loz olgusu bulunmaktad?r (2).
Hastal?k Kontrol ve ?nleme Merkezi (Centers for Disease Control and Prevention; CDC) ve DS? taraf?ndan t?berk?lozun ba?lang?? tedavisinde primer ila?lar?n kombine kullan?m? ?nerilmektedir. Bununla birlikte antit?berk?loz ila? direnci ?nemli bir sorun olu?turmaktad?r. Primer antit?berk?loz ila?lardan en az?ndan izoniazid (INH) ve rifampisin (RIF) direnci g?steren izolatlar ?ok ilaca diren?li (??D) olarak tan?mlanmakta ve 2010 y?l? i?in d?nyan?n ?o?u b?lgesinde %5'ten daha az oranda saptand??? bildirilmektedir. ?lkemizde de farkl? zaman ve b?lgelerde yap?lan yay?nlarda ??D t?berk?loz izolatlar?n?n oran? (??D-MTC) %4-6 aras?nda de?i?mektedir (3).
Yeterli t?berk?loz kontrol program? uygulanmayan, t?berk?loz oran? ve tedavi uyumsuzlu?u y?ksek oranda bulunan az geli?mi? yoksul toplumlarda y?ksek oranda ila? direnci bulundu?u bilinmektedir. Ancak bu toplumlarda eksik ya da hatal? bildirimler, d?zensiz kay?tlar ve standardize olmayan laboratuvar sonu?lar? gibi nedenlerle diren? prevalanslar? ger?e?i yans?tmamaktad?r. Asl?nda ila? direnci verilerine en ?ok gereksinim duyulan, diren? verilerinin en az oldu?u bu topluluklard?r (4). Uzun s?reli ve ?oklu antibiyotik tedavisi gerektiren t?berk?lozun tan? konduktan sonra en k?sa zamanda ve do?ru antibiyotik kombinasyonuyla tedaviye ba?lanmas?, g?n?m?zde ?oklu antibiyotik diren?li su?lar?yla b?y?k bir problem olan bu hastal???n etkili tedavisinde ?nemlidir. Bundan dolay? duyarl?l?k ve tan? testlerinin h?zl? ve do?ru bir ?ekilde sonu?land?r?lmas? gerekmektedir. Agar ve yumurta bazl? ve i?lerine antibiyotik diskleri veya belirli oranlarda antibiyotik konsantreleri eklenerek yap?lan t?berk?loz antibiyotik duyarl?l?k testleri s?relerinin uzun olmas? yeni aray??lar? da beraberinde getirmi?tir (5).
Biz de bu ?al??mada Van y?resinde tespit edilen Mycobacterium tuberculosis complex k?kenlerinin, tedavide ilk se?ilecek ila?lar olan d?rt maj?r antit?berk?loz ilaca kar?? diren? profillerini ortaya koymak ve rutin mikobakteriyoloji laboratuvarlar?nda uygulanan h?zl? ve g?venilir ticari y?ntemleri agar proporsiyon y?ntemiyle kar??la?t?rmay? ama?lad?k.
MATERYAL ve METOD
Laboratuvar?m?za t?berk?loz ?n tan?l? hastalardan, k?lt?r istemiyle g?nderilmi? klinik ?rneklerden (balgam, mide a?l?k suyu, idrar, beyin omurilik s?v?s?, trakeal aspirat vb.) soyutlanan 60 su? ?al??maya al?nd?. Bu su?lardan Niasin testi pozitif, nitrat red?ksiyonu pozitif, ?s?ya stabil katalaz test negatif, pigment ?retimi negatif, 37?C'de ?reme h?z? yava? olan ve TK PNB (Salubris A?.; T?rkiye) besiyerinde ?reyen 58 izolat M. tuberculosis complex olarak tan?mland? ve ?al??maya al?nd?. ?al??mada kontrol k?keni olarak M. tuberculosis ATCC H37Rv su?u kullan?ld?.
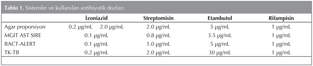
?al??maya al?nan 58 su? ve kontrol su?unun streptomisin (SM), INH, RIF, etambutol (EMB)'e kar?? duyarl?l?klar? Manuel MGIT AST SIRE sistemi (Becton Dickonson and Company-USA), BacT/ALERT 3D sistemi MB/BacT ve SIRE kiti (bioM?rieux SA-Fransa), TK anti-TB & PNB KIT (Salubris A.?; T?rkiye) ve alt?n standart olarak kabul edilen agar proporsiyon (orant?) y?ntemleri kullan?larak test edildi. Sistemlerde kullan?lan antibiyotiklerin dozlar? Tablo 1'de verilmi?tir.
BacT/ALERT? 3D Sistemi
Bu ?al??mada; antibiyotik bulunan ?i?e pozitif bulunmaz veya direkt kontrolden daha b?y?k ve proporsiyonel kontrolden daha b?y?k saptama zaman?na sahipse, mikobakteri duyarl? olarak raporland?. Antibiyotik bulunan ?i?e, direkt kontrole e?it veya daha b?y?k ancak proporsiyonel kontrole e?it veya daha az pozitif saptama zaman?na sahipse mikobakteri o antimikobakteriyele diren?li olarak raporland?. On be? g?n i?inde direkt kontrol ve/veya proporsiyonel kontrol ?i?esi pozitif sonu? vermezse test iptal edilerek tekrarland?.
BBL MGIT AST SIRE Sistemi
Bu ?al??mada; ekimi takiben ???nc? g?nden itibaren t?pler g?nl?k olarak 365 nm uzun dalga boyunda uv transl?minat?rl? MGIT okuyucuda okutuldu. Kontrol MGIT t?p? pozitif oldu?unda, ila?l? MGIT t?plerinin sonu?lar? de?erlendirildi. Kontrol MGIT t?p? negatif ise tekrar ink?be edilmeye devam edildi. Kontrol MGIT t?p? 12 g?n boyunca takip edildi. E?er 12. g?n sonunda hala negatifse test tekrar edildi. ?la?l? MGIT t?p?, kontrol t?p?n?n floresan vermesinden itibaren iki g?n ge?ti?i halde hala floresan vermiyorsa negatif (duyarl?) olarak raporland?. Bunun tersine ila? i?eren MGIT t?p?, kontrol t?p?n?n floresan vermesi esnas?nda veya floresandan itibaren iki g?n i?inde floresan veriyorsa pozitif (diren?li) olarak rapor edildi.
TK ANT?-TB & PNB K?T
Bu ?al??mada; Test, TK Medium? t?p? sar?ya d?nd??? zaman de?erlendirmeye al?nd?. Bir su?a ait TK Medium t?p? sar?ya d?nd??? zaman, i?erilerinde antimikobakteriyel ila? bulunan t?plerden rengi sar?ya d?nen yani ?remenin pozitif oldu?u t?p hangi antimikobakteriyale aitse o su?, o antimikobakteriyale diren?li olarak, rengi k?rm?z? kalm?? t?plerdeki antimikobakteriyallere ise duyarl? olarak raporland?.
Agar Proporsiyon (Orant?) Y?ntemi
Besiyerlerinin Haz?rlanmas?
Besiyerleri her biri 200 mL'lik olacak ?ekilde 8 balon joje i?inde haz?rland?. Her bir 200 mL'lik 7H10 agar besiyerinin haz?rlanmas? icin; bir cam balon joje i?ine, 180 mL distile su, 3.8 g 7H10 agar besiyeri ve 1 mL gliserol eklenerek ?s? kayna?? ?zerinde eritildi (?retici firman?n ?nerdi?i ?ekilde). Otoklavda 121?C'de 15 dakika s?reyle sterilize edildi.
Daha sonra 50-55?C'lik su banyosunda so?umaya b?rak?ld?. Besiyerlerinin s?cakl??? 50-55?C'ye indi?inde i?lerine zenginle?tirici olarak 20 mL OADC (oleik asit, albumin, dekstroz ve katalaz) kar???m? eklendi.
?la? Dil?syonlar?n?n Haz?rlanmas?
Antibiyotiklerin steril distile su ile veya uygun ??z?c?ler ile (streptomisin, izoniazid ve etambutol i?in distile su, rifampisin icin metanol) 10.000 μg/mL'lik (en az 1000 μg/mL olmal?) stok sol?syonlar? haz?rland?. Stok sol?syonlar haz?rlan?rken gerekli miktar antibiyotikler ?zerinde belirtilen potens (% veya μg/mg) dikkate al?narak ?u form?le g?re hesapland?:
A??rl?k (mg) = Hacim (mL) x istenilen konsantrasyon (μg/mL) / Potens (μg/mg)
Streptomisin Sol?syonunun Haz?rlanmas?
Potensi= 800 mg/g
125 mg streptomisin s?lfat 10 mL distile su i?inde eritildi. B?ylece 10.000 μg/mL olan sol?syon elde edildi. Sol?syon 0.22 μm por ?apl? membran filtrelerinden ge?irilerek sterilize edildi. Steril edilen 10.000 μg/mL'lik stok sol?syondan, 1 mL al?narak 9 mL steril distile su ?zerine eklendi. B?ylece 1000 μg/mL'lik bir sol?syon elde edilmi? oldu. Bu sol?syondan 0.4 mL al?narak 55?C'ye so?utulmu? ?zeri antibiyotik ismiyle etiketlenmi? 200 mL besiyerine eklendi. B?ylece son konsantrasyonu 2 μg/mL olan streptomisinli besiyeri elde edilmi? oldu.
1000 μg/mL'lik stok sol?syondan 2 mL al?narak, 55?C'ye so?utulmu? ?zeri antibiyotik ismiyle etiketlenmi? 200 mL besiyerine eklendi ve son konstrasyonu 10 μg/mL olan streptomisinli besiyeri elde edilmi? oldu.
?zoniazid (INH) Sol?syonunun Haz?rlanmas?
Potensi= 1000 mg/g
100 mg (100.000 μg) izoniazid 10 mL distile su i?inde ??zd?r?ld?. B?ylece 10.000 μg/mL INH sol?syonu elde edildi. Sol?syon 0.22 μm'lik membran filtresinden ge?irilerek sterilize edildi. Steril 10.000 μg/mL'lik stok sol?syondan 1 mL al?narak 9 mL distile su ile kar??t?r?ld? ve 1000 μg/mL'lik bir sol?syondan da 1 mL al?n?p 9 mL distile su ile kar??t?r?ld???nda, 100 μg/mL'lik stok sol?syon elde edildi. 100 μg/mL'lik stok sol?syondan 0.4 mL al?narak 55?C'ye so?utulmu? 200 mL Middlebrook 7H10 agar besiyerine eklenerek, mililitresinde 0.2 μg INH olacak ?ekilde besiyeri elde edilmi? oldu.
100 μg/mL'lik stok sol?syondan 2 mL al?narak, 55?C'ye so?utulmu? 200 mL Middlebrook 7H10 agar besiyerine eklenerek, mililitresinde 1 μg INH olan besiyeri elde edilmi? oldu.
Rifampisin Sol?syonunun haz?rlanmas?
Potensi= 1000 mg/g
100 mg rifampisin 10 mL metanol i?inde eritildi. B?ylece 10.000 μg/ml rifampisin sol?syonu elde edildi. Sol?syon 0.22 μm'lik membran filtresinden ge?irilerek sterilize edildi. Steril 10.000 μg/mL'lik stok sol?syondan 1 mL al?narak, 9 mL distile su ile kar??t?r?ld? ve b?ylece mililitresinde 1000 μg rifampisin bulunan bir sol?syon olu?turuldu.
Bu sol?syondan 0.2 mL al?narak, 55?C'ye so?utulmu? 200 mL Middlebrook 7H10 agar besiyerine eklenerek, mililitresinde 1 μg rifampisin bulunan bir besiyeri elde edilmi? oldu.
Etambutol Sol?syonunun Haz?rlanmas?
Potensi= 1000 mg/g
100 mg (100.000 μg) etambutol, 10 mL steril distile su i?inde ??zd?r?ld?. B?ylece 10.000 μg/mL etambutol sol?syonu elde edildi. Sol?syon 0.22 μm'lik membran filtresinden ge?irilerek sterilize edildi. 10.000 μg/mL'lik sol?syonundan 1 mL al?narak 9 mL distile su ile kar??t?r?larak mililitresinde 1000 μg etambutol olan sol?syon elde edildi.
Bu sol?syondan 1.2 mL al?narak so?utulmu? 200 mL besiyerine eklendi. B?ylece 6 μg/mL'lik etambutollu besiyeri elde edildi.
Bu ?ekilde haz?rlanan ila? stok sol?syonlar? a?z? kapal? ependorf t?plerinde 2 mL'lik hacimlere b?l?nerek -80?C'de alt? ay boyunca saklanabilmektedir. ?al??madan ?nce oda ?s?s?nda ??zd?r?lmeleri gerekir.
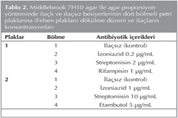
Haz?rlanan ila?l? ve ila?s?z besiyerleri, daha ?nceden haz?rlanm?? ve etiketlenmi? d?rt b?lmeli steril plastik petri plaklar?na (Felsen plaklar?) her b?lmeye 5 mL olacak ?ekilde Tablo 2'de belirtilen d?zende d?k?ld?. D?k?len besiyerleri direkt ???ktan korunarak, kapaklar? yar? ac?k ?ekilde biyog?venlik s?n?f 2 kabin i?inde kurumaya b?rak?ld?. Daha sonra deliksiz plastik torbalara konularak +4?C'de sakland?.
Mikobakteri S?spansiyonlar?n?n Haz?rlanmas?
?al??maya al?nan L?wenstein-Jensen besiyerinde ?retilmi? M. tuberculosis complex olarak isimlendirilmi? k?kenler steril tek kullan?ml?k plastik ?zeler yard?m?yla bol miktarda (besiyerinden almamaya dikkat edilerek) topland?. ??inde 8-10 adet cam boncuk ve 5-6 mL Middlebrook 7H9 broth bulunan hasta isimleri ile etiketlenmi? steril cam t?plerdeki s?v? besiyerine emulsifiye edildi. 1-2 dakika s?reyle t?pler vortekslendi. B?y?k partik?llerin ??kmesi ve olu?an aerosollerin azalmas? i?in 20 dakika s?reyle t?p bekletildi. S?pernatant, steril past?r pipeti yard?m?yla etiketlenmi? bo? bir steril cam t?pe al?nd?. Gerekti?inde s?v? besiyeri ekleyerek s?spansiyonun bulan?kl??? McFarland No: 1'e ayarland? (yakla??k 107 CFU/mL).
Daha sonra steril distile suyla etiketlenmi? bo? steril cam t?plerde bu s?spansiyonun 10-2 (1/100) ve 10-4 (1/10.000) dil?syonlar? haz?rland?.
?nok?lasyon ve ?nk?basyon
?al??maya al?nan her bir M. tuberculosis complex i?in; iki set test besiyeri (1 ve 2 nolu plaklar?n her birinden iki?er tane) oda ?s?s?na getirildi. Plak y?zeylerinin kuru olmas?na dikkat edildi. Petri plaklar? hasta k?lt?r numaras? ve dil?syon oranlar?n? g?sterecek ?ekilde (setlerden biri 10-2, di?eri 10-4) i?aretlendi. ?nce 1 nolu setin her bir b?lmesine ?nceden haz?rlanm?? olan 10-2 basil dil?syonundan steril ?l?ekli past?r pipeti kullan?larak, 0.1'er mL inok?le edildi. Sonra 2 nolu set icin ayn? i?lem 10-4 dil?syon ile tekrarland?. ?nok?lumun saf olup olmad???n? kontrol etmek amac?yla dil?e edilmemi? s?spansiyondan 1-2 damla, bir adet kanl? agar besiyerine ekildi. ?nok?lumun besiyerlerine absorbe olmas? i?in, inok?le edilen plaklar agarl? taraf? a?a??da olacak ?ekilde oda ?s?s?nda kabin i?inde yakla??k 1 saat s?reyle bekletildi. Daha sonra her bir petri pla?? CO2 ge?irgen torbalara konularak 36?C'de ink?basyona b?rak?ld?.
Bu ?al??mada; ink?basyonun ilk yedi g?n?nde kontaminant bakteri varl??? a??s?ndan kanl? agarlar incelendi. Kontaminasyon saptan?lan testler iptal edilerek, tekrarland?. Test besiyerlerinde ise antibiyotiksiz kontrol b?lmeleri ?? hafta boyunca her hafta incelendi. ???nc? hafta sonunda ?reme yetersizse, test tekrar edildi. ?? haftadan ?nce kontrol kadran?nda say?labilir d?zeyde 50'den fazla koloni (+1 veya daha fazla) saptanmas? halinde plaklar de?erlendirilmeye al?nd?. ?nk?basyon sonunda t?m kadranlardaki koloniler say?larak Tablo 2'ye g?re kantite edildi. "Diren? oran? (%)= ila?l? b?lmedeki koloni say?s? x 100 / kontrol b?lmesindeki koloni say?s?" form?l? uygulanarak diren? oran? %1 olan sonu?lar diren?li; < %1 tespit edilenler ise duyarl? olarak raporland?. Kar??la?t?rma yap?l?rken ayn? dil?syonlardaki ?remeler kullan?ld? ve de?erlendirmede, kontrol b?lmelerindeki koloni say?s? 4+ olan dil?syonlar de?erlendirmeye al?nd?. Bu durumda t?m antit?berk?loz ila?lara duyarl?l?k tespit edildiyse sonu? raporland?. Fakat tek bir antit?berk?loz ilaca diren? g?r?lmesi durumunda test yo?un inok?lum ??phesiyle iptal edilerek tekrarland?.
Kalite Kontrol
?al??mada kullan?lan t?m sistemler t?m ila?lara duyarl? oldu?u bilinen M. tuberculosis H37Rv (ATCC 27294) kalite kontrol su?u ile kontrol edildi.
?statistiksel Yorum
Sistemlerin diren? ve duyarl?l?k tespitlerindeki ?zg?ll?k, duyarl?l?k ve genel uyumlar? agar proporsiyon y?ntemiyle kar??la?t?r?larak kappa istati?i ile de?erlendirilmi?tir. Kappa de?erlerine g?re uyum:
0.81-1.00 de?er aral???nda m?kemmel
0.61-0.80 de?er aral???nda g??l?
0.41-0.60 de?er aral???nda belirgin
0.10-0.40 de?er aral???nda zay?f
< 0.10 de?er aral???nda ise uyum yok olarak yorumlanm??t?r (6).
?la?lar?n duyarl?l?k zaman? (g?n) olarak sistemler aras?nda fark olup olmad??? ise tek y?nl? varyant analizi (One-ONAVA) kullan?larak de?erlendirilmi?tir.
BULGULAR
T?berk?loz ?n tan?l?, farkl? hastalardan k?lt?r istemiyle mikobakteriyoloji laboratuvar?m?za g?nderilmi? ve LJ besiyerlerinde ?retilmi? 60 su?tan 58 tanesi (%96.6) M. tuberculosis complex olarak tan?mland? ve ?al??maya al?nd?. Elli sekiz su?un 47 (%81)'si balgam, 11 (%19)'i ise akci?er d??? t?berk?loz ?rneklerinden (3 lenf drenaj?, 2 beyin omurilik s?v?s?, 2 plevral mayi, 2 idrar, 2 mide a?l?k s?v?s?) izole edildi. Hastalar?n 48'i yeni olgu olup 10'u daha ?nce tedavi alm?? hastalard?.
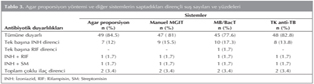
?al??maya al?nan 58 su?un 49 (%84.5)'u agar proporsiyon y?ntemiyle t?m antit?berk?loz ila?lara duyarl? olarak bulunurken, di?er sistemlerde bu say? s?ras?yla Manuel MGIT'da 47 (%81), MB/BacT'da 45 (%77.6), TK anti-TB'de 48 (%82.8) olarak tespit edildi. Agar proporsiyon y?ntemiyle INH'nin 0.2 g/mL'lik konsantrasyonuna 7 (%12) su?ta diren? saptanm?? ve bu 7 su? INH'ye d???k d?zey diren?li olarak kabul edilmi?tir. Y?ksek d?zey INH direnci ise tespit edilmemi?tir. Di?er sistemlerde de ayn? 7 su? INH diren?li bulunmu?tur. Manuel MGIT AST SIRE sistemi, bu 7 su?un d???nda 2 (%15.5) su?ta, MB/BacT 3 (%17.3) su?ta, TK anti-TB ise 1 (%13.8) su?ta daha? tek ba??na INH direnci saptam??t?r. Agar proporsiyon y?ntemiyle streptomisine ve izoniazide diren?li 1 (%1.7) su? saptanm?? ve bu su? t?m sistemler taraf?ndan tespit edilmi?tir. Manuel MGIT, MB/BacT, TK anti-TB ve agar proporsiyon y?ntemiyle RIF'a, 1 (%1.7) su?ta diren? saptan?rken bu su? ayn? zamanda INH direnci de ta??maktad?r. Bu diren? d???nda MB/BacT sistemi tek ba??na 1 su?ta RIF direnci tespit etmi?tir (Tablo 3).
Daha ?nce tedavi alm?? 10 hastadan birinde INH direnci tespit edilirken, di?er 9 hastan?n izolat? t?m antit?berk?loz ila?lara duyarl? bulunmu?tur.
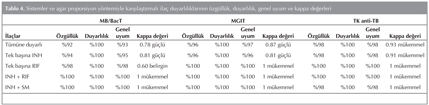
Sistemlerin diren? ve duyarl?l?k tespit etmedeki ?zg?ll?k, duyarl?l?k ve genel uyumlar? agar proporsiyon y?ntemiyle kar??la?t?r?larak hesaplanm??t?r. Tablo 4'te sistemlerin agar proporsiyon y?ntemine g?re diren? tespit etmede ?zg?ll?k, duyarl?l?k genel uyumlar? ve kappa de?erleri g?r?lmektedir.
Bu do?rultuda; MGIT AST SIRE sistemiyle 58 su?un 47'sinde t?m maj?r antit?berk?loz ila?lara duyarl?l?k tespit edilmi?tir. Agar proporsiyon y?ntemiyle kar??la?t?r?ld?klar?nda ?zg?ll?k, duyarl?l?k ve genel uyumu s?ras?yla %96, %100 ve %97 olarak hesaplanm??t?r. Kappa de?eri 0.87 olarak bulunmu? ve duyarl?l?k saptamada sistem m?kemmel uyumlu olarak yorumlanm??t?r. MGIT AST SIRE sistemi agar proporsiyonla tespit edilen tek ba??na INH diren?li 7 su?u do?ru olarak tespit etmi? fakat 2 INH duyarl? su?u diren?li olarak raporlam??t?r. Buna g?re ?zg?ll?k, duyarl?l?k ve genel uyumu s?rayla %96, %100, %96 bulunmu?tur. Kappa de?eri 0.81'dir. Tek ba??na SM, RIF ve EMB'ye diren? tespit edilmemi? ve sistem duyarl?l?k tespiti a??s?ndan agar proporsiyonla tam olarak (%100) uyumlu bulunmu?tur. ?oklu diren? i?in de durum ayn?d?r. Bir su?ta INH + RIF ve bir su?ta da INH + streptomisin (SM) direnci tespit edilmi? ve agar proporsiyonla tam uyum g?stermi?tir (%100).
BacT/ALERT 3D sistemi MB/BacT SIRE kiti ile 58 su?un 45'inde t?m maj?r antit?berk?loz ila?lara duyarl?l?k tespit edilmi? ve ?zg?ll?k, duyarl?l?k ve genel uyumlar? referans y?ntem olan agar proporsiyonla kar??la?t?r?larak s?ras?yla %92, %100 ve %93 olarak bulunmu?tur. Hesaplanan kappa de?eri 0.78 dir ve g??l? bir uyumdan bahsedilir.
Buna g?re agar proporsiyon y?ntemiyle INH'ye diren? saptanan 7 su? sistem taraf?ndan tespit edilmi? fakat INH duyarl? 3 su? sistem taraf?ndan yanl?? diren?li olarak raporlanm??t?r. INH duyarl?l?k tespitinde sistemin ?zg?ll?k, duyarl?l?k, genel uyum ve kappa de?erleri s?ras?yla %94, %100, %95, 0.84 olarak hesaplanm??t?r. Agar proporsiyon y?ntemiyle tek ba??na RIF direnci saptanmam??ken BacT/ALERT 3D sistemi, MB/BacT SIRE kitiyle 1 su?ta yanl?? diren? tespit edilmi?tir. RIF i?in s?ras?yla ?zg?ll?k %98, duyarl?l?k %100, genel uyum %98 hesaplanm?? kappa de?eri 0.91 olarak bulunmu?tur. EMB, SM ve ?oklu ila? direnci i?in t?m de?erler %100'd?r.
TK anti-TB sistemiyle duyarl?l?k saptamada ?zg?ll?k, duyarl?l?k ve genel uyum s?ras?yla %98, %100, %98 ve kapa de?eri 0.93 hesaplanm?? ve m?kemmel uyuma sahip bulunmu?tur.
Ayr?ca IHN i?in %98 ?zg?ll?k, %100 duyarl?l?k ve %98 genel uyuma sahip olup kappa de?eri 0.91'dir. Di?er ila?lar i?in de?erler %100'd?r.
?la?lar?n duyarl?l???n? tespit etme zaman? (g?n) olarak sistemler aras?nda fark olup olmad???n? belirlemek amac?yla; tek y?nl? varyans analizi (One-ANOVA) yap?lm??t?r. Yap?lan varyans analizi sonucunda; ila?lar?n duyarl?l???n? tespit etme zaman? bak?m?ndan her ?? sistem aras?ndaki fark istatistik olarak anlaml? bulunmu?tur (p< 0.01) (Tablo 5).
Buna g?re MGIT sistemiyle ortalama 5 g?nde (min 3; maks 7), TK anti-TB sistemiyle ortalama 11.7 g?nde (min 7; maks 20), MB/BacT sistemiyle ortalama 13.6 g?nde (min 8; maks 22) duyarl?l?klar tespit edilmi?tir.
TARTI?MA
G?n?m?zde t?berk?loz tedavisinde kullan?lan primer antit?berk?loz ila?lar, INH, RIF, SM, ETM ve pirazinamiddir. T?berk?lozda etkenin k?sa s?rede tan?nmas?, ila? direncinin saptanmas? ve ila?lar?n uygun dozlarda uygulanmas? son derece ?nemlidir. Bu nedenle klasik laboratuvar tan? y?ntemleri yan?nda h?zl? sonu? veren, duyarl?l??? ve ?zg?ll??? y?ksek, kolay uygulanabilir yeni k?lt?r y?ntemleri ile molek?ler biyoloji teknikleri geli?tirilmektedir. Antit?berk?loz ila?lara kar?? diren? geli?imini saptamak i?in M. tuberculosis k?kenlerinin antit?berk?loz ila?lara duyarl?l?klar?n?n belirlenmesinde, DS? taraf?ndan s?v? (7H12 besiyeri kullan?lan ticari sistemler) ve kat? [proporsiyon y?ntemi (Middlebrook 7H10/7H11 agar veya L?wenstein-Jensen: LJ)] bazl? y?ntemler ?nerilmektedir (7).
?al??maya toplam 58 M. tuberculosis complex su?u al?nm?? olup, bu su?lardan 48'i yeni olgulardan, 10'u? ise daha ?nce tedavi alm?? olgulardan izole edilmi?tir ve bu 10'u sadece birinde INH direncine rastlanm??t?r. Bu say?lar?n b?lgemizdeki primer ve sekonder diren? oranlar?n? do?ru yans?tmayaca?? d???n?lerek primer ve sekonder diren? ?eklinde bir de?erlendirmeye gidilmemi?tir.
Aslan ve arkada?lar?, Baylan ve arkada?lar?, Durmaz ve arkada?lar?, Yayl? ve arkada?lar?, Karada? ve arkada?lar?, Orhan ve arkada?lar? ile Tansel ve arkada?lar?n?n yapt?klar? ?al??malarda INH diren?leri s?ras?yla %14.3, %7.9, %10.22, %9.3, %8, %13.93, %9 ?eklinde olup, bizim ?al??mam?zda oldu?u gibi tekli INH diren?leri di?er diren?lere g?re y?ksektir (8,9,10,11,12,13,14). Bu ?al??mada ikili ila? direncinde INH ile birlikte RIF'e ve SM'ye diren? tespit edilmi?tir. Bu durumda RIF ve SM'ye %1.7'lik bir diren? s?z konusudur. ?ki ilaca diren? oran? ise %3.4't?r. EMB direnci ise yoktur. Durmaz ve arkada?lar?n?n, Yayl? ve arkada?lar?n?n, ?enol ve arkada?lar?n?n yapt?klar? ?al??malarda ?oklu ila? direnci s?ras?yla %2.26, %2.7, %2 bulunmu?tur (10,11,15). ?al???lan su? say?s?, ger?ek diren? durumunu g?stermek i?in yetersiz olsa da saptanan ila? diren? oranlar?, tedaviye do?ru y?n vermek ad?na, ila? duyarl?l?k testi ?al??malar?n?n yap?lmas? gerekti?ini g?stermesi bak?m?ndan ?nemlidir. ?al??mada saptanan %12 oran?nda bir INH direnci g?z ard? edilmemelidir. Y?resel, primer INH direncinin %4'?n ?st?nde olmas? durumunda en az d?rt antit?berk?loz ila?la tedaviye ba?lanmas? ilkesi nedeniyle, bu de?er b?lgemizdeki tedavi se?ene?ini y?nlendirmesi a??s?ndan da ayr? bir ?neme sahiptir (16).
Yurt d???nda ise 1997 y?l?nda MGIT sistemiyle INH ve RIF duyarl?l??? ?zerine ?al???lm?? ve BACTEC 460 sistemi ile kar??la?t?r?lmas? yap?lm??t?r. ?al??ma sonucunda genel uyum INH i?in %97.3, RIF i?in %100 bulunmu?tur (17). Bu ?al??mada MGIT sisteminin genel uyumu INH i?in %96 bulunmu?tur.
1999 y?l?nda Avrupa'da yap?lan ?ok merkezli bir ?al??mada ise MGIT sistemi yine BACTEC 460 TB sistemiyle kar??la?t?r?lm??, uyumsuz sonu?lar proporsiyon y?ntemiyle tekrar analiz edilmi?tir (18). ?al??ma sonucunda INH, RIF ve SM i?in genel uyum %99 bulunmu?tur. 3.75 ?g/mL'lik konsantrasyonda ?al???ld???nda EMB i?in do?ruluk seviyesi %98 olarak tespit edilmi?tir.
2000-2001 y?l?nda Avrupa ve Amerika'da yap?lan ?al??malarda MGIT AST SIRE sistemi agar proporsiyon metoduyla kar??la?t?r?lm?? ve d?rt maj?r anti-t?berk?loza duyarl?l?k tespitinde genel uyumda %95.3 ile %100 aras?nda de?erler tespit edilmi?tir (19,20,21). Bu ?al??mada ise manuel MGIT sisteminin d?rt maj?r antit?berk?loza duyarl?l?k tespitinde genel uyumu %97, INH'de ?zg?ll?k ve duyarl?l?k s?ras?yla %94 ve %100 olarak tespit edilmi?tir. ?al??mada, EMB'ye kar?? diren?li su? bulunmad???ndan MGIT sisteminin EMB direncini saptamadaki ba?ar?s? de?erlendirilememi?tir.
Manuel MGIT sistemiyle yap?lan ?al??ma say?s? s?n?rl?d?r. Tam otomatize bir sistem olan MGIT 960 sistemi bu sistemin yerini alm?? g?r?nmektedir. Manuel MGIT sistemi, ?zellikle MDR-TB su?lar?n?n h?zl? tespitinde referans sistem BACTEC 460 sistemi kadar g?venilir oldu?u yap?lan ?al??malarla g?sterilmi?tir (17,19,21). Bu ?al??mada da di?er bir referans y?ntem olan agar proporsiyonla duyarl?l?k genel uyumu ve ?zellikle INH direncinde g??l? bir uyum s?z konusudur.
Wing Wai Yew, Steena Ching Wa Tong'un 2001 y?l?nda yapt?klar? MB/BacT sistemiyle agar proporsiyon y?nteminin kar??la?t?r?lmal? ?al??mas?nda, iki metod aras?nda genel uyum SM (1 ?g/mL) i?in %99, INH (1 ?g/mL) i?in %95.2, RIF (1 ?g/mL) i?inse %100 olarak bulunmu?tur (22). 2006 y?l?nda BacT/ALERT 3D sistemiyle DS? ait 80 su? kullan?larak yap?lan bir ?al??mada, INH (0.09 mg/L) i?in duyarl?l?k %100, ?zg?ll?k %95, EMB (1.8 mg/L) i?inse s?ras?yla %100 ve %98 bulunmu?tur (21). Yap?lan bu iki ?al??mada ve bu ?al??mada INH i?in duyarl?l?k %100 bulunmu?tur. ?al??mada antibiyotiklere diren? say?s? az oldu?u i?in kar??la?t?rma yapmak do?ru bulunmam??t?r.
Duyarl?l?k tespit zamanlar?na bak?ld???nda MGIT sistemi en h?zl? sistem olarak g?r?lmektedir. MB/BacT sisteminde ortalama s?re 13.6 g?n olarak tespit edilmi?tir. Bu s?re uzun gibi g?r?nse de; ?al??mada, indirekt inok?lum (LJ besiyerinde ?retilmi? su?lardan 1.0 McFarland haz?rlanarak) kullan?ld???ndan, MB/BacT ?al??ma prosed?r gere?i olarak haz?rlanan 1.0 McFarland'l?k inok?lum, cihaza y?klenmi? ve ?reme tespitinden sonra su?lar duyarl?l?k testine tabii tutulmu?lard?r. Cihaz?n ortalama ?retim zaman? 8.55 g?n (min 3-maks 20 g?n) olarak bulunmu?tur. MB/BacT sisteminin ortalama tespit zaman?n?n y?ksek ??kmas? buna ba?lanabilir. T?m sistemler indirekt inok?lum ile ?al???ld???ndan bu s?re MB/BacT sisteminde duyarl?l?k tespit zaman?n?n i?inde de?erlendirilmi?tir.
Sonu? olarak ?al??mada; standart ve referans y?ntem olan agar proporsiyon y?ntemiyle, tekli ila? direnci olarak sadece INH'ye kar?? diren? tespit edilmi? olup, t?m sistemler %100 duyarl?l?kla (ger?ek diren?lileri tespit etme yetene?i) INH direncini tespit etmi?lerdir. Agar proporsiyon y?ntemiyle bir su?ta INH + RIF (MDR) ve bir su?ta da INH + SM direnci tespit edilmi?, t?m sistemler taraf?ndan bu su?lar %100 duyarl?l?k ve %100 ?zg?ll?kle bulunmu?lard?r. Her ?? sistemin de, yap?lan di?er ?al??malarda belirtildi?i gibi, maj?r antit?berk?loz ila?lar olan INH, SM, EMB ve RIF i?in duyarl?l?k tespitinde, rutin mikobakteriyoloji laboratuvarlar?nda kullan?labilecek; i? g?c? az, h?zl? ve g?venilir y?ntemler oldu?u g?r?lmektedir.
?lkemizde toplumun t?m?n? yans?tan, g?venilir, standardize edilmi? diren? raporlar? bulunmamakla birlikte, de?i?ik merkezlerden bildirilen raporlar diren? sorununun k???msenmeyecek boyutta oldu?unu g?stermektedir.
Bu ?al??malar?n ?????nda, etkili t?berk?loz tedavisinin sa?lanabilmesi i?in ?lke genelinde, ?lke ger?ekleriyle ba?lant?l? olarak h?zl?, g?venilir, standardize edilmi? hem izolasyon-identifikasyon, hem de duyarl?l?k testlerinin yap?labildi?i sistemlerin mikobakteriyoloji laboratuvarlar?nda kullan?ma girmesi gerekti?i anla??lmaktad?r.
?IKAR ?ATI?MASI
Bildirilmemi?tir.
KAYNAKLAR
- Global tuberkulosis Report 2012, Eri?im tarihi: 10 Eyl?l 2013. Available from: http://apps.who.int/iris/bitstream/10665/75938/1/9789241564502_eng.pdf
- ?z Y, Aslan M, Ak?it F, Durmaz G, Kiraz N. Mycobacterium tuberculosis kompleks izolatlar?n?n primer antit?berk?loz ila?lara duyarl?l???n?n de?erlendirilmesi. ANKEM 2012;26(Suppl 1):20-4.
- World Health Organization, Global tuberculosis control: WHO Report, WHO, Geneva 2011.
- Aslan G, Delialio?lu N, Emekda? G. Mycobacterium tuberculosis su?lar?n?n izoniazid, rifampisin, streptomisin ve etambutol duyarl?l?klar?n?n BACTEC y?ntemi ile belirlenmesi. ANKEM 2005;19(1):43-7.
- ?zt?rkeri H , Emekda? G, Kocabeyo?lu ?, G?z?a??k A. T?berk?loz basillerinin major antit?berk?loz ila?lara duyarl?l???n?n saptanmas?nda E-test ile BACTEC y?nteminin kar??la?t?r?lmas?. ANKEM 2000;14(1):1-4.
- Keskin S. ?ki y?nl? (contigency) tablolarda kappa istati?inin kullan?m?, Biyoteknoloji (K?kem) Derg 2001;25(1):53-7.
- Dibek AM. Mycobacterium tuberculosis complex k?kenlerinin MB/BacT sistemi ile ila? duyarl?l?klar?n? saptanmas? ve sistemin standardize edilmesi (Uzmanl?k tezi). ?zmir: Ege ?niversitesi T?p fak?ltesi Mikrobiyoloji ve Klinik Mikrobiyoloji Anabilim Dal?; 1999.
- Aslan G, Delialio?lu N, Y?ld?z ?, Direkel ?, Emekda? G. Mycobacterium t?berculosis su?lar?n?n primer antit?berk?loz ila?lara kar?? duyarl?l???n?n belirlenmesinde BACTEC 460 ve agar proporsiyon y?ntemlerinin kar??la?t?r?lmas?. ?nfeksiyon Derg 2007;21(2):75-80.
- Baylan O, K?sa ?, Albay A, Do?anc? L. Mikobakteriyoloji laboratuvar?m?zda 2002 y?l?nda t?berk?loz olgular?ndan izole edilen M.tuberculosis kompleks (MTC) su?lar? ve antit?berk?loz ila? duyarl?l?k sonu?lar?. G?lhane T?p Derg 2003;45(3):256-62.
- Durmaz R, ?zerol IH, Durmaz B, G?nal S, ?eno?lu A, Evliyao?lu E. Primary drug resistance and molecular epidemiology of Mycobacterium tuberculosis isolates from patients in a population with high tuberculosis incidence in Turkey. Microb Drug Resist 2003;9(4):361-6.
- Yayl? G, S?zen H, A?alar C. Isparta y?resinde izole edilen Mycobacterium tuberculosis su?lar?n?n antit?berk?loz ila?lara duyarl?l?klar?. T?rk Mikrobiyol Cem Derg 2003;33(1):24-30.
- Karada? A, Toka? M, G?venli A, S?nb?l M, G?nayd?n M, Sani? A. Klinik ?rneklerden izole edilen t?berk?loz basili kompleksinin maj?r antit?berk?loz ila?lara diren? oranlar?. ANKEM 2004;18(4):189-92.
- Orhan G, Zer Y, Balc? ?, Bayram A, Korkmaz G. Mikobakteriyoloji laboratuvar?nda incelenen ?rneklerin retrospektif olarak de?erlendirilmesi. T?rk Mikrobiyol Cem Derg 2002;32(3-4):225-9.
- Tansel ?, Y?ksel P, Kulo?lu F, Akata F. Mycobacterium tuberculosis su?lar?n?n antit?berk?loz ila?lara direnci: Trakya ?niversitesi hastanesinin iki y?ll?k sonu?lar?. ?nfeksiyon Derg 2003;17(1):23-6.
- ?enol G, Co?kun M, Bi?men C, Erer OF. Aktif akci?er t?berk?lozlu hastalardan izole edilen Mycobacterium tuberculosis k?kenlerinin ila? diren? oranlar?n?n de?erlendirilmesi. Klimik Derg 2006;19(2):71-4.
- Oktun M, Akata F, Karabay O, Tabako?lu E, Tu?rul M, D?ndar V. Trakya ?niversitesi Hastanesi'ne 1996 y?l? i?inde ba?vuran t?berk?lozlu olgularda antit?berk?loz ila?lara diren? sorunu. ?nfeksiyon Derg 1997;3(11):191-6.
- Bergman JS, Woods GL. Mycobacterial Growth indicator tube for susceptibility testing of Mycobacterium tuberculosis to isoniazid and rifampisin. Diagn Microbiol Infect Dis 1997;28(3):153-6.
- R?sch Gerdes S, Domehl C, Nardi G, Gismondo MR, Welscher HM, Pfyffer GE. Multicenter evaluation of the Mycobacteria Growth Indicator Tube for testing susceptibility of Mycobacterium tuberculosis to first line drug. J Clin Microbiol 1999;37(1):45-8.
- Canbau E, Truffot Pernot C, Boulahbal F, Wichlacz C, Grosset J, Jarlier V. Mycobacterial Growth Indicator Tube versus the proportion method on L?wenstein Jensen for antibiotic susceptibility testing of Mycobacterium tuberculosis. Eur J Clin Microbiol Infect Dis 2000;19(12):938-42.
- Macondo EA, Ba F, Gaye-Diallo A, Toure-Kane NC, Kaire O, Gueye-Ndiaye A, et al. Rapid suspeptibility testing of Mycobacterium tuberculosis by the Mycobacteria Growth Indicator Tube (MGIT AST SIRE). Clin Microbiol Infect 2000;6(7):363-7.
- Bergman JS, Fish G, Woods GL. Evulation of BBL MGIT (Mycobacteria Growth Indicator Tube) AST SIRE system for antimycobacterial susceptibility testing of Mycobacterium tuberculosis to 4 primary antituberculous drugs. Arch Pathol Lab Med 2000;124(1):82-6.
- Wing Wai Y, Steena CWT, Kin SL, Simon Kwok FL, Chi Hung C, Elaine PW. Comparison of MB/BacT system and agar proportion method in drug susceptibility testing of Mycobacterium tuberculosis. Diagn Microbiol Infect Dis 2001;39:229-32.
Yaz??ma Adresi (Address for Correspondence)
Dr. H?seyin G?D?C?O?LU
Y?z?nc? Y?l ?niversitesi T?p Fak?ltesi,
T?bbi Mikrobiyoloji Anabilim Dal?, VAN - TURKEY
e-mail: hguducu@hotmail.com