REVIEW
Doi: 10.5578/tt.6982
Tuberk Toraks 2014;62(1):79-84

Akci?er Kanserinde 7. Tnm Evrelemesinden 8.'ye Do?ru
Deniz K?KSAL1, Seha AKDUMAN2
1 Hacettepe ?niversitesi T?p Fak?ltesi, G???s Hastal?klar? Anabilim Dal?, Ankara, T?rkiye
1 Department of Chest Diseases, Faculty of Medicine, Hacettepe University, Ankara, Turkey
2 Tunceli Devlet Hastanesi, G???s Hastal?klar? Klini?i, Tunceli, T?rkiye
2 Clinic of Chest Diseases, Tunceli State Hospital, Tunceli, Turkey
?ZET
Akci?er Kanserinde 7. TNM Evrelemesinden 8.?ye Do?ru
Akci?er kanserinin anatomik yayg?nl???, TNM s?n?flamas?yla tan?mlan?r ve halen en ?nemli prognostik fakt?rd?r. T?m?r ?zelliklerindeki de?i?iklikler, tan?sal y?ntemlerdeki ve tedavideki geli?melere ba?l? olarak TNM-evreleme sistemi zamanla g?ncellenmektedir. 7. TNM evreleme sistemi, uluslararas?, olduk?a geni? ve retrospektif bir veri taban?na dayanarak olu?turulmu?tur. Verilerin retrospektif olmas? nedeniyle halen cevaplanmayan sorular vard?r. Bu nedenle ?Prospektif Akci?er Kanseri Evreleme Projesi? olu?turulmu?tur. Bu projede T, N, M tan?mlay?c?lar?n?n ayr?nt?l? de?erlendirilmesinin yan? s?ra, ?imdiye kadar hi? ele al?nmayan demografik veriler, histolojik ?zellikler, baz? biyokimyasal ve molek?ler prediktif ve prognostik belirleyiciler incelenmektedir. Proje 8. TNM evrelemesinin temelini olu?turacakt?r. Bu makalede akci?er kanserinde 7. TNM evrelemesinden 8.?ye do?ru muhtemel de?i?iklikler tart???lm??t?r.
Anahtar kelimeler: Akci?er kanseri, TNM evrelemesi
SUMMARY
From the 7th TNM Staging to the 8th in Lung Cancer
The anatomic extent of disease, that is described by the TNM-classification remains the most important prognostic factor for lung cancer. Based on the changes in tumor characteristics, advances in diagnostic methods and treatment strategies, TNM-classifications are updated from time to time. The 7th TNM-classification was created on the basis of an international, large, and retrospective database. However due to retrospective data, there are still unanswered questions. Therefore "Prospective Lung Cancer Staging Project" is designed. In this project, in addition to the detailed evaluation of T, N, M descriptors; other factors, which were not considered to be relevant to lung cancer staging before, were also analyzed such as demographic data, histologic characteristics, certain biochemical and molecular prognostic and predictive factors. This project will be the basis of 8th TNM-classification for lung cancer. In this manuscript, we discuss the probable changes from the 7th TNM classification to the 8th.
Key words: Lung cancer, TNM staging
G?R??
Evreleme, akci?er kanserli bir hastan?n de?erlendirilmesinde en ?nemli ad?md?r. Hastal???n yayg?nl???n? belirleyerek tedavinin planlanmas?n? ve prognozun ?ng?r?lmesini sa?lar. Akci?er kanseri evrelemesinde, hastal???n anatomik yayg?nl???n? temel alan ve ilk olarak 1946 y?l?nda Denoix taraf?ndan geli?tirilen T (T?m?r), N (Nod), M (Metastaz) sistemi kullan?lmaktad?r (1).
Halen 7. versiyonunu kulland???m?z TNM evrelemesinin ilk versiyonu 1973 y?l?nda Mountain taraf?ndan geli?tirilmi?, AJCC (American Joint Committee on Cancer) ve UICC (International Union against Cancer) taraf?ndan kabul g?rm??t?r (2). Bundan sonraki y?llarda, t?m?r ?zelliklerindeki de?i?iklikler, tan?sal y?ntemlerdeki ve tedavideki geli?melere ba?l? olarak evreleme sistemleri d?zenli olarak de?erlendirilerek g?ncellenmi?tir.
7. TNM evrelemesi
Halen kullanmakta oldu?umuz 7. TNM evreleme sistemi, 1973-1997 y?llar? aras?nda kullan?lan alt? evrelemenin ard?ndan, 2009 y?l?nda yay?nlanarak kullan?lmaya ba?lanm??t?r (3). 1997 y?l?nda kullan?ma giren 6. evrelemede, evreler aras? sa?kal?m e?rilerinin kesi?mesi ve evre tan?mlay?c?lar?n?n yetersiz olmas? nedeniyle, IASLC (International Association for the Study of Lung Cancer) taraf?ndan "Akci?er Kanseri Evreleme Projesi" olu?turulmu?tur (4,5). Projenin tamamlanmas? sonras?nda, ?nerilen de?i?iklikler, AJCC ve UICC taraf?ndan kabul g?rm??t?r. 7. evreleme sistemi, k???k h?creli d??? akci?er kanseri (KHDAK)'nin yan? s?ra bronkopulmoner karsinoid t?m?rlerin ve k???k h?creli akci?er kanseri (KHAK)'nin evrelenmesi i?in de ?nerilmi?tir (6,7).
7. TNM evreleme sisteminin en g??l? yan?, bug?ne kadar var olan en geni? veri taban?na sahip olmas?d?r. 1974 y?l?nda yay?nlanan ilk evrelemenin veri taban?nda tek merkezden 2155 hasta varken, 1997 y?l?nda yay?nlanan 6. evrelemenin veri taban?nda yine tek merkezden 5319 hasta yer alm??t?r (2,8). 7. TNM evreleme sisteminin dayana?? olan "Akci?er Kanseri Evreleme Projesi"nde ise Kuzey Amerika, Asya, Avrupa ve Avustralya'da bulunan 19 ?lkeden 46 merkez ve 100.869 hasta yer alm??t?r (4). Proje kapsam?nda, 1990-2000 y?llar? aras?nda, veri taban?na kay?tl? 100.869 hastan?n verileri retrospektif olarak de?erlendirilmi?tir. Ancak evreleme i?in gerekli verileri, tedavi ve takip kay?tlar? eksik olan 19.854 (%19.6) hasta proje d??? tutulmu?, 81.015 hasta projeye dahil edilmi?tir. Bu hastalar?n da 13.290'? KHAK iken 67.725'i KHDAK'd?r. Klinik evreleme 53.640 hastada, patolojik evreleme 33.933 hastada, hem klinik hem patolojik evreleme 20.006 hastada yap?lm??t?r. Hastalar?n %95'i en az 2 y?l veya ?l?me kadar izlenmi?tir. Verilerin de?erlendirilmesi i?in uygun istatistiksel y?ntem kullan?lm??, hem internal hem de eksternal validasyon yap?lm??t?r (9).
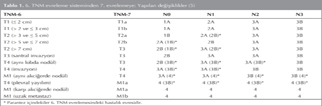
7. evreleme sistemiyle gelen yenilikler Tablo 1'de ?zetlenmi?tir (5). Bu evreleme sistemindeki en ?nemli yenilik, T belirteciyle ilgili olarak t?m?r ?aplar?na baz? s?n?r de?erler konmas?d?r. T1 t?m?rler ikiye ayr?lm??, ?ap? 2 cm ve alt?nda olanlar T1a; ?ap? 2 cm'den b?y?k, 3 cm ve alt?nda olanlar T1b olarak s?n?flanm??t?r. T2 t?m?rler de, ?ap? 3 cm'den b?y?k, 5 cm ve alt?nda olanlar T2a; ?ap? 5 cm'den b?y?k, 7 cm ve alt?nda olan T2b olarak s?n?flanm??t?r. ?ap? 7 cm'den b?y?k olan t?m?rler ise do?rudan T3 olarak de?erlendirilmi?tir. Di?er bir yenilik ise e?lik eden nod?llerle ilgilidir. Ayn? lobdaki uydu nod?ller T4 olarak evrelenirken T3; ayn? akci?er farkl? lobdaki nod?ller ise M1 olarak evrelenirken T4 olarak evrelenmi?tir. Malign plevra ve perikard ef?zyonu de?i?ikli?in yap?ld??? di?er bir durumdur. ?nceki evrelemede T4 olarak evrelense de, sa?kal?mlar?n?n M1 olgularla benzerli?i nedeniyle tedavileri de bu ?ekilde planlanan olgular, bu evreleme sisteminde M1a olarak evrelenmi?tir. Ayr?ca, M1 s?n?flamas? da ikiye ayr?lm??t?r; plevra/perikard ef?zyonu ve kar?? akci?er metastazlar? M1a olarak s?n?flan?rken, uzak organ metastazlar? M1b olarak s?n?flanm??t?r. T?m bu de?i?ikliklerin yan? s?ra genel hastal?k evresinde de de?i?iklikler olmu?, toplamda 10 evre grubu daha d???k evreye kayarken, 7 evre grubu ileri evreye kaym??t?r.
7. TNM evreleme sisteminin dayana?? olan "Akci?er Kanseri Evreleme Projesi"nin en ?nemli olumsuz yan?, primer olarak TNM evrelemesini g?ncellemek ama?l? toplanmam?? olan verileri retrospektif olarak de?erlendirmesidir. Olgu say?s? ?ok olmas?na kar??n kaliteli veri elde edilememi?tir. Bu durum olgular?n yakla??k %20'sinin proje d??? kalmas?ndan da anla??labilmektedir (10). Projede Afrika, G?ney Amerika, Hindistan gibi baz? b?lgeler yer almazken; Rusya, ?in ve Endonezya'n?n kat?l?m? da yetersizdir. Hastalar?n topland??? 1990-2000 y?llar? aras?nda, belli b?lgeler ve zaman periyodlar?nda tan? y?ntemleri standardize de?ildir ve her merkezde evreleme ama?l? pozitron emisyon tomografisi (PET) kullan?m? mevcut de?ildir. Ayr?ca, baz? veri tabanlar?n?n TNM s?n?flamas?n? ?al??mak i?in uygun olmad??? g?r?lm??t?r. Klinik ve/veya patolojik T tan?m? yap?lm?? olsa da, ayr?nt?n?n yer almamas? T3 ve T4 tan?mlay?c?lar? ?zerinde ?al??maya engel olmu?tur (11). Ayn? ?ekilde N1 ve N2 ayr?m? ve M1'in ?e?itli formlar? ?zerinde de ?al???lamam??t?r (12,13). B?lgeler aras?nda kullan?lan farkl? nodal haritalar (Naruke ve Mountain-Dressler gibi), N evreleme ?zerinde ?al??maya olanak vermemi? ve bu nedenle 7. evrelemede N s?n?flamas?yla ilgili de?i?iklik yap?lamam?? ancak yeni bir lenf nodu haritas? ?nerilmi?tir (14). Proje kapsam?nda her t?rl? tedavi modalitesini alan hastalar olsa da, cerrahi yap?lan olgular ?o?unluktad?r. Olgular?n da??l?m? uniform de?ildir ve belli hastal?k subgruplar? belli bir b?lgeden veya belli bir veri taban?ndan al?nsa da olduk?a farkl? y?ntemlerle tedavi edildikleri g?r?lm??t?r. Bu nedenle hastalar?n ald?klar? tedaviler de?erlendirmeye al?nmam??t?r (15). Lenfanjitis karsinomatoza varl???n?n evrelemeye etkisi de?erlendirilmemi?tir. Evreleme tamamen anatomik ?zelliklere dayand?r?lm??, prognostik ve prediktif oldu?u bilinen baz? molek?ler belirleyicilere yer verilmemi?tir.
G?r?ld??? ?zere 7. TNM evrelemesi, olduk?a ?nemli bir geli?medir, ?imdiye kadar maj?r de?i?ikliklerin yap?ld??? ilk evrelemedir ancak halen m?kemmel olmaktan uzakt?r.
7. evrelemenin b?t?n bu olumsuz yanlar?n? g?z ?n?ne alarak, IASLC prospektif bir proje ?nerisinde bulunmu?tur. Bu projeye daha ?nceki veri taban?nda yer almayan, G?ney Amerika ve Afrika da kat?lm??t?r. Projenin tamamlanmas?yla ?ekillenecek olan 8. TNM evrelemesinin 2016 y?l?nda yay?nlanmas? beklenmektedir. Projenin zaman ?izelgesi Tablo 2'de g?r?lmektedir (16). Projeye yeni tan? alan hastalar dahil edilmektedir. Veri toplanmas? i?in, web ortam?nda kolay kullan?labilen bir veri toplama sistemi olu?turulmu?tur. Veri toplama ve analizlerini, "Cancer Research ve Biostatistics (CRAB)" yapmaktad?r. Proje kapsam?nda toplanan veriler Tablo 3'te ?zetlenmi?tir.
8. TNM evrelemesinden beklenenler
T evresi
T?m?r boyutunun prognostik ?nemi 7. evrelemede ortaya konmu?tur. T?m?r boyutu sadece erken evrede de?il, ileri evre hastal?kta da ?nemlidir. Lokal ileri evre (evre 3A ve 3B) cerrahi aday? olmayan 12.315 hastan?n de?erlendirildi?i bir ?al??mada, hastalar t?m?r ?aplar?na g?re 4 gruba (0.1-3 cm; 3.1-5 cm; 5.1-7 cm; 7.1-20 cm) ayr?ld???nda, hastal?k spesifik ve genel sa?kal?m e?rilerinin ?ak??mad??? g?r?lm??t?r (17). 8. evrelemede de t?m?r boyutunun ?neminin ortaya konmas? beklenmektedir. Ayr?ca, her bir T tan?mlay?c?s?n?n s?n?flama do?rulu?unu saptamak ama?l?, T evresinin kay?tlar? ayr?nt?l? olarak tutulmaktad?r. Klinik olarak evrelenen olgularda, primer t?m?r?n yeri, boyutu ve yayg?nl???n?n yan? s?ra proje kapsam?nda lenfanjitis karsinomatoza (cLy) varl??? da de?erlendirilmektedir. Radyolojik olarak lenfanjitis karsinomatoza yok ise cLy0, primer t?m?r etraf?nda varsa cLy1, t?m?r alan? d???nda ancak ayn? lobda ise cLy2, ayn? taraf akci?erde ise cLy3, kar?? akci?erde ise cLy4 olarak kay?t alt?na al?nmaktad?r.
E?lik eden nod?l varl???nda, nod?l?n yeri (primer t?m?rle ayn? lobda, ayn? veya kar?? akci?erde), histolojisi, primer t?m?re mesafesinin kayd? yap?lmaktad?r. Cerrahi rezeksiyon yap?lan olgularda, visseral plevran?n tutulum derecesi de?erlendirilmektedir. Visseral plevra invazyonu, t?m?r?n elastik membran? a?mas? olarak tan?mlanmakta ve ??pheli durumlarda elastin boyalar? ile de?erlendirme yap?lmaktad?r (18). Ayr?ca, ven?z ve lenfatik invazyon varl???, fiss?rlerin durumu, g???s duvar? invazyonu olanlarda invazyon derinli?i ve plevral lavaj sitolojisi de?erlendirilmektedir (16). G???s duvar? invazyon derinli?i ?? grupta (pT3a: Sadece paryetel plevrada tutulum, pT3b: Endotorasik fasiyada tutulum, pT3c: Kosta ve yumu?ak dokuda tutulum) ele al?nmaktad?r.
Yak?n zamanda yay?nlanan bir meta-analizde, torakotomiden hemen sonra al?nan plevral lavaj sitolojisinin pozitif oldu?u olgularda, lokal ve uzak rek?rrens riskinin daha fazla oldu?u ve sa?kal?m?n olumsuz etkilendi?i g?r?lm??t?r (19). Mevcut evrelemede yer almayan plevral lavaj sitoloji pozitifli?inin inkomplet rezeksiyon olarak ele al?nmas? gerekti?i g?r??? hakim olup, bu hastalarda adjuvant tedavilerin kullan?lmas? uygun g?r?lmektedir (20).
N Evresi
7. TNM evrelemesi veri taban?nda, N evresine y?nelik yap?lan de?erlendirmelerde, N1 ve N2 kategorisinde yer alan farkl? nodal zonlar?n tutulumunun prognozu etkilemedi?i g?r?lm??t?r. Ancak tutulan nodal zon say?s?n?n prognostik ?nemi vard?r. Tek zon N1 tutulumu olan hastalar?n sa?kal?m?, ?ok zonda N1 tutulumu olan hastalardan daha iyi bulunmu?tur. Benzer ?ekilde tek zon N2'de metastaz olan hastalar?n sa?kal?m?, ?ok zon N2'de metastaz olanlardan daha iyi bulunmu?tur. Ayr?ca, ?ok zon N1 tutulumu, tek zon N2 tutulumuyla benzer prognoza sahip bulunmu?tur (12). Metastatik lenf nodu say?s?n?n ?nemini vurgulayan bir di?er ?al??mada, 2000-2006 y?llar? aras?nda opere edilen 1659 KHDAK'l? hasta, tutulan lenf nodu say?s?na g?re s?n?flanm?? (nN0: metastatik nod yok, nN1: 1-2 lenf nodunda, nN2: 3-6 lenf nodunda, nN3: 7 ve ?st?nde lenf nodunda metastaz) ve metastatik lenf nodu say?s?n?n y?ksek olmas? k?t? sa?kal?mla ili?kili bulunmu?tur (21).
7. evreleme projesinde farkl? lenf nodu haritalar?n?n kullan?lmas?; ayr?ca nodal zon say?s?n?n ?neminin validasyonunu yapacak ?l??de, her T evresine d??ecek N evresi say?s?n?n yeterli olmamas? sonucu, 7. evrelemede N evrelemesine y?nelik bir de?i?iklik yap?lamam??, ancak yeni bir lenf nodu haritas? ?nerilmi?tir. 8. evreleme projesi i?in de bu harita kullan?lmaktad?r. 8. evrelemede N evrelemesine y?nelik hedefler, N durumunun prognostik ?nemini saptamak; N1 ve N2 kategorilerinde tutulan lenf nodu alan?n?n prognostik ?nemini saptamak; N1 ve N2 kategoride, nodal yayg?nl???n (tek veya ?ok istasyon), nod b?y?kl???n?n (tutulan en b?y?k nodun N kategorisi), her nodal kategoride tutulan nodlar?n ve ekstrakaps?ler yay?m varl???n?n prognostik ?nemini saptamak; N3 nodal lokasyonun (kar?? mediyasten, ipsilateral veya kontralateral supraklavikuler fossa) prognostik ?nemini belirlemektir.
M Evresi
7. evreleme sisteminin veri taban? de?erlendirildi?inde, ?ok say?da uzak organ metastaz? olan hastalar?n sa?kal?m?, tek uzak organ metastaz? olanlara g?re biraz daha k?t? bulunmu?tur. Uzak metastazlar?n?n yerleri kar??la?t?r?ld???nda ise belirgin bir prognoz fark? saptanmazken, beyin metastaz? varl??? biraz daha k?t? prognozla ili?kili bulunmu?tur. 7. evreleme sisteminde uzak organ metastazlar? M1b olarak tan?mlanm??, ancak veri taban? M1b'yi subgrupland?rmak i?in yeterli olmam??t?r (13). 8. evrelemede M evrelemesi i?in hedefler, 7. evrelemede tan?mlanan M durumunun prognostik ?nemini ortaya koymak; tek organda tek metastaz, tek organda ?ok metastaz veya birden ?ok organda ?oklu metastaz?n prognostik ?nemini saptamakt?r (16).
Di?er
8. evreleme projesi i?in toplanan veriler incelenirse, bu evrelemede ilave hedeflerin oldu?u g?r?lebilmektedir (Tablo 3). ?imdiye kadar hi?bir evreleme sisteminde g?ndeme getirilmeyen, hastal???n anatomik yayg?nl??? d???nda baz? fakt?rlerin prognostik ?neminin ara?t?r?lmas? i?in veri toplanmaktad?r. Demografik verilerin (ya?, cinsiyet, ?rk) yan? s?ra, baz? klinik durumlar (performans durumu, kilo kayb?, komorbid durumlar), baz? laboratuvar parametreleri (laktat dehidrogenaz, alkalen fosfataz, kalsiyum, sodyum, albumin, hemoglobin d?zeyi, beyaz k?re, n?trofil ve trombosit say?s?), solunum fonksiyon testleri, PET/CT verileri ve t?m?r?n histolojik ?zellikleri, diferansiyasyon derecesi kaydedilmektedir (12). Cerrahi rezeksiyon yap?lan olgularda klinik (cTNM) ve patolojik (pTNM) TNM evresi kar??la?t?r?larak klinik evreleme y?ntemlerinin g?venilirli?i ara?t?r?lacakt?r.
PET/CT g?n?m?zde akci?er kanseri evrelemesinde yayg?n olarak kullan?lan ve klinik evreleme do?rulu?unu art?ran ?nemli bir g?r?nt?leme y?ntemidir. Ayr?ca, tedavi ?ncesi ?l??len primer t?m?r SUVmaks de?erinin ba??ms?z bir prognostik fakt?r oldu?u g?sterilmi?tir (22). Bu nedenle yeni proje kapsam?nda primer t?m?rdeki, metastatik lenf nodlar? ve uzak metastaz b?lgelerindeki SUVmaks de?erleri kaydedilmektedir.
Tam, tam olmayan veya emin olunmayan rezeksiyonlar?n prognostik ?nemi di?er bir ara?t?rma konusudur (16). Emin olunmayan rezeksiyon tan?m? bu projede g?ndeme getirilmi?tir. Makroskopik veya mikroskopik rezid?el t?m?r kalmam?? ancak tam rezeksiyon diyebilmek i?in yeterli say?da lenf nodu (en az alt? istasyon ?rneklenmi?, bunlardan ??? subkarinal alan? i?erecek ?ekilde mediastinal, ??? N1 istasyon olacak ?ekilde) ??kar?lmam?? ise veya ??kar?lan en y?ksek lenf nodu metastatik bulunmu?sa emin olunmayan rezeksiyon olarak s?n?flanm??t?r.
Sonu? olarak; 7. TNM evrelemesi olduk?a ?nemli bir geli?medir, ?imdiye kadar maj?r de?i?ikliklerin yap?ld??? ilk evrelemedir, ancak halen m?kemmel olmaktan uzakt?r. Metodolojisi iyi tan?mlanm??, prospektif bir veri taban?na dayal? olacak olan 8. TNM evrelemesi, ?nceki evrelemelerin eksik y?nleri bir ?l??de kapatacak gibi g?r?nmektedir, ancak analiz sonu?lar?n?n hen?z ??km?? olmamas? nedeniyle, yorum yapmak i?in erkendir.
?IKAR ?ATI?MASI
Bildirilmemi?tir.
KAYNAKLAR
- Denoix PF. Enquete permanent dans les centres anticancereux. Bull Inst Natl Hyg 1946;1:70-5.
- Mountain CF, Carr DT, Anderson WA. A system for the clinical staging of lung cancer. Am J Roentgenol Radium Ther Nucl Med 1974;120:130-8.
- Goldstraw P. International Association for the Study of Lung Cancer Staging Manual in Thoracic Oncology. 1st ed. Florida, USA: Editorial Rx Press; 2009.
- Goldstraw P, Crowley JJ. The International Association for the Study of Lung Cancer international staging project on lung cancer. J Thorac Oncol 2006;1:281-6.
- Goldstraw P, Crowley J, Chansky K, Giroux DJ, Groome PA, Rami-Porta R, et al. The IASLC Lung Cancer Staging Project: proposals for the revision of the TNM stage groupings in the forthcoming (seventh) edition of the TNM classification of malignant tumors. J Thorac Oncol 2007;2:706-14.
- Shepherd FA, Crowley J, Van Houtte P, Postmus PE, Carney D, Chansky K, et al. The IASLC Lung Cancer Staging Project: proposals regarding the clinical staging of small-cell lung cancer in the forthcoming (seventh) edition of the TNM classification for lung cancer. J Thorac Oncol 2007;2:1067-77.
- Travis WD, Giroux DJ, Chansky K, Crowley J, Asamura H, Brambilla E, et al. The IASLC Lung Cancer Staging Project: Proposals for the inclusion of Carcinoid tumours in the forthcoming (seventh) edition of the TNM Classification for Lung Cancer. J Thorac Oncol 2008;3:1213-23.
- Mountain CF. Revisions in the international system for staging lung cancer. Chest 1997;111:1710-7.
- Groome PA, Bolejack V, Crowley JJ, Kennedy C, Krasnik M, Sobin LH, et al. The IASLC Lung Cancer Staging Project: Validation of the proposals for revision of the T, N and M descriptors and consequent stage groupings in the forthcoming (seventh) TNM classification for lung cancer. J Thorac Oncol 2007;2:694-705.
- Turna A. 7. evrelemeye do?ru: yan?tlar?n? ald???m?z sorular ve havada kalan ?mitlerimiz. T?rk G???s Kalp Damar Cer Derg 2008;16:71-3.
- Rami-Porta R, Ball D, Crowley J, Giroux DJ, Jett J, Travis WD, et al. The IASLC Lung Cancer Staging Project: proposals for the revision of the T descriptors in the forthcoming (seventh) edition of the TNM classification for lung cancer. J Thorac Oncol 2007;2:593-602.
- Rusch VW, Crowley J, Giroux DJ, Goldstraw P, Im JG, Tsuboi M, et al. The IASLC Lung Cancer Staging Project: proposals for the revision of the N descriptors in the forthcoming seventh edition of the TNM classification for lung cancer. J Thorac Oncol 2007;27:603-12.
- Postmus PE, Brambilla E, Chansky K, Crowley J, Goldstraw P, Patz EF Jr, et al. The IASLC Lung Cancer Staging Project: proposals for revision of the M descriptors in the forthcoming (seventh) edition of the TNM classification of lung cancer. J Thorac Oncol 2007;2:686-93.
- Rusch V, Asamura H, Watanabe H, Giroux DJ, Rami-Porta R, Goldstraw P, et al. The IASLC Lung Cancer Staging Project: A Proposal for a New International Node Map in the Forthcoming Seventh Edition of the TNM Classification for Lung Cancer. J Thorac Oncol 2009;4:568-77.
- Detterbeck FC, Postmus PE, Tanoue LT. The stage classification of lung cancer. Diagnosis and management of lung cacer, 3rd ed: ACCP evidence-based clinical practice guidelines. Chest 2013;143(5)(Suppl):e191-e210.
- Giroux DJ, Rami-Porta R, Chansky K, Crowley JJ, Groome PA, Postmus PE, et al. The IASLC Lung Cancer Staging Project. Data elements for the prospective Project. J Thorac Oncol 2009;4:679-83.
- Morgensztern D, Wagar S, Subramanian J, Gao F, Trinkaus K, Govindan R. Prognostic significance of tumor size in patients with stage III non-small cell lung cancer. A Survelliance, Epidemiology, and End Results (SEER) survey from 1998 to 2003. J Thorac Oncol 2012;7:1479-84.
- Travis WD, Brambilla E, Rami-Porta R, Vallieres E, Tsuboi M, Rusch V, et al. International Staging Committee. Visceral pleural invasion: pathologic criteria and use of elastin stain: proposal for the 7th edition of TNM classification for lung cancer. J Thorac Oncol 2008;3:1384-90.
- International Pleural Lavage Cytology Collaborators. Impact of positive pleural lavage cytology on survival in patients undergoing lung resection for non-small cell lung cancer: an international individual patient data meta-anlaysis. J Thorac Cardiovasc Surg 2010;139:1441-6.
- Toufektzian L, Sepsas E, Drossos V, Gkiozos I, Syrigos K. Pleural lavage cytology: where do we stand? Lung Cancer 2013 Oct 27. Doi: 10.1016/ j.lungcan. 2013.10.012.
- Wei S, Asamura H, Kawachi R, Sakurai H, Watanabe S. Which is the beter prognostic factor for resected non-small cell lung cancer. The number of metastatic lymph nodes or the currently used nodal stage classification? J Thorac Oncol 2011;6:310-8.
- Berghmans T, Dusart M, Paesmans M, Hossein-Foucher C, Buvat I, Castaigne C, et al. Primary tumour standardized uptake value (SUV max) measured on florodeoxyglucose emission tomography (PDG-PET) is of prognostic value for survival in non-small cell lung cancer (NSCLC): A systematic review and meta-analysis (MA) by the European Lung Cancer Working Party for the IASLC Lung Cancer Staging Project. J Thorac Oncol 2008;3:6-12.
Yaz??ma Adresi (Address for Correspondence)
Dr. Deniz K?KSAL
Hacettepe ?niversitesi T?p Fak?ltesi,
G???s Hastal?klar? Anabilim Dal?,
ANKARA - TURKEY
e-mail: deniz_koksal@yahoo.com