REVIEW
Doi: 10.5578/tt.6810
Tuberk Toraks 2014;62(1):68-78

Santral Uyku Apne Sendromu Tedavisi, G?ncel Bilgiler ve Literat?r?n G?zden Ge?irilmesi
Handan ?N?N? K?SEO?LU1, Asiye KANBAY2, O?uz K?KT?RK3
1 Gaziosmanpa?a ?niversitesi T?p Fak?ltesi, G???s Hastal?klar? Anabilim Dal?, Tokat, T?rkiye
1 Department of Chest Diseases, Faculty of Medicine, Gaziosmanpasa University, Tokat, Turkey
2 ?stanbul G?ztepe E?itim ve Ara?t?rma Hastanesi, G???s Hastal?klar? Klini?i, ?stanbul, T?rkiye
2 Clinic of Chest Diseases, Istanbul Goztepe Training and Research Hospital, Istanbul, Turkey
3 Gazi ?niversitesi T?p Fak?ltesi, G???s Hastal?klar? Anabilim Dal?, Ankara, T?rkiye
3 Department of Chest Diseases, Faculty of Medicine, Gazi University, Ankara, Turkey
?ZET
Santral Uyku Apne Sendromu Tedavisi, G?ncel Bilgiler ve Literat?r?n G?zden Ge?irilmesi
Santral uyku apne sendromu (central sleep apnea syndrome, CSAS); solunum merkezinden kaynaklanan solunum d?rt?s?n?n azalmas? veya kaybolmas? sonucu uykuda solunum durmas?yla karakterize bir hastal?k tablosudur. Uyku bozukluklar? merkezine ba?vuran olgular?n %5'inden az?nda g?r?lmekle birlikte, konjestif kalp yetmezli?i, b?brek yetmezli?i, santral sinir sistemi patolojilerinin varl???nda CSAS g?r?lme oran? artar. Uluslararas? Uyku Bozukluklar? S?n?flamas?n?n son versiyonunda (International Classification of Sleep Disorders, ICSD-2) alt? ba?l?kta toplanm?? olan CSAS'?n tedavisi, her bir CSAS tipi i?in ayr?cal?k g?sterir. Bu derlemede CSAS tedavi yakla??mlar?n?n g?ncel bilgiler ?????nda g?zden ge?irilmesi ama?lanm??t?r.
Anahtar kelimeler: Santral uyku apne sendromu, Cheyne-stokes solunumu, adaptif servo ventilasyon
SUMMARY
The Treatment of Central Sleep-apnea Syndrome, Updated Information, and Review of the Literature
Central sleep-apnea syndrome (CSAS) is a disease state characterized by respiratory arrest as a result of decrease or lack of respiratory drive originating from respiratory center. Although it is seen in less than 5% of the casses who consult to the sleep disorders center, incidence of CSAS increases in the presence of congestive heart and/or renal failure, and central nervous system abnormalities. Treatment of CSAS which has been analyzed under six headings in the last version of International Classification of Sleep Disorders (ICSD-2), differs among each type of CSAS. In this review, our aim is to analyze treatment alternatives for CSAS in the light of currently updated information.
Key words: Central sleep apnea syndrome, cheyne-stokes respiration, adaptive servo ventilation
G?R??
Santral uyku apne sendromu (central sleep apnea syndrome, CSAS); solunum merkezinden kaynaklanan solunum d?rt?s?n?n azalmas? veya kaybolmas? sonucunda uykuda solunum durmas?yla karakterize bir hastal?k tablosudur (1). Bir ba?ka ifadeyle solunum merkezinin solunum kaslar?na komut vermesinde aksamalar geli?mektedir. Sonu?ta solunum yoklu?uyla birlikte solunum ?abas? da durmu?, g???s-kar?n hareketleri kaybolmu?tur. CSAS toplumda nadir g?r?l?r, uyku bozukluklar? merkezine ba?vuran olgular?n %5'inden az?n? CSAS'l? olgular olu?turur; ancak baz? klinik bozukluklarda CSAS prevalans? artar (2). ?rne?in; konjestif kalp yetmezli?i (KKY) olan olgularda CSAS prevalans? %30-50 aras?nda bildirilmektedir (3).
Santral uyku apne sendromlar? Uluslararas? Uyku Bozukluklar? S?n?flamas?n?n 2. versiyonunda (International Classification of Sleep Disorder-2, ICSD-2) alt? ba?l?kta toplanm??t?r (4):
I. Primer santral uyku apne sendromu
II. Cheyne-Stokes solunumuna ba?l? santral uyku apne sendromu
III. Y?ksek irtifa periyodik solunumuna ba?l? santral uyku apne sendromu
IV. Cheyne-Stokes d??? medikal durumlara ba?l? santral uyku apne sendromu
V. ?la? veya madde kullan?m?na ba?l? santral uyku apne sendromu
VI. Primer infant santral uyku apne sendromu
Bu derlemede CSAS ile ilgili tedavi yakla??mlar?n?n g?ncel bilgiler ?????nda g?zden ge?irilmesi ama?lanm??t?r. ?nfantta g?r?len CSAS hari?, di?er CSAS tipleri i?in tedavi se?enekleri ayr? ayr? de?erlendirilecek, konuyla ilgili en son 2012 y?l?nda Amerikan Uyku T?bb? Akademisi (American Academy of Sleep Medicine, AASM) taraf?ndan yay?nlanm?? olan rehberin ?nerileri vurgulanacakt?r.
PRIMER CSAS TEDAV?S?
Primer CSAS'da, etyoloji bilinmemektedir. Fizyopa-tolojisinde; karbondioksite (CO2) kar?? artm?? yan?ta (hiper kemosensitivite) ba?l? solunum kontrol?nde instabilite ve bunun sonucu meydana gelen hipokapninin predispoze fakt?r oldu?u d???n?lmektedir. Nadir g?r?len bir durum oldu?u i?in tedavi yakla??mlar?yla ilgili az say?da ?al??ma mevcuttur ve yap?lan ?al??malar?n kan?t d?zeyleri d???kt?r. Primer CSAS olu?umunda hiperventilasyona ba?l? hipokapni sorumlu tutuldu?undan, teorik olarak CO2 d?zeyinin y?kseltilmesi santral apnelerin d?zelmesinde fayda sa?layacakt?r. Karbondioksit ile zenginle?tirilmi? hava solutulmas? veya ?l? bo?luk hacminin art?r?lmas? arter kan?ndaki CO2 parsiyel bas?nc?nda (pCO2) 1-3 mmHg art?? sa?layarak santral apneleri engelleyebilir. Konuyla ilgili 6 primer CSAS tan?l? hastan?n de?erlendirildi?i bir nonrandomize ?al??mada; olgulara ilk gece yaln?zca oda havas? solutulmu?, ikinci gece ba?lang??ta oda havas? solutulduktan sonra santral apneler g?r?ld???nde y?z maskesi tak?larak CO2'den zenginle?tirilmi? gaz kar???m? solutulmu?. FICO2 %1.0-2.0 oldu?unda t?m hastalarda santral apnelerin kayboldu?u g?r?lm??. ???nc? gece FICO2 %1.5-2.3 ?eklinde art?r?ld???nda transk?tan?z yolla ?l??len pCO2'nin artt??? g?r?lm??. D?rd?nc? gece ?al??may? s?rd?ren 4 olguya, y?z maskesi tak?larak ?l? bo?luk hacmi 100 cc art?r?lm??. ?al??man?n sonucunda; CO2'den zenginle?tirilmi? gaz solutulmas? veya ?l? bo?luk eklenmesiyle transk?tan?z olarak ?l??len pCO2'nin artt???, santral apne-hipopnelerin kayboldu?u tespit edilmi?tir (5). Karbondioksit solutma i?leminin kolay uygulanabilir bir y?ntem olmamas? ve CO2'nin kolay elde edilememesi nedeniyle AASM taraf?ndan, bu yakla??m primer CSAS i?in bir tedavi se?ene?i olarak ?nerilmemektedir (6).
Primer CSAS'da bir di?er tedavi yakla??m? olarak solunumu stim?le eden ajanlar?n etkinli?i ara?t?r?lm??t?r. Bu ajanlardan biri olan asetazolamid (ACET) karbonik anhidraz enzimini inhibe ederek metabolik asidoz olu?turur ve solunum merkezini stim?le eder. D???k doz (250 mg/g?n) ACET'in, 14 hastada, bir gece kullan?m? sonras?, santral apne-hipopne indeksi (AH?)'nin 25.5 ? 6.8'den 13.8 ? 5.2'ye, bir ay kullan?m? sonras? ise 6.6 ? 2.9'a geriledi?i (p< 0.01), bununla birlikte g?nd?z uykululukta d?zelme oldu?u, obstr?ktif apne indeksi (OA?), total uyku zaman? ve uyku etkinli?inde anlaml? de?i?iklik olmad??? g?sterilmi?tir (7). Farkl? bir ?al??mada ise y?ksek doz (1000 mg/g?n) ACET'in, 6 hastada, bir hafta kullan?m?yla pH'da (7.42 & 7.34), santral apne indeksinde (SA?) (54 ? 29 & 12 ? 20), total apne say?s?nda %69 azalma, uyku kalitesi ve g?nd?z uykululukta iyile?me izlenmi?tir (8). Primer CSAS'da ACET kullan?m?yla ilgili kan?tlar?n s?n?rl? olmas?, ACET'in parestezi, kulak ??nlamas?, gastrointestinal semptomlar, elektrolit bozuklu?u, metabolik asidoz, uykululuk-uyu?ukluk gibi yan etkileri olmas? nedeniyle AASM rehberinde rutin kullan?m? ?nerilmemi?, tedavide opsiyonel olarak d???n?lebilece?i belirtilmi?tir (6).
Primer CSAS'?n medikal tedavisinde etkinli?i ara?t?r?lan di?er ajanlar sedatiflerdir. Arousallar hiperventilasyona neden olarak santral apne olu?umunu ind?kler. K?sa etkili benzodiazepinlerin arousal say?s?n? azaltt??? g?sterilmi?tir. Nonbenzodiazepin grubundan bir hipnotik ajan olan zolpidemin, 20 hastada, dokuz haftal?k kullan?m?yla santral AH?'nin (26.0 ? 17.2 & 7.1 ? 11.8, p< 0.001), arousal say?s?n?n (24.0 ? 11.6 & 15.1 ? 7.7, p< 0.001) azald???, uyku kalitesi ve g?nd?z uykululu?un iyile?ti?i, uyku s?reklili?inin sa?land???, obstr?ktif AH? ve oksijen sat?rasyonunda de?i?iklik olmad??? (k?t?le?me de olmad???) g?sterilmi?tir (9). Farkl? bir ?al??mada 5 hastada, Triazolam, plasebo ile kar??la?t?r?lm??, triazolam grubunda santral apnelerin anlaml? d?zeyde azald???, total uykunun artt???, uyku kalitesi ve g?nd?z performans?n iyile?ti?i g?sterilmi?tir (10). Sedatifleriyle ilgili az say?da ?al??ma olmas? ve bu ?al??malar?n da az say?da olgularla yap?lm?? olmas? nedeniyle CSAS'?n tedavisindeki yerinden net olarak bahsedilememektedir. Sedatiflerin solunum depresyonu gibi yan etkileri nedeniyle ?ncelikli kullan?mlar?n?n tercih edilmemesi, di?er tedavi se?enekleri ba?ar?s?z olursa ve hastada solunum depresyonuna neden olacak bir risk fakt?r? yoksa tedavide d???n?lmesi ?nerilmektedir (6). Hipnotik ajanlar?n kullan?ld??? olgularda yak?n klinik takip yap?lmal?d?r.
Primer CSAS'da pozitif hava yolu bas?nc? (Positive Airway Pressure, PAP) tedavisinin etkinli?inin ara?t?r?ld??? ?al??ma say?s? son derece k?s?tl?d?r. S?rekli pozitif bas?n? uygulayan CPAP (Continous Positive Airway Pressure) tedavisinin faringeal kollapsa ba?l? reflekslerin yol a?t??? santral apneleri ortadan kald?rd??? bilinmektedir. Ayr?ca, arousal ve hiperventilasyonu engelleyerek, hafif derecede CO2 retansiyonuna neden olmaktad?r. Santral solunumsal olaylar? potansiyel d?zelticidir, anlaml? bir riski yoktur, pek?ok merkezde bulunabilen cihazlar olmas? nedeniyle primer CSAS'da tedavi se?ene?i olarak d???n?lebilir (6).
Cheyne-Stokes Solunumuna Ba?l? CSAS Tedavisi
Cheyne-Stokes solunumu (CSS, periyodik solunum), konjestif kalp yetmezli?i (KKY), inme, y?ksek irtifa ve b?brek yetmezli?inde g?r?len bir solunum paternidir. KKY'li olgular?n %30-40'?nda CSS g?r?l?r. Bu olgular genellikle ejeksiyon fraksiyonu (EF) d???k, aritmi prevalans? daha y?ksek olgulard?r. KKY'li olgularda CSS/CSAS varl??? artm?? morbidite ve mortaliteyle ili?kilidir (6,11). KKY'ye sekonder CSS-CSAS tedavisi ?u ba?l?klar alt?nda sunulacakt?r:
Altta yatan KKY'nin etkin medikal tedavisi
Oksijen tedavisi
Karbondioksit inhalasyonu
Solunum stim?lanlar?
PAP tedavisi
CPAP (Continous Positive Airway Pressure)
BPAP (Bilevel Positive Airway Pressure)
ASV (Adaptive Servo Ventilation)
Frenik sinir stim?lasyonu
Kardiyak m?dahaleler
Altta Yatan KKY'nin Etkin Medikal Tedavisi
KKY'ye sekonder CSS-CSAS'l? olgular?n tedavisinde ?ncelikli olan, KKY'nin etkin medikal tedavisidir. Bu ama?la di?retikler, beta-blokerler ve ACE inhibit?rleri kullan?lmaktad?r. Yap?lan bir ?al??mada; fonksiyonel klasifikasyonu New York Hearth Association (NYHA) Class II-III, sol ventrik?l ejeksiyon fraksiyonu (EF) < %50 olan 16 hastada, 6 ayl?k Carvedilol (beta-bloker) tedavisi sonras? sol ventrik?l EF'de art?? (32 ? 7.4 & 45 ? 9.8, p< 0.001) brain natri?retik peptid (BNP) d?zeyi [159 (69-458) pg/mL & 38 (16-193) pg/mL, p= 0.017], AH? (34 ? 13 & 14 ? 13, p= 0.003) ve SA? (13 ? 11 & 1.9 ? 4.3, p< 0.001)'de anlaml? azalma izlenmi?tir (12). Bu ?al??man?n sonucunda; beta-blok?rlerin CO2'ye kar?? santral kemosensitiviteyi azaltarak ve sol ventrik?l EF'yi art?rarak santral solunumsal olaylarda d?zelme sa?lad??? bildirilmi?tir. Bir di?er medikal ajan olan kaptopril (ACE inhibit?r?)'in, NYHA Class II-III, hafif-orta derecede kalp yetmezli?i olan 8 hastada, bir ayl?k kullan?m? sonras?nda; PSG de?erlendirmesinde y?zeyel uykuda azalma, derin uyku ve REM uykusunda art??, AH? ve arousal say?s?nda anlaml? d?zelme izlenmi?tir. Olgulardan yedisine bir gecelik oksijen tedavisi eklenmesiyle uyku evreleri ve solunumsal olaylarda daha da iyile?me oldu?u g?zlenmi?tir (13). Bu ?al??man?n sonucunda; medikal tedavilerin santral solunumsal olaylarda d?zelme sa?lasalar bile, KKY'ye sekonder CSAS tedavisini ba??ms?z olarak sa?layaca??n? s?ylemenin g?? oldu?u belirtilmi?tir. Farkl? bir ?al??mada; anemisi olan KKY olgular?nda, anemi tedavisinin solunumsal olaylara etkisi ara?t?r?lm??t?r. Otuz sekiz hastada, eritropoetin (EPO) ve intraven?z demir (IV Fe) tedavisiyle, 3 ay sonunda; santral AH? (26.5 ? 14.6 & 18.6 ? 7.7), obstr?ktif AH? (9.4? ?10.9 & 6.9 ? 9.8) ve Cheyne-Stokes solunumunda (13.1 ? 16.4 & 9.0 ? 12.2) anlaml? azalma izlenmi?tir. ?al??mada hemoglobin d?zeyindeki art??la, santral apneler, oksijen sat?rasyonu, Epworth uykululuk skoru, ve NYHA s?n?f? korele olarak bulunmu?tur (p< 0.001). Ancak; kan?t d?zeylerinin d???kl??? ve potansiyel yan etkileri nedeniyle, EPO ve IV Fe tedavileri rutinde ?nerilmemektedir (14).
Oksijen tedavisi
Uykuda, oksijenin solunum kontrol? ?zerindeki etki mekanizmas? komplekstir. Hipoksi; periferik kemoresept?r duyarl?l???nda art??a neden olarak, hiperventilasyona bu da hipokapniye yol a?ar. Hiperoksi; periferik kemoresept?rlerde inhibisyona yol a?arak, solunum kontrol? ?zerindeki "loop gain" ad? verilen feedback mekanizmay? bask?lar (15,16). KKY'li olgularda oksijen tedavisinin solunumsal parametreler ve kardiyak fonksiyonlar ?zerine etkisinin de?erlendirildi?i ?al??malardan baz?lar? Tablo 1'de g?sterilmi?tir (17,18,19,20,21). Bir?ok ?al??mada AH? ve EF ?zerine olumlu etkilerinin g?zlenmesi nedeniyle, nokt?rnal oksijen tedavisi, KKY ile ili?kili CSAS tedavisinde endikedir (6).
Karbondioksit ?nhalasyonu
Primer CSAS'daki etki mekanizmas?na benzer ?ekilde pCO2'deki art??, KKY tan?l? CSS-CSAS'l? olgularda santral solunumsal olaylarda etkili olabilmektedir. A??r KKY olan (EF< %35, NYHA III-IV) 6 hastada, %3'l?k CO2'nin (pCO2'de 4-5 mmHg art??a yol a??yor) 3 gece solutulmas? sonras?; CSS s?resi/total uyku zaman? oran? (%62-2.2 p= 0.0012) ve NREM AH? (33.5 & 0 p= 0.026)'de anlaml? azalma izlenmi?tir. ?al??mada santral AH? ile ilgili bilgi verilememi?tir (22). Karbondioksit, kolay elde edilebilir ve uygulanabilir bir gaz olmamas? nedeniyle, g?n?m?zde tedavi se?ene?i olarak ?nerilmemektedir (6).
Solunum stim?lanlar?
Teofilin, solunum merkezine direkt stimulat?r etkiyle solunumu art?ran bir ajand?r. Teofilin etkisinin plasebo ile kar??la?t?r?ld??? bir ?al??mada; EF< %45 olan 15 hastada, 5 g?nl?k teofilin tedavisi sonras?, teofilin alan grupta bazal de?erlere g?re AH? (p< 0.001), SA? (p< 0.001), gece < %90 desat?rasyon zaman?nda (p< 0.05) anlaml? iyile?me g?r?l?rken, EF'de de?i?iklik izlenmemi?tir (23). Farkl? bir ?al??mada, stabil KKY'li 36 hastada, teofilin tedavisi sonras? AH?, SA?, AR?, oksijen desat?rasyonunda anlaml? d?zelme olurken, uyku mimarisi-etkinli?i ve obstr?ktif AH?'de de?i?iklik g?r?lmemi?tir (24). Bir di?er solunum stim?lan? olan ACET'in KKY'li 20 hastada, santral apneler ?zerine etkinli?inin plasebo ile kar??la?t?r?ld??? randomize ?ift-k?r, prospektif bir ?al??mada, plasebo grubunda bazal de?erlere g?re de?i?iklik izlenmezken, ACET alanlarda santral apne say?s? (49 ? 28 & 23 ? 21, p= 0.004) ve < %90 desat?rasyon zaman?nda (19 ? 32 & 6 ? 13; p= 0.01) azalma, uyku kalitesi ve g?nd?z uykululukta subjektif d?zelme izlenmi?, EF'de anlaml? d?zelme tespit edilmemi?tir (25). Sonu?ta; ACET ve teofilinin, CSAS'?n e?lik etti?i KKY tedavisinde kullan?m?yla ilgili kan?tlar s?n?rl?d?r, ancak; standart medikal tedavi optimize edildikten sonra, PAP tedavisini tolere edemeyen hastalara yak?n klinik takip ile uygulanabilir (6).
PAP tedavisi
CPAP: KKY'nin e?lik etti?i CSAS-CSS tedavisinde ?zerinde en ?ok ?al??ma yap?lan tedavi yakla??m? CPAP'd?r. Amerikan Kalp Cemiyeti (American Colle-ge of Cardiology/American Heart Association, ACC/AHA)'nin 2005 y?l?nda yay?nlad??? kronik kalp yetmezli?i tan?-tedavi k?lavuzunda; sol ventrik?l sistolik disfonksiyonu olan, CSS veya obstr?ktif apnelerin e?lik etti?i olgularda, CPAP tedavisinin sol ventrik?l yap? ve fonksiyonunu iyile?tirdi?i bildirilmektedir (26). CPAP tedavisinin etkileri ??yle ?zetlenebilir (27,28):
?st hava yolu direncini azalt?r.
Kollabe ve ventile olmayan alveolleri a?ar, oksijenasyonu art?r?r.
?ntratorasik bas?nc? art?r?r, interstisyel s?v? vask?ler kompart?mana ?ekilir ve pulmoner ?dem d?zelir.
Miyokardiyal transmural bas?n? fark?n? azalt?r, b?ylece miyokard gerilimi ve y?k? azal?r, kalbin ?n y?k? ve ard y?k? azal?r, sonu?ta at?m hacmi ve kalp debisi artar.
Solunum s?ras?nda plevral bas?n? dalgalanmalar?n? engelleyerek kalp h?z? de?i?kenli?ini azalt?r.
?l? bo?luk olu?turarak, pCO2 d?zeyini art?r?r, CO2'deki dalgalanmalar? azalt?r.
Sempatik aktiviteyi azalt?r.
Miyokard kanlanmas?n? (oksijenasyonu) d?zelterek aritmileri giderir.
Dispneyi d?zeltir, ya?am kalitesini art?r?r.
CPAP tedavisiyle santral apneler ilk gecede tamam?yla d?zelebilir. AH?> 15 olan KKY'li 29 hastada (21 CSAS, 8 OSAS) bir gecelik CPAP tedavisi sonras?, CSAS'l? olgular?n 9 (%43)'unda CPAP yan?t? elde edilmi?tir (29). CPAP'a yan?t veren-vermeyen olgular kar??la?t?r?ld???nda; demografik ?zellikler, arter kan gaz? parametreleri, sol ventrik?l EF, kan bas?nc? parametrelerinin her iki grupta benzer oldu?u g?r?lm??t?r. CPAP'a yan?t vermeyenlerde AH? ve SA?'nin daha y?ksek oldu?u tespit edilmi?, CPAP'a yan?t verenlerde ise VPS, ventrik?ler ta?ikardi gibi aritmilerin, periyodik solunum paterninin, arousal indeksinin d?zeldi?i g?r?lm??. Bu parametrelerin hi?biri CPAP yan?ts?zlarda d?zelmemi?tir. Farkl? bir ?al??mada ise; EF< %50, NYHA Class III-IV olan 8 hastaya iki gece uygulanan CPAP tedavisi sonras?, CSS say?s?, AH?, AR?, oksijen sat?rasyonunda de?i?iklik izlenmezken, uyku kalitesinde bozulma, insomni ?ikayetleri, total uyku zaman? ve uyku etkinli?inde azalma oldu?u g?r?lm??t?r (30). CPAP'?n uzun s?reli etkilerinin de?erlendirildi?i ?al??malara bakt???m?zda; CANPAP (Canadian Continuous Positive Airway Pressure for Patients with Central Sleep Apnea and Heart Failure) ?al??mas?nda; NYHA II-IV, EF< %40 olan CSAS tan?l? 258 hastan?n 128'ine medikal tedaviyle birlikte CPAP tedavisi uygulan?rken, 130 olguya yaln?zca medikal tedavi verilerek kontrol grubu olu?turulmu?tur (31). ?? ay sonra; CPAP grubunda AH? ve plazma NE d?zeylerinde azalma, EF, ortalama-minimum oksijen sat?rasyonu ve 6 dakika y?r?me mesafesinde anlaml? art?? izlenirken, uyku s?resi, uyku mimarisi, arousal s?kl??? ve serum ANP d?zeyleri a??s?ndan gruplar aras?nda fark g?r?lmemi?tir. AH?, EF ve oksijen sat?rasyonundaki de?i?imlerle ilgili olumlu etkiler iki y?l boyunca devam etmi?tir. CPAP'?n s?rvi ?zerine etkisinin ara?t?r?ld??? bu ?al??mada; transplants?z survi, hospitalizasyon oran?, mortalite ve ya?am kalitesi a??s?ndan gruplar aras?nda fark izlenmemesi ?zerine, ?al??ma ikinci y?l?n sonunda durdurulmu?tur. Randomize kontroll? bir ba?ka ?al??mada; KKY'li, EF< %45, NYHA II-III olan, optimal medikal tedavi alan 66 olgunun (29 CSS-CSAS, 37 CSAS) median 2.2 y?ll?k takibi sonras?; CPAP kullananlarda mortalite ve kardiyak transplantasyon a??s?ndan r?latif riskin %60 azald??? g?r?lm??t?r (%95 CI, %2-84, p= 0.047) (32). ?al??man?n altgrup analizlerinde, transplants?z sa?kal?m oran?n?n, CSS-CSAS'l?larda, CSS olmayanlara g?re anlaml? oranda d???k oldu?u, ancak bu grupta CPAP kullananlarda, kullanmayanlara g?re sa?kal?m?n belirgin artt??? tespit edilmi?tir. (kardiyak olay g?r?lme oran? CPAP kullananlarda %25, kullanmayanlarda %56, r?latif riskte azalma %81 (%95 CI, %26-95, p= 0.0167). CPAP'?n EF ?zerine etkinli?inin de?erlendirildi?i bir meta-analizde (7 ?al??ma) ise, CPAP kullananlarda kontrol grubuna g?re EF'da ortalama %6 (%95 CI, %2.4-10.5) art?? tespit edilmi?tir (6). CPAP tedavisinin AH? ?zerine etkisinin de?erlendirildi?i bir di?er metaanalizde (5 ?al??ma), AH?'de azalma kontrol grubuna g?re 21 (%95 CI, 17-25), bazal de?ere g?re 30 (%95 CI, 23-37) tespit edilmi?tir (6). Sonu?ta; KKY ili?kili CSAS'da, AH?'yi hedeflenen normal seviyelere getirmede ba?lang?? tedavisi olarak CPAP endikedir (6).
BPAP: BPAP, CSAS-CSS tedavisinde CPAP ile benzer etkinli?e sahiptir. CPAP tedavisini tolere edemeyen, y?ksek bas?n? (> 12 cmH2O) ihtiyac? olan, e?lik eden hipoventilasyonu olanlarda tercih edilir. BPAP'?n desteksiz solunum h?z ayar?yla kullan?lmas?, hiperventilasyona yol a?arak hipokapni geli?imine ve santral apnelerde k?t?le?meye neden olabilir (27). Literat?rde BPAP-S ile yap?lan s?n?rl? ?al??ma mevcuttur. AH?> 20 olan, dilate kardiyomyopatili 21 olguda; standart medikal tedavi (n= 11) ile BPAP-S + medikal tedavi (n= 10) gruplar? kar??la?t?r?lm??t?r (33). Bir gece BPAP-S kullan?m? sonras? AH?, AR?, idrar NE d?zeyleri anlaml? azalm??; 3 ay sonra BPAP-S grubunda; LVEF'de artma, LV sistol sonu internal ?ap, kalp h?z?, sistolik-diyastolik KB, BNP d?zeyinde azalma izlenirken, yaln?zca medikal tedavi alan grupta bu parametrelerin hi?birinde de?i?iklik izlenmemi?tir. Takiplerde (31 ? 2.3 ay), BPAP-S grubunda ?l?m izlenmezken, medikal tedavi grubunda 7 (%63.6) olguda ?l?m g?r?lm??t?r. BPAP-ST KKY ili?kili CSAS'l? olgularda gerek LVEF, gerek AH?'de belirgin d?zelme sa?lamakta, CPAP'a yan?t al?namayan olgularda bu parametreleri d?zeltmektedir (34,35,36). AASM, KKY ile ili?kili CSAS tedavisinde, CPAP, ASV ve oksijen tedavisi ile yeterli yan?t al?namad??? durumlarda BPAP-ST ile tedavinin d???n?lebilece?i belirtmektedir (6).
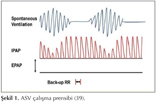
Adaptive servo ventilasyon (ASV): KKY'li ve CSS olan olgularda ASV'nin etkin oldu?u ilk kez 2001'de Teschler ve arkada?lar? taraf?ndan bildirilmi?tir (37). ASV, dakika ventilasyon hedefli (VPAP Adapt SV) veya tidal vol?m hedefli (BIPAP autoSV) algoritmalarla ?al??an bir cihazd?r. Dakika ventilasyon hedefli algoritmada, cihaz hastan?n son ?? dakikal?k dakika ventilasyonunu haf?zas?nda tutarak, bunun %90'?n? vermeyi hedefler. Tidal vol?m hedefli algoritmada ise; inspiryumda verilen bas?n? (?PAP) de?i?kendir. Hastan?n son iki-?? solunumundaki tidal vol?m de?i?imini alg?layarak, buna g?re ?PAP'? ayarlar. Hastan?n tidal vol?m? artt???nda cihaz ?PAP'? azalt?r, tidal vol?m azald???nda ise ?PAP'? art?r?r. B?ylece tidal vol?m dalgalanmalar? ASV ile stabilize edilir (38). Ayarlanan EPAP de?eri ile yetmezlikli kalpte olumlu hemodinamik etkiler sa?lan?r, santral apneler sonras? hava yolundaki kapanma engellenir. ?PAP de?i?kendir (?PAPmax-min), apne-hipopne olu?unca yeterli ventilasyonu sa?lamak i?in ?PAP artar, hiperventilasyon oldu?unda ise ?PAP deste?i azal?r, b?ylece hipokapni geli?imi engellenmi? olur. Santral apne say?s? artt???nda ?timed back up? moda ge?erek, daha ?nceden belirlenen solunum say?s? ve inspiryum s?resi kadar destek olur. ?ekil 1'de ASV cihaz?n?n ?al??ma prensibi g?sterilmi?tir.
ASV cihaz?; CSAS veya CSS olan, CPAP ve BPAP titrasyonunun ba?ar?s?z oldu?u, hastan?n tedaviye uyumunun sa?lanamad??? durumlarda veya ilk gece PSG tetkikinde ?n planda santral apne veya CSS'nin g?r?ld??? ya da EF< %40 olan KKY'li hastalarda CPAP-BPAP uygulanmaks?z?n kullan?labilir.
ASV'nin KKY'de akut etkisinin de?erlendirildi?i bir ?al??mada, (NYHA Class II-IV, EF< %50 olan 30 hasta), ASV uygulamas?ndan 30 dakika sonra yap?lan EKO'da; kalp h?z? ve kan bas?nc?n?n azald???, kardiyak outputun artt??? g?sterilmi?tir (p< 0.0001) (40). NYHA Class II-III olan 9 hastada bir gecelik ASV kullan?m? sonras?, plazma epinefrin, norepinefrin ve serum NT-proBNP d?zeylerinin azald???, AKG analizinde oksijen sat?rasyonu ve pO2'nin artt??? tespit edilmi?tir (41). ASV'nin uzun s?reli kullan?m etkilerinin de?erlendirildi?i ?al??malarda; ASV kullanan olgularda, kullanmayanlara g?re AH?, AR?, A?'nin normale d?nd???, oksijen sat?rasyonunun d?zeldi?i, NYHA skoru, EF, BNP d?zeyi, maksimal oksijen t?ketimi, 6 dakika y?r?me mesafesinde anlaml? iyile?me oldu?u tespit edilmi?tir (42,43,44,45,46,47). ASV'nin ya?am? tehdit edici aritmilerde de d?zelme sa?lad??? g?sterilmi?tir (48). ASV'nin CPAP ile kar??la?t?r?ld??? ?al??malarda AH? ve EF'de her iki tedavi grubunda d?zelme olmakla beraber, ASV kullananlarda iyile?menin daha fazla oldu?u g?r?lm??t?r (49,50). ASV'nin BPAP-ST ile kar??la?t?r?ld??? bir ?al??mada AH? ve oksijenasyon a??s?ndan gruplar aras?nda fark izlenmemi?tir (51).
Antisiklik modulated ventilasyon (ACMV, AMV, trilevel ASV) farkl? bir ASV modelidir. Klasik ASV'de oldu?u gibi ?PAPmax-min parametrelerine ilave olarak, bir EPAP de?eri yerine EPAPmax-min olarak iki ayr? bas?n? de?eri belirlenmektedir (?ekil 2). Farkl? bir tan?mlamayla ASV + APAP kombinasyonu ?eklinde tasarlanan AMV'nin, OSAS ve CSS birlikteli?i, santral-mix apne birlikteli?i olan olgularda kullan?m? ?nerilmektedir.
KKY tan?l?, AH? ≥ 15 olan PSG'de solunumsal olaylar?n b?y?k k?sm?n?n santral ve mix apnelerden olu?tu?u (obstr?ktif apne say?s? < %20) 45 hastada 3 ay AMV kullan?m? sonras?; AH?'de azalma, ortalama O2 sat?rasyonu, NYHA s?n?f?nda d?zelme, kardiyopulmoner egzersiz testinde maksimal O2 t?ketiminde ve g?nd?z pCO2 de?erlerinde anlaml? art?? tespit edilmi?tir (52). Farkl? bir ?al??mada; obstr?ktif-santral apneleri-CSS olan, e?lik eden HT, KAH, MY ?yk?s? bulunan 12 hastan?n 7'sinde, iki haftal?k AMV tedavisi sonras? total AH?, obstr?ktif AH?, santral AH?'de d?zelme (p< 0.01), AR?, oksijen sat?rasyonu ve uyku profilinde iyile?me tespit edilmi?tir (53).
Frenik Sinir Stim?lasyonu
Yeni geli?tirilmi? bir tedavi modalitesidir. ?lk kullan?m yeri; spinal kord hasar?na ba?l? solunum paralizisi geli?en ve konjenital santral alveoler hipoventilasyonu olan (Ondine's Curse) olgulard?r. Sa? frenik sinirin sa? brakiosefalik venle, sol frenik sinirin sol brakiosefalik/perikardiyofrenik venle kom?ulu?undan yola ??karak, pacemakera benzer bir cihaz yard?m?yla sinirin stim?lasyonu sa?lanmaktad?r. Aksiller veya subklavyen venden girilerek (transven?z yol), eksternal pulse jenerat?r sistemi kullan?larak stim?lasyon ger?ekle?tirilmektedir. Bir veya iki gecelik uygulamayla, santral apnelerin elimine edilmesi i?in gereken frenik sinir stim?lasyon miktar? titre edilir (54). Frenik sinir stim?lasyonu ile apne olu?umu engellenerek solunum stabilize edilir, intratorasik bas?n? subatmosferik d?zeyde kal?r (55). CSAS tan?l? 16 hastada yap?lan bir ?al??mada, frenik sinir stim?lasyonu ile AH?, santral AH?, OD?'de anlaml? d?zelme ve dola??m gecikme zaman?nda iyile?me g?r?l?rken, uyku etkinli?i ve uyku kalitesi ?zerine herhangi bir etki izlenmemi?tir (56).
Kardiyak m?dahaleler
Bu grupta yer alan m?dahaleler kardiyak resenkronizasyon tedavisi (KRT), atrial overdrive pacing (AOP), kardiyak transplantasyon olarak ?? ba?l?kta toplanabilir.
a) Kardiyak resenkronizasyon tedavisi (KRT): Vent-rik?ler dissenkroni, KKY'li hastalarda kardiyak pompa fonksiyonunu bozan bir durumdur. KRT, dal blo?u olan olgularda pace arac?l???yla bir veya her iki ventrik?l?n stim?lasyonu ile pompa fonksiyonlar?n? d?zeltir. CSAS'l? olgularda KRT ile hem EF'de hem de AH?'de belirgin d?zelmeler oldu?u g?sterilmi?tir (57,58,59,60).
b) Atrial overdrive pacing (AOP): Atriyuma yerle?tirilen pace ile kalp h?z?n?n bazale g?re 15-10 art?r?lmas? sa?lan?r. Bu y?ntem, kardiyak outputu art?rarak, pulmoner ven?z konjesyonu azaltarak, dola??m zaman?n? k?saltarak CSAS'da etkin olabilmektedir (61).
c) Kardiyak transplantasyon: Prospektif, nonrandomize-kontroll? bir ?al??mada; 22 olguda (13 CSAS + KKY, 9 KKY) transplantasyondan ortalama 13 ay sonra; CSAS'l? olgularda AH?'nin 28 ? 15 & 7 ? 6'ya geriledi?i, 6 olguda AH?< 5 oldu?u, 3 olguda CSAS'?n devam etti?i, 4 olguda OSAS geli?ti?i tespit edilirken, t?m olgularda EF ve ?riner NE ekskresyonunun anlaml? d?zeldi?i g?r?lm??t?r (62).
KKY'li olgularda, farmakolojik tedavi optimize edildikten sonra, nonfarmakolojik yakla??mlar CSAS'?n d?zelmesini sa?layabilir. Bu yakla??mlar ile CSAS'da d?zelmeler bildirilmesine ra?men; spesifik beceri gerektirmeleri, ?nemli morbiditeye sahip olmalar?, maliyetin y?ksek olmas? ve her yerde kolay uygulanamamas? nedeniyle kardiyoloji literat?r?nde endikasyonlar? s?n?rl?d?r (6).
Y?ksek ?rtifa Periyodik Solunumuna Ba?l? CSAS Tedavisi
Y?ksek irtifada hipoksinin ind?kledi?i hiperventilasyon hipokapniye, bu da periyodik solunum paterninin geli?mesine yol a?ar. Y?ksek irtifa denilebilmesi i?in en az 4000 metre y?ksekli?e ??k?lm?? olmas? gerekmektedir. Y?ksek irtifaya ba?l? periyodik solunumunun tedavisinde genelde farmakolojik ajanlar?n etkinli?i ara?t?r?lm??t?r. ?svi?re'de y?ksek irtifa ara?t?rma istasyonunda 3454 metre y?kseklikte, 30 kat?l?mc?yla ger?ekle?tirilen bir ?al??mada; Teofilin (2 x 250 mg) - ACET (2 x 250 mg) plasebo ile kar??la?t?r?lm??; ard???k 2 g?n?n sonunda yap?lan polisomnografi incelemesinde; Teofilin-ACET kullan?m? ile AH?'nin normale d?nd???, ACET alanlarda oksijen sat?rasyonunda anlaml? d?zelme oldu?u tespit edilmi?tir. ACET alanlar?n %60'?nda parestezi, teofilin alanlar?n %70'inde ?arp?nt?, hemen t?m olgularda artm?? di?rez izlenmi?tir (63). Bir benzodiazepin olan Temazepam (10 mg)'?n plasebo ile kar??la?t?r?ld???, 33 kat?l?mc?yla ger?ekle?tirilen farkl? bir ?al??mada, 410 metrede iken t?rmanmaya ba?lay?p, 17. g?n?n sonunda 5000 metreye ula?an olgulardan Temazepam alanlarda periyodik solunum oran?nda anlaml? azalma izlenirken (p= 0.016), oksijen sat?rasyonunun da d??t??? g?r?lm??t?r (p= 0.013). ?laca ba?l? yan etki (ertesi g?n reaksiyonlarda yava?lama, uyan?kl???n s?rd?r?lmesi, kognitif fonksiyonlarda de?i?im?) izlenmemi?tir (64). Hipnotik ajanlardan Zolpidem-zaleplon'un plasebo ile kar??la?t?r?ld??? bir ba?ka ?al??ma ise; 12 kat?l?mc? ile, 1 gece deniz seviyesinde 3 gece 4000 metre y?kseklikte ger?ekle?tirilmi?tir. Her iki ajanla da AH? ve oksijen sat?rasyonunda anlaml? de?i?im olmazken, yava? dalga uykusunda art?? izlenmi?, ila?lara ba?l? yan etki g?zlenmemi?tir (65). G?n?m?zde, kan?t d?zeylerinin ?ok d???k olmas?, y?ksek irtifaya ba?l? CSAS tedavisinde farmakolojik ajanlar?n kullan?m?na ili?kin bir ?neri olu?turmay? engellemektedir. Hastal???n do?as? gere?i bu ila?lar yaln?zca k?sa bir s?re i?in kullan?lmal?d?r (6).
Cheyne-Stokes D??? Medikal Durumlara Ba?l? CSAS Tedavisi
Bu gurupta en s?k g?r?len patolojiler santral sinir sistemi lezyonlar? (vask?ler, neoplastik, dejeneratif, travmatik, demiyelinizan vs.) ve son d?nem b?brek hastal???d?r (SDBH). CSAS'da ?ncelikli olan altta yatan primer hastal???n etkin tedavisidir. SDBH'da oksijen tedavisinin etkinli?inin ara?t?r?ld??? bir ?al??mada, 11 periton diyaliz hastas?nda; gece boyu ortalama O2 sat?rasyonu ve minimum O2 sat?rasyonunun anlaml? artt???, santral apne ve hipopnelerin belirgin azald??? g?r?lm??t?r (66). KBY'li 6 hastada CPAP etkisinin ara?t?r?ld??? bir di?er ?al??mada; bir gece CPAP kullan?m? sonunda AH? ve oksijen sat?rasyonunda belirgin d?zelme izlenmi?tir (67). Sonu?ta; SDBH'na ba?l? CSAS tedavisinde; CPAP, oksijen tedavisi, diyaliz s?resince uygulanacak bikarbonat tamponu ve nokt?rnal diyaliz yakla??m? tedavi se?enekleri olarak d???n?lebilir (6).
?la? veya Madde Kullan?m?na Ba?l? CSAS Tedavisi
Bu grupta yer alan ajanlar?n prototipi opioidlerdir. Kronik opioid kullan?m?na (120-420 mg/g?n) ba?l? CSAS geli?en ve CPAP'a yan?t al?namayan 4 olguda BPAP ile AH?'nin 60'tan 16.6'ya geriledi?i, 3 olguda santral apnelerin tamamiyle elimine oldu?u, Epworth uykululuk skorunun geriledi?i, hipoksemi ve uyku fragmantasyonunun azald??? tespit edilmi?tir (68). Farkl? bir ?al??mada 5 hastada ASV ile CPAP etkinli?i kar??la?t?r?lm??; bazal AH?: 70 ? 19, CPAP ile 55 ? 25, ASV ile 20 ? 18'e gerilemi?, santral apneler CPAP ile artarken, ASV ile tamamen elimine edilmi?tir (69). CPAP ve ASV'nin santral apneler ?zerine hi? etkisi olmad??? y?n?nde bulgular da mevcuttur, bu sonu? titrasyon metoduyla ili?kilendirilmi?tir (70). G?n?m?zde; opioid kullan?m?na ba?l? CSAS tedavisinde kan?tlar?n yetersizli?i bir ?neri olu?umunu engellemektedir. CPAP'?n BPAP ve ASV'den daha az etkili olup olmad???n? de?erlendirecek ileri ?al??malara ihtiya? vard?r (6).
??kar ?at??mas?
Bildirilmemi?tir.
KAYNAKLAR
- Momomura S. Treatment of Cheyne-Stokes respiration-central sleep apnea in patients with heart failure. J Cardiology 2012;59:110-6.
- Eckert DJ, Jordan AS, Merchia P, Malhotr A. Central sleep apnea. Pathophysiology and treatment. Chest 2007;131:595-607.
- Silva CP, Filho GL, Marcondes B, Junior GO, Mangini S. Reduction of central sleep apnea in heart failure patients with beta-blockers therapy. Arq Bras Cardiol 2010;94:223-9.
- American Academy of Sleep Medicine: International classification of sleep disorders. Diagnostic and coding manual, 2nd ed. Westchester, Illinois: American Academy of Sleep Medicine 2005.
- Xie A, Rankin F, Rutherford R, Bradley T. Effects of inhaled CO2 and added dead space on idiopathic central sleep apnea. J Appl Physiol 1997;82:918-26.
- Aurora RN, Chowdhuri S, Ramar K, Bista SR, Casey KR, Lamm CI, et al. The treatment of central sleep apnea syndromes in adults: practice parameters with an evidence-based literature review and meta-analyses. Sleep 2012;35:17-40.
- DeBacker W, Verbraecken J, Willemen M, Wittesaele W, DeCock W, et al. Central apnea index decreases after prolonged treatment with acetazolamide. Am J Respir Crit Care Med 1995;151:87-91.
- White D, Zwillich C, Pickett C, Douglas N, Findley L, Weil J. Central sleep apnea: improvement with acetazolamide therapy. Arch Intern Med 1982;142:1816-9.
- Quadri S, Drake C, Hudgel DW. Improvement of idiopathic central sleep apnea with zolpidem. J Clin Sleep Med 2009;5:122-9.
- Bonnet M, Dexter J, Arand D. The effect of triazolam on arousal and respiration in central sleep apnea patients. Sleep 1990;13:31-41.
- Lanfranchi PA, Braghiroli A, Bosimini E, Mazzuero G, Colombo R, Donner CF, et al. Prognostic value of nocturnal Cheyne-Stokes respiration in chronic heart failure. Circulation 1999;99:1435-40.
- Tamura A, Kawano Y, Kadota J. Carvedilol reduces the severity of central sleep apnea in chronic heart failure. Circ J 2009;73:295-8.
- Walsh J, Andrews R, Starling R, Cowley A, Johnston I, Kinnear W. Effects of captopril and oxygen on sleep apnoea in patients with mild to moderate congestive cardiac failure. Br Heart J 1995;73:237-41.
- Zilberman M, Silverberg D, Bits I, Steinbruch S, Wexler D, Sheps D, et al. Improvement of anemia with erythropoietin and intravenous iron reduces sleep-related breathing disorders and improves daytime sleepiness in anemic patients with congestive heart failure. Am Heart J 2007;154:870-6.
- Chowdhuri S, Shanidze I, Pierchala L, Belen D, Mateika J, Badr M. Effect of episodic hypoxia on the susceptibility to hypocapnic central apnea during NREM sleep. J Appl Physiol 2010;108:368-77.
- Xie A, Skatrud J, Puleo D, Dempsey J. Influence of arterial O2 on the susceptibility to posthyperventilation apnea during sleep. J Appl Physiol 2006;100:171-7.
- Sasayama S, Izumi T, Seino Y, Ueshima K, Asanoi H. Effects of nocturnal oxygen therapy on outcome measures in patients with chronic heart failure and cheyne-stokes respiration. Circ J 2006;70:1-7.
- Toyama T, Seki R, Kasama S, Isobe N, Sakurai S, Adachi H, et al. Effectiveness of nocturnal home oxygen therapy to improve exercise capacity, cardiac function and cardiac sympathetic nerve activiy in patients with chronic heart failure and central sleep apnea. Circ J 2009;73:299-304.
- Shigemitsu M, Nishio K, Kusuyama T, Itoh S, Konno N, Katagiri T. Nocturnal oxygen therapy prevents progress of congestive heart failure with central sleep apnea. Int J Cardiol 2007;115:354-60.
- Brostrom A, Hubbert L, Jakobsson P, Johansson P, Fridlund B, Dahlstrum U. Effects of long-term nocturnal oxygen treatment in patients with severe heart failure. J Cardiovasc Nurs 2005;20:385-96.
- Andreas S, Clemens C, Sandholzer H, Figulla H, Kreuzer H. Improvement of exercise capacity with treatment of Cheyne-Stokes respiration in patients with congestive heart failure. J Am Coll Cardiol 1996;27:1486-90.
- Steens R, Millar T, Xiaoling S, Biberdorf D, Buckle P, Ahmed M, et al. Effect of inhaled 3% CO2 on Cheyne-Stokes respiration in congestive heart failure. Sleep 1994;17:61-8.
- Javaheri S, Parker T, Wexler L, Liming J, Lindower P, Roselle G. Effect of theophylline on sleep-disordered breathing in heart failure. N Engl J Med 1996;335:562-7.
- Hu K, Li Q, Yang J, Hu S, Chen X. The effect of theophylline on sleepdisordered breathing in patients with stable chronic congestive heart failure. Chin Med J 2003;116:1711-6.
- Javaheri S. Acetazolamide improves central sleep apnea in heart failure: a double-blind, prospective study. Am J Respir Crit Care Med 2006;173:234-7.
- Hunt SA, Abraham WT, Chin MH, Feldman AM, Francis GS, Ganiats TG, et al. ACC/AHA 2005 guideline update for the diagnosis and management of chronic heart failure in the adult: a report of the American College of Cardiology/American Heart Association Task Force on Practice Guidelines (Writing Committee to Update the 2001 Guidelines for the Evaluation and Management of Heart Failure) Circulation 2005;112:e154-235.
- Johnson KG, Johnson DC. Bilevel positive airway pressure worsens central apneas during sleep. Chest 2005;128:2141-50.
- Dursuno?lu D, Dursuno?lu N. Kalp yetersizli?i hastalar?nda noninvaziv mekanik ventilasyon tedavisi. Anadolu Kardiyoloji Dergisi 2012;12:261-8.
- Javaheri S. Effects of continuous positive airway pressure on sleep apnea and ventricular irritability in patients with heart failure. Circulation 2000;101:392-7.
- Buckle P, Millar T, Kryger M. The effects of short-term nasal CPAP on Cheyne-Stokes respiration in congestive heart failure. Chest 1992;102:31-5.
- Bradley T, Logan A, Kimoff RJ, Series F, Morrison D, Ferguson K, et al. Continuous positive airway pressure for central sleep apnea and heart failure. N Engl J Med 2005;353:2025-33.
- Sin DD, Logan AG, Fitzgerald FS, Liu PP, Bradley TD. Effects of continuous positive airway pressure on cardiovascular outcomes in heart failure patients with and without Cheyne-Stokes respiration. Circulation 2000;102:61-6.
- Noda A, Izawa H, Asano H, Nakata S, Hirashiki A, Murase Y, et al. Beneficial effect of bilevel positive airway pressure on left ventricular function in ambulatory patients with idiopathic dilated cardiomyopathy and central sleep apnea-hypopnea: a preliminary study. Chest 2007;131:1694-701.
- Dohi T, Kasai T, Narui K, Ishiwata S, Ohno M, Yamaguchi T, et al. Bi-level positive airway pressure ventilation for treating heart failure with central sleep apnea that is unresponsive to continuous postitive airway pressure. Circ J 2008;72:1100-5.
- Kasai T, Narui K, Dohi T, Ishiwata S, Yoshimura K, Nishiyama S, et al. Efficacy of nasal bi-level positive airway pressure in congestive heart failure patients with Cheyne-Stokes respiration and central sleep apnea. Circ J 2005;69:913-21.
- Willson G, Wilcox I, Piper A, Flynn WE, Norman M, Grunstein RR, et al. Noninvasive pressure preset ventilation for the treatment of Cheyne-Stokes respiration during sleep. Eur Respir J 2001;17:1250-7.
- Teschler H, D?hring J, Wang YM, Berthon-Jones M. Adaptive pressure support servo-ventilation: a novel treatment for Cheyne-Stokes respiration in heart failure. Am J Respir Crit Care Med 2001;164:614-9.
- www.resmed.com Accessed date:19 November 2013.
- Oldenburg O. Cheyne-Stokes respiration in chronic heart failure-Treatment with adaptive servoventilation therapy. Circ J 2012;76:2305-17.
- Haruki N, Takeuchi M, Kaku K, Yoshitani H, Kuwaki H, Tamura M, et al. Comparison of acute and chronic impact of adaptive servo-ventilation on left chamber geometry and function in patients with chronic heart failure. Eur J Heart Fail 2011;13:1140-6.
- Gur S, Dursuno?lu D, Dursuno?lu N, K?l?c M. Acute effects of adaptive servo-ventilation therapy on neurohormones and Cheyne-Stokes respiration in the patients with heart failure. Anadolu Kardiyol Derg 2009;9:206-14.
- Oldenburg O, Bitter T, Lehmann R, Korte S, Dimitriadis Z, Faber L, et al. Adaptive servoventilation improves cardiac function and respiratory stability. Clin Res Cardiol 2011;100:107-15.
- Haruki N, Takeuchi M, Kaku K, Yoshitani H, Kuwaki H, Tamura M, et al. Comparison of acute and chronic impact of adaptive servoventilation on left chamber geometry and function in patients with chronic heart failure. Eur J Heart Fail 2011;13:1140-6.
- Hastings P, Vazir A, Meadows G, Dayer M, Poole-Wilson P, McIntyre H, et al. Adaptive servo-ventilation in heart failure patients with sleep apnea: a real world study. Int J Cardiol 2010;139:17-24.
- Koyama T, Watanabe H, Kobukai Y, Makabe S, Munehisa Y, Kosaka T, et al. Beneficial effects of adaptive servo ventilation in patients with chronic heart failure. Circ J 2010;74:2118-24.
- Hetland A, Haugaa K, Olseng M, Gjesdal O, Ross S, Saberniak J, et al. Three months treatment with adaptive servo-ventilation improves cardiac function and physical activity in patients with chronic heart failure and Cheyne-Stokes respiration in a prospective randomized controlled trial. Cardiology 2013;126:81-90.
- Miyata M, Yoshihisa A, Suzuki S, Yamada S, Kamioka M, Kamiyama Y, et al. Adaptive servo ventilation improves Cheyne-Stokes respiration, cardiac function, and prognosis in chronic heart failure patients with cardiac resynchronization therapy. J Cardiol 2012;60:222-7.
- Bitter T, Westerheide N, Langer C, Prinz C, Horstkotte D, Oldenburg O. Cheyne-Stokes respiration in patients with congestive heart failure: association with malignant arrhythmic events and effects of adaptive servoventilation therpy-an observational study. Circulation 2010;122(Suppl 1):Abstract 16707.
- Philippe C, Stoica-Herman M, Drouot X, Raffestin B, Escourrou P, Hittinger L, et al. Compliance with and efficacy of adaptive servoventilation (ASV) versus continuous positive airway pressure (CPAP) in the treatment of Cheyne-Stokes respiration in heart failure over a six month period. Heart 2006;92:337-42.
- Albert NM, Boehmer JP, MD, Collins SP, Ezekowitz JA, Givertz MM, Katz SD, et al. Heart Failure Society of America (HFSA) 2010 Comprehensive Heart Failure Practice Guideline. J Card Fail 2010;16:e1-e2.
- Fietze I, Blau A, Glos M, Theres H, Baumann G, Penzel T. Bi-level positive pressure ventilation and adaptive servo ventilation in patients with heart failure and Cheyne-Stokes respiration. Sleep Med 2008;9:652-59.
- Oldenburg O, Bitter T, Wellmann B, Fischbach T, Efken C, Schmidt A, et al. Trilevel adaptive servoventilation for the treatment of central and mixed sleep apnea in chronic heart failure patients. Sleep Medicine 2013;14:422-27.
- Randerath WJ, Galetke W, Kenter M, Richter K, Sch?fer T. Combined adaptive servo-ventilation and automatic positive airway pressure (anticyclic modulated ventilation) in co-existing obstructive and central sleep apnea syndrome and periodic breathing. Sleep Med 2009;10:898-903.
- Augostini R. A novel approach to the treatment of central sleep apnea in patients with heart failure. Herzschr Elektrophysiol 2012;23:9-13.
- Floras JS. Transvenous phrenic nerve stimulation for central sleep apnoea in heart failure: chicken or egg? Eur Heart 2012;33:810-12.
- Ponikowski P, Javaheri S, Michalkiewicz D, Bart B, Czarnecka D, Jastrzebski M, et al. Transvenous phrenic nerve stimulation for the treatment of central sleep apnoea in heart failure. Eur Heart J 2012;33:889-94.
- Yiu K, Lee K, Lau C, Siu CW, Miu KM, Lam B, et al. Alleviation of pulmonary hypertension by cardiac resynchronization therapy is associated with improvement in central sleep apnea. Pacing Clin Electrophysiol 2008;31:1522-7.
- Sinha AM, Skobel E, Breithardt OA, Norra C, Markus KU, Breuer C, et al. Cardiac resynchronization therapy improves central sleep apnea and Cheyne-Stokes respiration in patients with chronic heart failure. J Am Coll Cardiol 2004;44:68-71.
- Gabor J, Newman D, Barnard-Roberts V, Korley V, Mangat I, Dorian P, et al. Improvement in Cheyne-Stokes respiration following cardiac resynchronization therapy. Eur Respir J 2005;26:95-100.
- Skobel EC, Sinha AM, Norra C, Randerath W, Breidhardt OA, Breuer C, et al. Effect of cardiac resynchronization therapy on sleep quality, quality of life, and symptomatic depression in patients with chronic heart failure and Cheyne, Stokes respiration. Sleep Breath 2005;9:159-66.
- Luthje L, Renner B, Kessels R, Vollmann D, Raupach T, Gerritse B, et al. Cardiac resynchronization therapy and atrial overdrive pacing for the treatment of central sleep apnoea. EurJ Heart Fail 2009;11:273-80.
- Mansfield D, Solin P, Roebuck T, Bergin P, Kaye D, Naughton M. The effect of successful heart transplant treatment of heart failure on central sleep apnea. Chest 2003;124:1675-81.
- Fischer R, Lang S, Leitl M, Thiere M, Steiner U, Huber R. Theophylline and acetazolamide reduce sleep-disordered breathing at high altitude. Eur Respir J 2004;23:47-52.
- Nickol A, Leverment J, Richards P, Seal P, Harris GA, Cleland J, et al. Temazepam at high altitude reduces periodic breathing without impairing next-day performance: a randomized cross-over double-blind study. J Sleep Res 2006;15:445-54.
- Beaumont M, Batejat D, Coste O, Van Beers P, Colas A, Cl?re JM, et al. Effects of Zolpidem and Zaleplon on sleep, respiratory patterns and performance at a simulated altitude of 4000 m. Neuropsychobiology 2004;49:154-62.
- Kumagai T, Ishibashi Y, Kawarazaki H, Kawarazaki W, Shimizu H, Kaname S, et al. Effects of nocturnal oxygen therapy on sleep apnea syndrome in peritoneal dialysis patients. Clin Nephrol 2008;70:332-9.
- Pressman M, Benz R, Schleifer C, Peterson D. Sleep disordered breathing in ESRD: acute beneficial effects of treatment with nasal continuous positive airway pressure. Kidney Int 1993;43:1134-9.
- Alattar M, Scharf S. Opioid-associated central sleep apnea: a case series. Sleep Breath 2009;13:201-6.
- Javaheri S, Malik A, Smith J, Chung E. Adaptive pressure support servoventilation: a novel treatment for sleep apnea associated with use of opioids. J Clin Sleep Med 2008;4:305-10.
- Farney R, Walker J, Boyle K, Cloward T, Shilling K. Adaptive servoventilation (asv) in patients with sleep disordered breathing associated with chronic opioid medications for non-malignant pain. J Clin Sleep Med 2008;4:311-9.
Yaz??ma Adresi (Address for Correspondence)
Dr. Handan ?N?N? K?SEO?LU
Gaziosmanpa?a ?niversitesi T?p Fak?ltesi,
G???s Hastal?klar? Anabilim Dal?,
TOKAT - TURKEY
e-mail: handaninonu@gmail.com