SHORT REPORT
Doi: 10.5578/tt.7154
Tuberk Toraks 2014;62(1):51-67

A??r Ast?m Tedavisi: Uzman G?r???
Haluk T?RKTA?1, Sevim BAVBEK2, G?lfem ?EL?K2, Tun?alp DEM?R3, Bilun GEM?C?O?LU3, Hakan G?NEN4,
Esen KIYAN5, Dil?ad MUNGAN2, ?pek K?v?lc?m O?UZ?LGEN1, Mehmet POLATLI6, Sevgi SARYAL7,
Abdullah SAYINER8, Elif ?EN7, Nurhayat YILDIRIM3, F?sun YILDIZ9, Arzu YORGANCIO?LU10
1 Gazi ?niversitesi T?p Fak?ltesi, G???s Hastal?klar? Anabilim Dal?, Ankara, T?rkiye
1 Department of Chest Diseases, Faculty of Medicine, Gazi University, Ankara, Turkey
2 Ankara ?niversitesi T?p Fak?ltesi, G???s Hastal?klar? Anabilim Dal?, ?mm?noloji Allerji Bilim Dal?, Ankara, T?rkiye
2 Division of Immunology Allergy, Department of Chest Diseases, Faculty of Medicine, Ankara University, Ankara, Turkey
3 ?stanbul ?niversitesi Cerrahpa?a T?p Fak?ltesi, G???s Hastal?klar? Anabilim Dal?, ?stanbul, T?rkiye
3 Department of Chest Diseases, Faculty of Cerrahpasa Medicine, Istanbul University, Istanbul, Turkey
4 Sa?l?k Bakanl??? S?reyyapa?a E?itim ve Ara?t?rma Hastanesi, G???s Hastal?klar? Klini?i, ?stanbul, T?rkiye
4 Clinic of Chest Diseases, Ministry of Health Sureyyapasa Training and Research Hospital, Istanbul, Turkey
5 ?stanbul ?niversitesi ?stanbul T?p Fak?ltesi, G???s Hastal?klar? Anabilim Dal?, ?stanbul, T?rkiye
5 Department of Chest Diseases, Faculty of Istanbul Medicine, Istanbul University, Istanbul, Turkey
6 Adnan Menderes ?niversitesi T?p Fak?ltesi, G???s Hastal?klar? Anabilim Dal?, Ayd?n, T?rkiye
6 Department of Chest Diseases, Faculty of Medicine, Adnan Menderes University, Aydin, Turkey
7 Ankara ?niversitesi T?p Fak?ltesi, G???s Hastal?klar? Anabilim Dal?, Ankara, T?rkiye
7 Department of Chest Diseases, Faculty of Medicine, Ankara University, Ankara, Turkey
8 Ege ?niversitesi T?p Fak?ltesi, G???s Hastal?klar? Anabilim Dal?, ?zmir, T?rkiye
8 Department of Chest Diseases, Faculty of Medicine, Ege University, Izmir, Turkey
9 Kocaeli ?niversitesi T?p Fak?ltesi, G???s Hastal?klar? Anabilim Dal?, Kocaeli, T?rkiye
9 Department of Chest Diseases, Faculty of Medicine, Kocaeli University, Kocaeli, Turkey
10 Celal Bayar ?niversitesi T?p Fak?ltesi, G???s Hastal?klar? Anabilim Dal?, Manisa, T?rkiye
10 Department of Chest Diseases, Faculty of Medicine, Celal Bayar University, Manisa, Turkey
?ZET
A??r Ast?m Tedavisi: Uzman G?r???
A??r ast?m t?m ast?ml? hasta pop?lasyonunun yakla??k %10'unu olu?turur. Ast?m kontrol?n?n sorun oldu?u bu grup hastalarda acil servis ba?vurular?, hastane yat??lar?, i?-g?? kay?plar? y?ksek oranlarda g?r?l?r. Dolay?s?yla tedavi maliyetleri ?ok y?ksektir ve t?m ast?m maliyetinin %50'si bu grup i?in harcanmaktad?r. Genellikle y?ksek doz inhaler steroid ve uzun etkili beta-2 agonist kombinasyonu ile kontrol alt?na al?namayan bu grup hastalarda farkl? tedavi se?enekleri denenmektedir. Bu k?sa raporda g?ncel literat?r verileri derlenerek standart tedaviye diren?li a??r ast?ml? hastalarda tedavi se?enekleri ?lkemiz ko?ullar? da g?z ?n?ne al?narak tart???lm?? ve g?nl?k klinik pratik i?in ?nerilerde bulunulmu?tur.
Anahtar kelimeler: A??r ast?m; tedaviye diren?li ast?m; uzman g?r???
SUMMARY
Treatment of Severe Asthma: Expert Opinion
Severe asthmatics account 10% of the all asthmatic population. Those asthmatics whose disease is inadequately controlled account for up to half of the cost for asthma, because they have more emergency room visits, more hospital admission and greater absenteeism from work. New therapeutic options were tried in those patients whose asthma was uncontrolled with standart high dose inhaled corticosteroid and long acting beta-2 agonsit combination therapy. In this paper taking into account the conditions of our country, current literature was reviewed and treatment options was discussed and graded recommendations are made for daily clinical practice in patients with severe treatment-refractory asthma.
Key words: Severe asthma; treatment-refractory; expert opinion
Y?NTEM
Tedaviye diren?li a??r ast?m tedavisi konusunda yap?lm?? bilimsel ?al??malar taranm??, elde edilen yay?nlar eri?kin ast?m? ve kronik obstr?ktif akci?er hastal??? (KOAH) konular?nda uzman olan 16 ki?ilik panelist grup taraf?ndan kan?t kalitesi a??s?ndan de?erlendirilmi? ve GRADE (Grading of Recommendations, Assessment, Development and Evaluation) (1) sistemati?i ?er?evesinde tedavide kullan?lan her bir ila? veya y?ntemin kan?t d?zeyi, etki ve yan etkileri ile maliyeti de g?z ?n?ne al?narak ?lkemiz ko?ullar?nda kullan?l?p kullan?lmayaca?? konusunda oylama yap?lm??t?r. Oylama sonucuna g?re de "pozitif" ya da "negatif" ve "kuvvetli" ya da "zay?f olarak" ?nerilerde bulunulmu?tur (Tablo 1).
Kan?tlar?n Kalitesi
Y?ksek: ?yi planlanm?? ve y?r?t?lm?? randomize klinik ?al??malardan elde edilen sonu?lar.
Orta: Az say?da hasta i?eren, daha d???k kalitede randomize klinik ?al??malardan elde edilen sonu?lar.
D???k: G?zlemsel ?al??malardan (Kohort ve olgu kontrol) elde edilen sonu?lar.
?ok d???k: Olgu serisi, uzman g?r???.
Kan?tlar?n De?erlendirilmesi
Y?ksek: Bundan sonra yap?lacak ?al??malar?n bu konudaki g?r???m?z? de?i?tirme olas?l??? ?ok d???kt?r.
Orta: Bundan sonra yap?lacak ?al??malar?n bu konudaki g?r???m?ze ?nemli etkisi olabilir, hatta g?r???m?z? de?i?tirebilir.
D???k: Bundan sonra yap?lacak ?al??malar?n bu konudaki g?r???m?ze ?nemli etkisi olacakt?r ve g?r???m?z? de?i?tirme olas?l??? ?ok y?ksektir.
?ok d???k: Halen var olan bu konudaki g?r???m?z ?ok yetersizdir, g?r?? olu?turabilmek i?in daha ?ok ?al??maya gereksinim vard?r.
?neriler
Kuvvetli ?neri: Hastalar?n b?y?k ?o?unlu?u ?nerilen y?ntem ya da tedavinin yap?lmas?n? ister, sadece k???k bir az?nl?k istemez. Bu ?neriler sa?l?k politikalar?, geri ?demeler vb. i?in yol g?sterici olur.
Zay?f ?neri: Yeterli derecede bilgilendirilirse bu durumdaki ki?ilerin ?o?unlu?u ?nerilen y?ntem ya da tedavinin yap?lmas?n? ister, ancak bir ?o?u da istemeyebilir. Hastan?n kendi karar?n? verebilmesi i?in ayr?nt?l? bilgi vererek hastaya yard?mc? olmak gerekir. Bu ?nerilerin yol g?sterici olabilmesi i?in daha ?ok tart??ma ve veriye gereksinim duyulur.
Pozitif ?neri: Kuvvetli ya da zay?f olarak s?z konusu tedavi veya i?lemin yap?lmas?n? ?nerir.
Negatif ?neri: Kuvvetli ya da zay?f olarak s?z konusu tedavi veya i?lemin yap?lmamas?n? ?nerir.
A?IR ASTIM
A??r Ast?m Tan?m? (2)
G?n?m?zde "a??r ast?m" y?ksek doz inhaler steroid ile birlikte ikinci bir kontrol edici ila? (Uzun etkili beta-agonist, l?kotrien resept?r antagonisti veya teofilin) ve/veya ?nceki y?la g?re > %50'den fazla kullan?lan oral steroide ra?men kontrol edilemeyen ast?m olarak tan?mlan?r.
Burada y?ksek doz inhaler steroid olarak kastedilen flutikazon propionat > 1000 μg veya buna e?de?er di?er inhaler steroid dozlar?d?r. Kontrol edilemeyen ast?m ise a?a??daki kriterlerden herhangi birinin varl??? olarak kabul edilmektedir:
Yetersiz semptom kontrol?: ACQ > 1.5 veya ACT < 19 (veya NAEPP k?lavuzuna g?re "not well controlled" olmas?.
S?k atak: Bir ?nceki y?l iki veya daha fazla sistemik steroid tedavisi alm?? olmas? (her birinde ?? g?nden fazla).
A??r atak: Bir ?nceki y?l en az bir kez hastane yat???, yo?un bak?m ?nitesine yat?? veya mekanik ventilasyon gereksinimi olmas?.
Persistan hava ak?m? k?s?tlamas?: Prebron-kodilat?r FEV1'in beklenenin %80'in alt?nda olmas?.
Yukar?da tan?m? yap?lan a??r ast?ml? hastalar genellikle iki ba?l?k alt?nda s?n?fland?r?l?rlar; sorunlu ast?m ve tedaviye diren?li ast?m.
A??r ast?m s?n?flamas? (2)
1. Sorunlu ast?m:
Yanl?? tan?,
Hasta uyumsuzlu?u,
Tedavi edilmemi? komorbiditeler,
En az ?? ay bir ast?m uzman? taraf?nda tedavi ve takip edilmemi? olmas?.
2. Tedaviye diren?li ast?m:
Y?ksek doz standart tedaviye ra?men,
Kontrol alt?na al?namam?? veya,
Ancak y?ksek doz tedavi ile kontrol? devam ettirilebilen.
Standart tedaviyle kontrol alt?na al?namayan hastalarda "tedaviye diren?li ast?m" demeden ?nce mutlaka ast?m kontrol?n? g??le?tiren nedenler g?zden ge?irilmelidir. Ast?mda kontrols?zl???n en ?nemli nedeni hastalar?n ila?lar?n? yeterli ve do?ru kullanmamalar?d?r. Hastalar ila? kullan?m? konusunda tekrar tekrar e?itilmeli ve ila?lar?n? do?ru ve d?zenli kullanmalar? sa?lanmal?d?r. Burada ?nemli bir nokta hastan?n ast?m tedavisine yan?t verebilmesi i?in hastal???n?n ast?m olmas? gerekir. Dolay?s?yla tedaviye yan?t vermeyen hastalarda vokal kord disfonksiyonu, bron?iyolit, bron?ektazi, pulmoner konjesyon, endobron?iyal obstr?ksiyonlar, KOAH gibi ast?mla kar??abilen di?er hastal?klar d??lanmal?d?r. Ayr?ca, ast?ma e?lik eden ve ast?m kontrol?n? g??le?tiren rinit, gastro?zefageal refl?, mantar infeksiyonlar?, ila?lar, allerjik bronkopulmoner aspergillozis (ABPA), vask?litler gibi hastal?klar da saptan?p tedavi edilmelidir. Son olarak da tedaviye diren?li ast?m demeden ?nce hastan?n bir ast?m merkezinde en az ?? ay boyunca konunun uzman? hekimler taraf?ndan takip ve tedavi edilmeleri gerekmektedir.
T?m bu yap?lanlara ra?men hasta y?ksek doz standart ast?m tedavisiyle kontrol alt?na al?nam?yorsa ya da ancak y?ksek doz tedaviyle kontrol devam ettirilebiliyor ve ila? dozlar? azalt?lam?yorsa bu grup hastalara da "tedaviye diren?li ast?m" denmektedir.
Tedaviye Diren?li A??r Ast?m Tedavisi
Uluslararas? ast?m tan? ve tedavi k?lavuzlar? a??r ast?m tedavisinde ilk se?enek ila?lar?n inhaler steroid ve uzun etkili beta-agonist kombinasyonu oldu?unu vurgulamaktad?r. Hasta uyumunun daha y?ksek olmas? ve inhaler steroidsiz tek ba??na uzun etkili beta-2 agonist kullan?m?n?n ?nlenmesi i?in her iki ilac?n fiks kombinasyonlar?n?n kullan?lmas? ?nerilmektedir. Ast?ml? hastalar?n b?y?k ?o?unlu?u inhaler steroid uzun etkili beta-agonist kombinasyon tedavisine iyi yan?t verir. A??r ast?ml? hastalarda steroid duyarl?l??? azalm?? olabilir. Y?ksek doz inhaler steroide yan?t al?namayan bir grup hastada sistemik steroide daha iyi yan?t al?nabilir. Ancak obezite, sigara kullan?m?, noneozinofilik inflamasyonun varl??? steroide olan yan?t?n azalmas?na neden olur.
Bu derlemede tedaviye diren?li ast?ml? hastalarda g?ncel tedavi se?enekleri tart???lacak ve GRADE sistemati?i ?er?evesinde ?nerilerde bulunulacakt?r. Kontrols?z ast?m?n en ?nemli nedeni olan "sorunlu hastalar" konusundaki ?neriler bu yaz?n?n kapsam? d???nda tutulmu?tur.
Ayr?nt?l? literat?r taramalar?nda standart tedaviye diren?li ast?m tedavisi konusunda yap?lm?? ?ok az say?da kan?t d?zeyi y?ksek, randomize klinik ?al??ma bulunabilmi?tir. Dolay?s?yla bir?ok ?neri hafif ve orta a??rl?ktaki ast?ml? hastalar?n tedavi ?al??malar?ndan elde edilen sonu?lara g?re indirekt olarak yap?lm??t?r.
Standart tedaviye diren?li ast?m tedavisi kesin s?n?rlarla ayr?lmamakla birlikte iki ba?l?k alt?nda toparlanabilir: Nonfenotipik tedavi ve fenotipik tedavi. Nonfenotipik tedavi, hastal???n ?zelliklerine bak?lmaks?z?n standart tedaviye yan?t vermeyen t?m a??r ast?ml? hastalarda denenebilecek tedavi se?enekleridir. Fenotipik tedavi ise baz? ?zellikleri olan hasta alt gruplar?nda daha iyi yan?t al?nmas? beklenen tedavilerdir. L?kotrien antagonistleri, teofilin, tiotropium nonfenotipik tedavi i?in, allerjik ast?ml? hastada anti-IgE, obez hastada kilo verme, persistan eozinofilisi ve a??r ataklar? olan hastada anti-IL-5'te fenotipik tedavi i?in ?rnek ila?lar olarak kabul edilebilir.
Ast?m tedavisinin temel hedefi ast?m?n kontrol alt?na al?nmas?d?r. Ast?m kontrol? klinik kontrol?n sa?lanmas? ve gelecek risklerin ?nlenmesi anlam?na gelmektedir. Verilen tedaviyle g?nler haftalar i?erisinde hastan?n semptomlar?nda azalma, solunum fonksiyonlar?nda d?zelme, kurtar?c? ila? kullan?m?nda azalmalar olur, buna klinik kontrol denir. Klinik kontrol?n sa?lanmas? hastan?n ya?am kalitesini art?r?r. Uygun tedaviyle uzun d?nemde, aylar, y?llar i?erisinde riskler de azal?r. Burada risk denince kastedilen ast?m ataklar?, solunum fonksiyon kay?plar?, ila? yan etkileri ve ast?m?n instabilitesidir. Ast?mda gelecek riskler hastal???n prognozunu belirler. Gelecek risklerin azalmamas? k?t? prognoz g?stergesidir. Genelde klinik kontrol ile gelecek riskler aras?nda bir ili?ki vard?r. Bir hastada uygun tedaviyle yeterli klinik kontrol sa?lan?rsa gelecek riskler de azal?r. Yani bir hasta ne kadar az semptomatikse, solunum fonksiyon testleri ne kadar normalse o kadar az atak g?r?l?rken, ne kadar ?ok semptomu varsa o kadar s?k atak g?r?lmektedir. Bu do?rudan ili?ki nedeniyle tedavi k?lavuzlar? ast?m tedavisinin ayarlanmas?n? klinik kontrole g?re yap?lmas?n? ?nerirler. Ancak baz? hastalarda semptomlar ile ataklar aras?ndaki bu ili?ki her zaman olmayabilir. Az semptomu olan hastalarda s?k a??r ataklar, ?ok semptomu olan hastalarda nadir ataklar g?r?lebilir. Dolay?s?yla bu grup hastalarda k?lavuzlar?n ?nerdi?i standart tedavilerle iyi yan?tlar al?nmayabilir. Bu grup hastalara "fenotipik ast?m k?meleri" denir. Semptom ve atak ili?kisine g?re a??r ast?ml?lar ?? k?mede toplanabilir; s?k semptom s?k atak, semptom predominant (s?k semptom seyrek atak) ve atak predominant (seyrek semptom s?k atak) (3). Bu ?? k?medeki ast?ml? hastalar?n temel ?zellikleri ?ekil 1'de ?zetlenmi?tir. Her bir k?me farkl? ?zellikleri olan ast?ml? hastalar? kapsamakla birlikte her zaman bu k?melerdeki hastalar?n birbirlerinden kesin s?n?rlarla ayr?lmas? m?mk?n de?ildir ve s?kl?kla ?rt??meler g?r?lebilmektedir. Standart tedaviye diren?li a??r ast?ml? hastalarda fenotipik k?mesel yakla??mlar hastalarda daha rasyonel tedavi se?imini ve tedaviye daha iyi yan?t al?nmas?n? sa?layabilmektedir. Farkl? a??r ast?m fenotiplerinde tedavi se?enekleri de ?ekil 2'de ?zetlenmi?tir.
S?k semptom s?k atak: Erken ya?ta ba?layan, atopi ?yk?s? olan, kad?n a??rl?kl? hastalard?r. Genellikle ailede ast?m, atopi ?yk?s? vard?r. S?k semptom g?r?l?r ve semptomlarla birlikte solunum fonksiyon testlerinde ciddi azalmalar vard?r. Balgam ve periferik kan eozinofilisi vard?r ve buna paralel olarak ekspirasyon havas?nda NO d?zeyleri (FeNO) y?ksektir. Ev hayvan? besleme, bu grupta s?kt?r. ?nhaler steroid tedavisine ?ok iyi yan?t verirler ancak tedavi uyumunda sorunlar oldu?u i?in kontrols?z ast?m oranlar?, acil servis ba?vurular?, hastane yat??lar? olduk?a s?k g?r?l?r.
S?k semptom ve s?k a??r ataklar? olan bu k?medeki hastalar?n tedavisinde temel sorun inhaler steroidlerin yetersiz dozda verilmesi veya hastalar?n inhaler steroidlerini d?zenli kullanmamalar?d?r. Tedavide temel olan, hastalar?n tedaviye uyumunu sa?lamakt?r. ?dame tedavisi ve semptom giderici olarak inhaler steroid- Formeterol fiks kombinasyonlar?n?n kullan?lmas? (SMART) inhaler steroid a????n? kapayaca?? i?in bu grup hastalarda iyi sonu?lar vermektedir. Allerjen duyarlanmas?n?n s?k g?r?ld??? bu grup hastalarda anti-IgE tedavisi de di?er bir se?enektir. Bu k?medeki hastalarda hava yolu inflamasyonu tipik olarak Th2 lenfosit arac?l?kl?d?r, dolay?s?yla anti-IL-13, anti-IL-4 gibi Th2 yola??na y?nelik biyolojik ajanlar gelecekte tedavi protokollerine girecektir. Ayr?ca, bu k?medeki hastalarda fungus infeksiyonlar? da s?k g?r?l?r. Antifungal ila?lar sadece kan?tlanm? ABPA's? olan hastalarda kulan?lmal?d?r, bunun d???nda rutin olarak kullan?lmamal?d?r.
Semptom predominant: Solunum fonksiyon testleri ile uyumlu ya da uyumsuz s?k semptomu olan ancak nadir a??r ataklar? olan hastalar?n k?mesidir. Genellikle ileri ya?ta ba?layan, postmenopozal obez kad?n hastalar?n bulundu?u gruptur. Sigara i?imi bu grupta daha y?ksek orandad?r. Balgam ve periferik kanda eozinofili s?k g?r?lmez. N?trofilik hava yolu inflamasyonu daha ?n plandad?r. FeNO d???kt?r. Dolay?s?yla inhaler ya da sistemik steroide iyi yan?t vermezler.
Semptom predominant ast?m k?mesindeki hastalarda hava yolu inflamasyonunun noneozinofilik olmas? nedeniyle streroide yan?t ?ok iyi olmayabilir, bu nedenle kontrol alt?na al?namayan bu grup hastalarda steroid dozunu art?rmamak gerekir. A??r ataklar seyrek ve semptom s?k oldu?u i?in daha ?ok semptoma y?nelik tedaviler ?n plana ??kmaktad?r. Bu gruptaki obez hastalarda ?ncelikli hedef hastan?n kilo vermesini sa?lamakt?r. S?k infeksiyon ?yk?s? olanlarda makrolid antibiyotikler, standart tedaviyle kontrol alt?na al?namayan hastalarda bron?iyal termoplasti denenebilir.
Atak predominant: Bu k?medeki hastalar?n en ?nemli ?zellikleri s?k semptom olmaks?z?n a??r ataklarla seyretmesidir. Genellikle ileri ya?larda ba?layan, eozinofilik ve nonatopik erkek hastalar bu gruptad?r. Y?ksek doz inhaler, hatta sistemik steriod tedavisine ra?men periferik kanda ya da balgamda eozinofili devam eder. Aspirin duyarl?l???n?n, nazal polip ve kronik sin?zitin en s?k g?r?ld??? hastalar bu gruptad?r. K???k hava yolu tutulumu ve fiks hava yolu obstr?ksiyonu da bu grup hastalarda s?kt?r.
Y?ksek doz inhaler steroide iyi yan?t vermeyen, s?k atak ve persistan eozinofili ile giden bu grup hastalarda parenteral depo steroid ile yan?t al?nd???n? g?steren ?al??malar vard?r. Eozinofilik inflamasyonu tedavi eden anti-IL-5 gibi biyolojik ajanlar ?mit vadetmektedir ancak hen?z klinik kullan?ma sunulmam??t?r. Analjezik intolerans?n?n y?ksek oranda g?r?ld??? bu grup hastada aspirin desensitizasyonu da ?nemli bir tedavi se?ene?i olabilir.
G?n?m?zde tedaviye diren?li a??r ast?ml? hasta gruplar? ve bu gruplardaki tedavi se?enekleri hakk?nda genel bilgiler verildikten sonra s?z? edilen her bir tedavi i?in kan?t d?zeyleri, panelistlerin g?r??leri, ?neriler ve yorumlar belirtilecektir.
Soru: Tedaviye diren?li a??r ast?ml? hastalarda l?kotrien resept?r antagonistleri (LTRA) kullan?lmal? m??
Tedaviye diren?li a??r ast?ml? hastalarda inhaler steroid, uzun etkili beta-agonist kombinasyonuna LTRA eklenmesini ara?t?ran yay?nlanm?? ?al??ma bulunamam??t?r. Ancak orta, a??r ast?ml? hastalarda inhaler steroide LTRA eklenmesiyle yap?lan birka? ?al??mada klinik ek yarar sa?land??? g?sterilmi?tir (4). ?nhaler steroide uzun etkili beta-2 agonist ya da LTRA eklenmesini ara?t?ran ?al??malarda uzun etkili beta-agonistler daha etkin bulunmu?tur (5,6). Aspirin duyarl? ast?ml? hastalarda inhaler steroide LTRA eklenmesinin daha iyi ast?m kontrol? sa?lad???n? g?steren ?al??malar vard?r (7,8).
?neri ve yorum: Tedaviye diren?li a??r ast?ml? hastalarda inhaler steroid, uzun etkili beta-2 agonist kombinasyonuna LTRA eklenmesini ara?t?ran ?al??ma yoktur, ancak hafif orta a??rl?ktaki ast?ml?larda yap?lan ?al??ma sonu?lar?ndan ??kar?mlar yap?labilir. Dolay?s?yla "kan?t d?zeyi d???kt?r". T?m k?lavuzlarda ilk ?? basamakta inhaler steroide alternatif ikinci se?enek ila? olarak kabul edilen LTRA'lar?n a??r ast?m hastalarda ek tedavide kullan?lmas? "kuvvetli pozitif" olarak kabul edilmi?tir. Panel ?yelerinin 14'? evet, biri ?ekimser oy kullanm??t?r. ?zellikle aspirinle ind?klenen ast?ml? hastalarda ?nerilebilir.
Soru: Tedaviye diren?li a??r ast?ml? hastalarda teofilin kullan?lmal? m??
Tedaviye diren?li a??r ast?ml? hastalarda inhaler steroid, uzun etkili beta-2 agonist kombinasyonuna teofilin eklenmesini ara?t?ran yay?nlanm?? ?al??ma bulunamam??t?r. Orta a??rl?ktaki ast?ml? hastalarda inhaler steroide teofilin eklenmesinin daha iyi ast?m kontrol? sa?lad???n? g?steren ?al??malar vard?r (9,10). Sigara i?en ast?ml? hastalarda d???k doz inhaler steroide teofilin eklenmesiyle daha iyi ast?m kontrol? sa?lanm??t?r (11). Bu da sigaran?n neden oldu?u HDAC s?presyonuna ba?l? steroide duyarl?l???ndaki azalman?n teofilin taraf?ndan ortadan kald?r?lmas?yla a??klanabilmektedir (12).
?neri ve yorum: Tedaviye diren?li a??r ast?ml? hastalarda inhaler steroid, uzun etkili beta-2 agonist kombinasyonuna teofilin eklenmesini ara?t?ran ?al??ma yoktur. Dolay?s?yla "kan?t d?zeyi d???kt?r". Orta, a??r ast?ml?larda yap?lan ?al??ma sonu?lar?ndan ??kar?mlar yap?labilir. Panel ?yelerinin 15'inin evet oyu ile "zay?f pozitif" olarak ?nerilmi?tir. Sigara i?en veya steroide diren? d???n?len hastalarda ?ncelikle ?nerilir.
Soru: Tedaviye diren?li a??r ast?ml? hastalarda tiotropium kullan?lmal? m??
Ast?m ataklar?nda rutin kullan?lan k?sa etki antikolinerjiklerden (ipratropium bromide) sonra, d?z kas kontraksiyonunu ve mukus sekresyonunu inhibe eden, uzun etkili antikolinerjikler (tiotropium bromide) KOAH tedavisinde y?llard?r yerini alm??t?r (13). ?pratropium bromide'in ast?m ataklar?nda k?sa etkili beta-agonistlere ek olarak kullan?lmas?n?n ek bronkodilastasyon sa?lad??? bilinmektedir. Uzun etkili antagonistlerin ast?m idame tedavisinde kullan?m?na dair randomize kontroll? ?al??malar ise son birka? y?l i?inde yay?nlanmaya ba?lam??t?r.
2010 y?l?nda "Asthma Clinical Research Network (ACRN)" taraf?ndan y?r?t?len, d???k doz inhaler steroidle kontrol alt?nda olmayan ast?ml? hastalara eklenen tiotropiumun etkilerinin ara?t?r?ld??? ?al??ma 210 ast?ml? hastada y?r?t?lm??t?r. Bu ?al??mada inhaler steroid dozunun iki kat?na ??kar?lmas?n?n etkisi, tedaviye salmeterol veya tiotropium eklenmesiyle kar??la?t?r?lm??t?r. Bir y?l sonunda PEF, FEV1, ast?m?n kontrol alt?nda oldu?u g?nler ve g?nd?z semptomlar?na bak?larak, tedaviye eklenen tiotropiumun inhaler steroid dozunun iki kat?na ??kar?lmas?ndan ?st?n, salmeterole g?re benzer etkinli?i oldu?u g?sterilmi?tir (14).
Orta a??r ast?ml?lardaki ilk ?al??ma ise Bateman ve arkada?lar? taraf?ndan yap?lm??t?r. Beta-2 adrenerjik resept?r gen polimorfizmi olan (B16 Arg/Arg), inhaler steroidle kontrol alt?nda olmayan orta a??r ast?ml?larda tiotropiumla, plasebodan ?st?n, salmeterole benzer solunum fonksiyon testi d?zelmeleri g?r?lm??, her ?? grupta da benzer oranda istenmeyen etki g?r?lm??, tiotropiumun basamak art?rmada salmeterole alternatif olabilece?i sonucuna var?lm??t?r (3,4,5,6,7,8,9,10,11,12,13,14,15). Sonraki y?llarda ise daha a??r ast?ml? hastalardaki yeri de?erlendirilmi?tir.
Ortalama FEV1 de?erleri %58 olan, en az iki kontrol edici ast?m tedavisi kullanan kontrols?z a??r ast?mda tiotropiumun iki farkl? dozunun (5-10 mcg) de?erlendirildi?i di?er bir randomize ?al??mada ise her iki dozun da plaseboya g?re anlaml? olarak solunum fonksiyon testlerini d?zeltti?i, ast?m ili?kili sa?l?k durumu ve semptomlar a??s?ndan ise gruplar aras? fark olmad??? g?sterilmi?tir (16).
Standart kombinasyon tedavisi kontrol alt?na al?namayan ast?ml?larda tiotropiumun etkinli?inin de?erlendirildi?i en geni? ?al??mada, ortalama FEV1 de?eri %54 olan 912 ast?ml? hastada, inhaler steroid ve salmeterol kombinasyonuna eklenen tiotropiumun plaseboya g?re bir y?l sonunda yan etki riskini art?rmadan sistemik steroid gerektiren ast?m ataklar?n? azaltt???, solunum fonksiyon testlerini iyile?tirdi?i g?zlenmi?tir (17).
Hangi ast?ml? olgular?n tiotropiuma daha iyi yan?t verdi?ini ara?t?ran ?al??malarda, d???k FEV1 de?eri olanlar?n, FEV1/FVC oran? d???k hastalar?n, gen? olgular?n, erkeklerin, ge?mi?te pasif veya aktif sigara ?yk?s? olanlar?n, beta-agonist ile reverzibilitesi daha fazla olanlar?n, amfizemi olan ast?ml?lar?n tiotropiuma daha iyi yan?t verdikleri g?sterilmi?tir (16,17,18,19).
Alt? randomize kontroll? ?al??mada 1648 kontrols?z ast?ml? hastada tiotropiumun etkilerinin de?erlendirildi?i meta-analizde ise tiotropiumun yan etki oran?nda art??a neden olmadan plaseboya g?re solunum fonksiyonlar?n? anlaml? d?zeltti?i, kurtar?c? ila? gereksinimi azaltt??? ancak gece semptomlar?na etkisi olmad??? g?sterilmi?tir (20).
?neri ve yorum: Tedaviye diren?li a??r ast?ml? hastalarda tiotropiumun kullan?m? konusundaki ?al??ma ve olgu say?s?n?n k?s?tl? olmas? nedeniyle "kan?t d?zeyi d???k" bulunmu?tur. Yap?lan oylamada 12 ki?i "evet", bir ki?i "hay?r", iki ki?i de "?ekimser" oy kullanm??t?r. D?rd?nc? basamak ve daha a??r ast?ml? hastalarda, ?zellikle sigara ?yk?s? olan olgularda standart tedaviye ek olarak kullan?lmas? "kuvvetli pozitif" olarak ?nerilir. G?venlik a??s?ndan ast?ml? hastalarda ?al??ma say?s? az oldu?undan kesin yorum yap?lamamakla birlikte KOAH'l? hastalarda yap?lan kapsaml? g?venlik ?al??malar? dikkate al?nd???nda kardiak sorunlar? olan hastalarda dikkatli takip ?nerilir.
Soru: Tedaviye diren?li a??r ast?ml? hastalarda inhaler steroid, formoterol fiks kombinasyonu ila?lar idame tedavisi ve kurtar?c? olarak (SMART) kullan?lmal? m??
?nhaler steroid + formoterol fiks kombinasyonunun d?zenli sabah ak?am idame tedavisi ve ayn? zamanda bu kombinasyonun ast?m semptomlar? oldu?u zaman semptom giderici olarak kullan?lmas? y?ntemine "Single Inhaler for Maintenance and Reliever Therapy (SMART)" konsepti denir. Ast?m ataklar? genellikle atak ?ncesi semptomlarda art??lar? takiben ortaya ??kar, yani artm?? semptomlar gelecek ata??n habercisidir. Bu tedavi konsepti atak ?ncesi artan semptomlar? h?zl? etkili bir beta-agonist olan formoterol ile giderirken, bu arada artan dozlarda inhaler steroid vererek gelecek ataklar?n ?nlenmesi mant???na dayan?r. Budesonid ve formoterol fiks kombinasyonuyla yap?lm??, on binlerce hastay? i?eren SMART ?al??malar? vard?r (21,22,23,24,25,26,27). T?m bu ?al??malarda inhaler steroid + uzun etkili beta-agonist kombinasyonu idame tedavisi ve k?sa etkili beta-agonistin semptom giderici olarak kullan?ld??? standart tedavi y?ntemleriyle kar??la?t?r?ld???nda ast?m ataklar?nda SMART ile anlaml? azalmalar?n oldu?u g?sterilmi?tir. Benzer ?ekilde beklometazon ve formoterol fiks kombinasyonu ile de standart tedaviye g?re ataklar azalm?? bulunmaktad?r (28). Ayr?ca, yap?lan ?al??malarda ?zellikle artm?? semptomlarla birlikte s?k a??r ataklar? olan hastalarda SMART ile ataklarda ?nemli azalmalar?n oldu?u g?sterilmi?tir (29,30).
?neri ve yorum: Standart tedaviye g?re SMART ile ast?m ataklar?nda anlaml? azalmalar sa?land??? konusunda "kan?t d?zeyi y?ksek" yay?nlar bulunmaktad?r. ?zellikle s?k semptom ve s?k atak k?mesindeki, inhaler steroide iyi yan?t veren eozinofilik, atopik ast?ml? hastalarda "kuvvetli pozitif" olarak ?nerilir. Panel ?yelerinin hepsi bu y?nde "evet" oyu kullanm??t?r.
Soru: Tedaviye diren?li a??r ast?ml? hastalarda anti-IgE kullan?lmal? m??
Bir monoklonal antikor olan omalizumab, dola??mdaki serbest IgE'yi ba?lar ve IgE'nin y?ksek ve d???k afiniteli resept?rlere ba?lanmas?n? ?nleyerek antiinflamatuvar etkinlik g?sterir (31).
?ok merkezli, randomize kontroll? ?al??malar, g?zlemsel ?al??malar ve ger?ek ya?am verilerinde anlaml? olarak acil ba?vurular?n?, atak oranlar?n? ve oral steroid gereksinimini azaltt??? g?sterilmi?tir (32,33,34,35,36,37,38,39). Ast?m kontrol?n?n omalizumab ba?lanan olgularda ilk alt? ay i?inde d?zeldi?i ve alt? y?la kadar korundu?unu g?steren g?zlemsel ?al??malar vard?r (37,38). Semptomlar?n d?zeldi?ini, kurtar?c? gereksiniminin azald???n? ve FEV1 de?erlerinde anlaml? d?zelmeler, ya?am kalitesinde anlaml? art??lar?n oldu?unu g?steren ?al??malar ?o?unluktad?r (32,36,37,38,39). Omalizumab tedavisine yan?t genellikle tedavinin 16. haftas?ndan itibaren de?erlendirilir ancak baz? hastalarda yan?t daha ge? ortaya ??kabilmektedir (40). Tedaviye iyi yan?t veren hasta oranlar? %50 ile %90 aras?nda de?i?mektedir, ancak ?nceden hangi hastan?n daha iyi yan?t verece?ini ?n g?rmek m?mk?n olmamaktad?r (33,35,39).
?lave oral steroid kullanan olgularda da atak d?zeylerini kullanmayan olgulardan daha fazla azalt?labildi?i g?sterilmi?tir (41). Sistemik steroidin omalizumab kullan?m? sonras?nda kesilebildi?i ve azalt?labildi?i olgular ?o?unlukta olmakla birlikte kan?t d?zeyi zay?ft?r (42).
Omalizumab kullan?m?na ba?l? olarak enjeksiyon yerindeki cilt reaksiyonlar? plaseboya g?re daha y?ksek bulunmu?tur. Binde iki olarak bildirilen anafilaksi d???nda kanser, parazitoz, kardiyovask?ler, serebrovask?ler olaylar vb. gibi ciddi yan etkiler plasebodan farks?z bulunmu?tur.
Omalizumab?n hastane yat??lar? ve acil ba?vurular?n? azaltarak sa?l?k harcamalar?nda azalma sa?lad???n? g?steren ?al??malar vard?r (43). Ancak maliyet analizleri anti-IgE tedavisinin y?ksek maliyetli bir tedavi y?ntemi oldu?unu g?stermektedir (33).
?neri ve yorum: A??r allerjik ast?ml? hastalarda anti-IgE tedavisi ?al??malar?n?n "kan?t d?zeyi y?ksektir". A??r allerjik ast?ml? hastalarda anti-IgE tedavisinin kullan?lmas? y?n?nde panelistlerin tamam? (16 ki?i) evet oyu kullanm??t?r. D?zenli y?ksek doz inhaler steroid ve uzun etkili beta-agonist kombinasyon tedavisine ra?men kontrol alt?nda al?namayan, 12 ya? ve ?zeri, perennial allerjisi olan, total IgE d?zeyi 30 IU/mL ile 1500 IU/mL aras?nda olan allerjik ast?ml? hastalarda kullan?lmas? "kuvvetli pozitif" olarak ?nerilir, ancak tedavi maliyetinin y?ksek olmas? da dikkate al?nmal?d?r.
Soru: Tedaviye diren?li obez, a??r ast?ml? hastalarda medikal ya da cerrahi kilo verme y?ntemleri uygulanmal? m??
Obezite ve ast?m halk sa?l??? ?zerine ?nemli etkileri olan hastal?klard?r. Son y?llarda her iki hastal???n prevalans?nda paralellik g?steren art??lar?n g?r?lmesi, epidemiyolojik olarak aralar?nda bir ili?ki olabilece?ini d???nd?rm??t?r. Beden kitle indeksi (BK?)'nin 30'un ?zerinde olmas?n?n ast?m riskini 2.7 kat art?rd??? yap?lan ?al??malarda g?sterilmi?tir (44). BK? art???n?n ast?ma neden olmas? konusunda akci?er mekanikleri , imm?nolojik, genetik, epigenetik, cinsiyet ve hormonal, komorbiditeler, oksidatif stres, inflamasyon, adipokinler, ?evresel ve davran??sal ortak fakt?rler gibi pek ?ok mekanizma rol oynamaktad?r (45). Ancak her ast?ml? BK? art???ndan e?it olarak etkilenmemektedir, burada ast?m?n ortaya ??k?? ya??n?n ?nemi vurgulanmaktad?r. Erken ve ge? ya?ta ortaya ??kan ast?ml?larda tedavinin farkl? planlanmas? gerekmektedir (46,47). Ge? ba?lang??l? ast?mda kilo verme stratejileri daha ?ok i?e yaramaktad?r (48,49).
Obeziteye ba?l? ast?m ayr? bir ast?m fenotipi olarak belirmektedir. Ge? ya?, kad?n cinsiyet, daha fazla semptom ve hastal?k kontrol?n?n daha zor oldu?u, noneozinofilik hava yolu inflamasyonunun g?r?ld??? ve kontrol edici ila?lara daha az yan?t veren bir gruptur (50). Semptomlar?n ?iddeti var olan inflamasyonla uyumsuzdur.
Obez ast?ml?larda tedavi yan?t? yetersiz olmaktad?r (51) . Daha y?ksek doz steroid gerekmekte bu da yan etkilere yol a?maktad?r. Bu nedenle alternatif tedaviler g?ndeme gelmeli ve hastalara kilo verdirilmelidir. Kilo vermeyle hastal?k kontrol?nde art?? bildiren ?al??malar pek ?oktur. FEV1, FVC gibi solunum fonksiyon parametreleri d?zelmekte, semptom ve kurtar?c? kullan?m?nda azalma ve ya?am kalitesinde iyile?meler belirgin olmaktad?r, ayr?ca ast?m kontrol testi ile de?erlendirilen hastal?k kontrol?nde de belirgin d?zelme g?r?lmektedir (52,53,54) Obeziteye ba?l? geli?en uyku bozukluklar? (OSAS), tip II diyabet, metabolik sendrom, gastro?zefageal refl? (G?R) gibi komorbiditeler de mutlaka tedavi edilmelidir (55).
BK? > 40 olan ki?ilerde kilo verme denenmeli ba?ar?l? olunmaz ise ancak bariatrik cerrahi endikasyonu g?ndeme gelmelidir (55). Bariatrik cerrahi sonras? hem klinik parametrelerde d?zelme saptanmakta hem de inflamasyonda belirgin d?zelme g?r?lmektedir (47,56) Ayr?ca, ila? kullan?m?nda %50'ye yak?n azalmayla hastal?k maliyetinde de belirgin d???? g?r?lmektedir (57).
Son y?llarda yay?nlanan iki meta-analizde obezite-ast?m ili?kisi ve tedavisi konusunda randomize kontroll? ?al??malar?n azl??? ve daha uzun soluklu ?al??malara gereksinim oldu?u vurgulanmaktad?r (58,59).
?neri ve yorum: Tedaviye diren?li, obez, a??r ast?ml? hastalarda kilo vermenin ast?m kontrol?ne etkisini ara?t?ran ?al??malar?n kan?t d?zeyi "orta d?zeyde" bulunmu?tur. Obez hastalarda kilo verme konusunda t?m panelistler ortak g?r??tedir ve "kuvvetli pozitif" olarak ?nermektedir. Diyet, egzersiz, ila?lar vb. y?ntemler uygulanmas?na ra?men kilo veremeyen hastalarda bariatrik cerrahi ?nerilir. Obezite ile birlikte s?k g?r?len G?R, OUAS gibi komorbiditeler de tedavi edilmelidir.
Soru: Tedaviye diren?li a??r ast?ml? hastalarda makrolid antibiyotikler kullan?lmal? m??
A??r ast?m heterojen bir hastal?k olup eozinofilik ve noneozinofilik fenotipleri vard?r. Noneozinofilik ast?mda inhaler steroid tedavisine ?ok iyi yan?t al?namaz. A??r ast?mda hastal?k s?resi genellikle daha uzundur, atopi oran? daha d???kt?r ve bu hastalar y?ksek doz inhaler kortikosteroid (?KS) + uzun etkili beta-2 agonistler ile tedaviye kar??n s?kl?kla sistemik steroid tedavisine gereksinim duyarlar. Makrolid antibiyotiklerin antimikrobiyal etkilerinin yan? s?ra antiinflamatuvar etkileri vard?r. Kronik n?trofilik hava yolu hastal?klar?nda makrolid kullan?m?n?n etkili oldu?u bildirilmi?tir (60). Kontrols?z ast?ml? olgularda almakta olduklar? tedaviye ek olarak uzun s?reli makrolid kullan?m?n?n semptomlarda, ya?am kalitesinde, PEF de?erlerinde ve hava yolu a??r? duyarl?l???nda d?zelmeye yol a?t??? bir meta-analizde bildirilmi?tir (61).
Tedaviye diren?li a??r ast?ml? hastalarda makrolid antibiyotiklerin uzun s?reli olarak tedaviye eklenmesine y?nelik birka? ?al??ma bulunmaktad?r.
Simpson ve arkada?lar?, randomize ?ift-k?r plasebo kontroll? ?al??malar?nda a??r ast?ml? olgular?n bir grubuna klaritromisin (2 x 500 mg/g?n), di?er grubuna plasebo vermi?ler ve n?trofilik inflamasyon bulgular?n? ve klinik parametreleri incelemi?lerdir. Sekiz haftal?k tedavi sonras? balgam IL-8 ve n?trofil d?zeylerinde makrolid grubunda belirgin azalma, ayn? grupta ya?am kalitesi ?l?eklerinde d?zelme bulmu?lard?r. Ancak ?al??ma n?trofilik inflamasyon g?stergelerini ilk sonlan?m noktas? olarak ald???ndan klinik ?l??tlerin de?erlendirilmesi i?in yeterince g??l? de?ildir (62).
Birinci basamakta y?r?t?len randomize, plasebo kontrollu, ?ift-k?r bir ?al??mada ise kontrolsuz ast?ml? olgular al?nm??; bir gruba azitromisin (600 mg/hafta), di?erine plasebo 12 hafta uygulanm?? ve bir y?l izlenmi?lerdir. Daha a??r ast?ml?, daha ge? ba?lang??l?, daha az atopik olan ???nc? bir gruba azitromisin (500 mg/hafta) verilmi? ve bu grup a??k olarak takip edilmi?tir. Ast?m semptomlar?nda, kontrol ve ya?am kalitesi ?l?eklerinde birinci ve ikinci grupta d?zelme olmazken, daha a??r ast?ml? olgularda bu parametrelerde anlaml? iyile?me g?zlenmi? ve bu d?zelme bir y?ll?k izlem s?resince devam etmi?tir (63).
Brusselle ve arkada?lar?, randomize, ?ift-k?r, plasebo kontrollu, paralel grup, ?ok merkezli bir ?al??ma y?r?tm??ler ve y?ksek doz ?KS + uzun etkili beta-2 agonist kullanmas?na kar??n son bir y?lda en az iki ast?m ata?? ve/veya solunum yolu infeksiyonu ?yk?s? olan ast?ml? hastalar? ?al??maya alm??lard?r. Aktif gruba 26 hafta boyunca, haftada 3 g?n 250 mg azitromisin uygulanm?? ve ?ncelikli olarak ast?m ata?? ve solunum yolu infeksiyonu s?kl??? ara?t?r?lm??t?r. Bunlara ek olarak solunum fonksiyon testi (SFT), ast?m kontrol?, ya?am kalitesi ve g?venlik de?erlendirilmi?tir. Sonu? olarak a??r ast?ml?larda tedaviye eklenen alt? ayl?k makrolid tedavisinin atak ve alt solunum yolu infeksiyonu s?kl???n? azaltmad??? g?r?lm??t?r. Ancak noneozinofilik ast?ml? alt grupta makrolidler ile atak s?kl???nda belirgin azalma sa?lanm??t?r. Genel olarak azitromisin uzun s?reli kullan?mda iyi tolere edilmi?tir (64).
?neri ve yorum: Tedaviye diren?li a??r ast?ml? hastalarda tedaviye uzun s?reli makrolid antibiyotiklerin eklenmesinin etkinli?i ile ilgili kan?tlar yetersizdir, "kan?t d?zeyi d???kt?r". Panel ?yelerinden alt?s? evet, d?rd? hay?r, ikisi ?ekimser oy kullanm?? ve "zay?f negatif ?neri" olarak kabul edilmi?tir. Noneozinofilik/n?trofilik olgularda, atipik mikroorganizmalar?n solunum yolu sekresyonlar?ndan izole edildi?i olgular ve s?k infeksiyon k?kenli atak ge?irenler ge?iren hastalarda denenebilir. Ancak uzun s?reli tedavi s?z konusu oldu?undan makrolidlere diren? geli?imi, kardiyo ve ototoksik yan etkiler g?z ?n?nde bulundurulmal?d?r.
Soru: Tedaviye diren?li a??r ast?ml? hastalarda TNF-α antagonistleri kullan?lmal? m??
Sa?l?kl? bireylere inhale rekombinant TNF-α verilmesi bron? hiperreaktivitesine ve hava yollar?nda n?trofiliye neden olmu?tur (65). Ast?ml? hastalarda yap?lan g?zlemsel ?al??malar TNF-α mRNA ve protein d?zeylerinin bu hastalar?n hava yollar?nda artm?? oldu?unu g?stermi?tir (66). Howard ve arkada?lar? hafif ve a??r ast?ml?larda yapt??? bir ?al??mada, TNF-α, TNF-α protein ve mRNA ekspresyonunun a??r ast?ml?lar?n BAL s?v?lar?nda ve bron?iyal biyopsilerinde artt???n? g?zlemlemi?, yine flow sitometre ile periferik kanda artm?? bulunan m TNF-α ve TNF-α resept?r 1 sadece a??r hastal?kta tespit edilmi?tir. TNF-α'n?n upreg?lasyonu a??r refrakter ast?m?n bir ?zelli?i oldu?u d???n?lerek a??r ast?mda ve ?zellikle n?trofilik inflamasyonla giden fenotiplerde anti-TNF-α tedavilerine yan?t al?nabilece?i d???n?lm??t?r (67).
Etanercept ile a??r ast?ml?larda yap?lan iki plasebo kontroll? ?al??madan biri olan Berry ve arkada?lar?n?n ?al??mas?nda BHR ve FEV1, d?zeyleri ve ast?m kontrol anketinde d?zelmeler saptan?rken, Morjoria ve arkada?lar?n?n ?al??mas?nda sadece ast?m kontrol testinde anlaml? d?zelme bulunmu?, di?er parametreler plasebodan farks?z olarak g?zlenmi?tir (68,69). Holgate ve arkada?lar? 132 orta-a??r ast?ml? hastaya plasebo kontroll? olarak yapt?klar? faz II ?al??mada 12 hafta s?reyle etanercept (25 mg sc) ve plasebo kullanm??lard?r. ?zlenen veriler, beklenen prebronkodilat?r FEV1 y?zdesi, ast?m kontrol anketi, ast?m ataklar? ve bron? hiperreaktivitesi olup sonu?lar plasebo ile kar??la?t?r?ld???nda farkl?l?k saptanmam??t?r. ?al??ma s?resince etanercept iyi tolere edilmi? ama ast?ml? hastalarda ?ok ?nemli bir yarar sa?lanamam??t?r. Ara?t?rmac?lar bu y?zden de ast?m tedavisinde yerinin olup olmayaca??n?n a??kl?k kazanmad???n? bildirmi?lerdir (70).
En fazla hasta kat?l?ml? bir ?al??mada 309 kontrol alt?nda olmayan (y?ksek doz ?KS ve uzun etkili beta-2 agoniste ra?men ve y?lda iki veya daha fazla atak ge?iren) a??r ast?ml? hasta 52 hafta s?reyle golimumab alan 3 grup (50, 100 ve 200 mg sc golimumab) veya plasebo alan 1 gruba ayr?lm??, g?venlik a??s?ndan da izlem 72 hafta s?rd?r?lm??t?r. Primer sonlan?m olarak beklenen FEV1 prebronkodilat?r y?zdesinde bazale g?re de?i?im ve a??r ataklar?n s?kl??? incelenmi?tir. 24. haftada bir?ok hasta ba?ta infeksiyonlar, malignansi (8 ki?i) ve 1 ?l?m olmak ?zere ciddi yan etkiler nedeniyle ?al??madan ayr?lm?? ve ?al??ma bu haftada sonland?r?lm??t?r. Primer sonlan?m a??s?ndan aktif tedavi ve plasebo gruplar? aras?nda farkl?l?k bulunmam??t?r (71).
?neri ve yorum: Tedaviye diren?li a??r ast?ml? hastalarda anti-TNF-α kullan?m? konusundaki ?al??ma ve olgu say?s?n?n k?s?tl? olmas? nedeniyle "kan?t d?zeyi orta" bulunmu?tur. Yap?lan oylamada oylamaya kat?lan 14 ki?i de kullan?lmamas? y?n?nde oy (hay?r) kullanm??t?r. Etkinli?inin belirsiz olmas?, ciddi yan etkilerinin fazla olmas? ve maliyetinin y?ksek olmas? nedeniyle "kuvvetli negatif" olarak ?nerilmektedir.
Soru: Tedaviye diren?li a??r ast?ml? hastalarda bron?iyal termoplasti uygulanmal? m??
Ast?ml? hastalarda hava yolu d?z kas art??? remodelingin bir par?as?d?r. A??r ast?mdan ?len hastalar?n doku ?rneklerinde hava yolu d?z kas h?crelerinde belirgin hipertrofi ve hiperplazi g?zlenmi?tir. Bu kas kitlesi hipersekretuvar, hiperkontraktil ve hiperproliferatif olma ile karakterli ?zel bir fenotip g?sterir. Ast?mda artm?? hava yolu d?z kas? hem bazal bir bronkokonstriksiyon yaratmakta hem de tetikleyicilere abart?l? yan?tlar ile g?nl?k ast?m yak?nmalar? veya ast?m ataklar?na yol a?maktad?r. Bu nedenle hava yolu d?z kas kitlesinin azalt?lmas?n?n, obstr?ksiyonu ve hava yolu remodelingini azaltarak hastal???n kontrol? ?zerinde etkili olaca?? varsay?labilir. Bron?iyal termoplasti direkt olarak hava yolu d?z kaslar?n? hedeflemi? ilk nonfarmakolojik tedavi se?ene?idir. Termal enerji ile hava yolu d?z kas kitlesi azalt?larak a??r ast?mda hastal???n kontrol alt?na al?nmas? ama?lanmaktad?r (72). K?peklerde ve akci?er kanserli hastalarda yap?lan ilk ?al??malarda bu kas kitlesinin ?nemli oranda azalt?labildi?i ve bunun bron? hiperreaktivitesinde azalmayla birlikte oldu?u g?sterilmi?tir (73,74). Arkas?ndan hafif-orta ast?ml? hastalarda yap?lan pilot ?al??mada bron?iyal termoplastinin erken ve ge? d?nemde g?venli oldu?u ve de sabah/ak?am PEF de?erleri, semptomsuz g?n say?s? ve bron? hiperreaktivitesi d?zelme ile birlikte oldu?u g?r?lm??t?r (75). Bron?iyal termoplasti ile ilgili esas veriler bundan sonra yap?lan ?? randomize kontroll? ?al??ma ile elde edilmi?tir (76,77,78).
?lk randomize kontroll? ?al??ma, orta-a??r ast?ml? 112 hastada yap?lm??t?r. ?al??maya ?KS ile birlikte uzun etkili beta-2 agonist kullanan ve uzun etkili beta-2 agonist kesilmesiyle ast?m kontrol? bozulan hastalar al?nm??t?r. Hastalar?n bir k?sm? bron?iyal termoplasti alm??, di?er grup ?KS veya ?KS + uzun etkili beta-2 agonist tedavisine devam etmi?ler. Bir y?ll?k izlem sonunda primer sonlanma noktas? olan hafif ataklar 3. ve 12 ayda bron?iyal termoplasti alan grupta anlaml? azalm??. Sekonder sonlanma noktalar? olan sabah PEF, semptomsuz g?nler, kurtar?c? ila? kullan?m?, ast?m ya?am kalitesi ve ast?m kontrol anketlerinde bron?iyal termoplasti alan grupta anlaml? d?zelmeler olmu?, FEV ve metakolin bron? hiperrreaktivitesinde de de?i?iklik olmam?? (76).
?kinci RK?, 34 a??r ast?ml? hastada bron?iyal termoplastinin g?venlik ve etkinli?ini de?erlendirmi?. Hastalar?n y?ksek doz ?KS, uzun etkili beta-2 agonist ve yar?s?n?n sistemik kortikosteroid ald??? bu ?al??mada bron?iyal termoplasti yap?lan hastalarda; ast?m ya?am kalitesi ve ast?m kontrol anketlerinde, kurtar?c? ila? kullan?m?nda ve pre-bronkodilat?r FEV1 de?erinde anlaml? d?zelmeler olmu?, ancak sabah/ak?am PEF, semptomsuz g?nler, semptom skorlar?, bron? hiperreaktivitesi ve post-bronkodilat?r FEV1 de?i?memi? (77).
Son randomize kontroll? ?al??ma, ilk plasebo kontroll? ?al??ma olarak ?zel bir ?neme sahiptir. ?ok merkezli olan bu ?al??maya toplam 288 hasta al?nm?? ve bron?iyal termoplasti alan hastalar?n %79?u, plasebo yap?lanlar?n ise %64??nde ast?m ya?am kalitesi skorlar?nda anlaml? d?zelmeler olmu?. Plasebo alanlarda da ya?am kalitesinde d?zelmelerin olmas? ilgin?tir. Tedavi sonras? bir y?ll?k izlemde ise a??r atak, ast?m nedenli acil ba?vurular? ve hospitalizasyonlar bron?iyal termoplasti grubundaki plaseboya g?re anlaml? olarak az g?r?lm?? (78). Bu ?? ?al??mada, bron?iyal termoplasti yap?lan hastalarda erken d?nemlerinde hospitalizasyon gerektiren solunumsal sorunlar olmu? ancak bir y?ll?k izlemde g?venlik verirleri a??s?ndan fark g?r?lmemi?tir. Ayr?ca, iki randomize kontroll? ?al??man?n 5 y?ll?k izlemlerinde g?venlik ve etkinli?in s?rd??? bildirilmi?tir (79,80). Ancak ?al??man?n plasebo aya??ndaki hastalar?n izlemi erken sonland?r?lm??t?r.
Sonu? olarak a??r ast?ml?lardaki az say?daki ?al??ma, bron?iyal termoplasti ile bron? hiperreaktivitesi ve FEV1 de?i?iklik olmad???n? ancak ya?am kalitesi, a??r atak, acil ba?vurusu, okul ve i?e gidilemeyen g?nlerde azalma oldu?unu g?stermi?tir. Ancak bu ?al??malara al?nma kriterlerinin ?ok k?s?tlay?c? olmas? bron?iyal termoplastinin hangi a??r ast?m fenotipi i?in uygun oldu?unu belirlemeyi zorla?t?rmaktad?r. Tedaviye yan?t? belirleyen fakt?rler bilinmemektedir. Hastalarda erken d?nemde hospitalizasyona gidebilecek kadar ciddi solunumsal yan etkiler olmakla birlikte bron?iyal termoplastinin risk/yarar oran? hakk?nda veri yoktur? (81,82). Y?r?t?lmekte olan ve termoplastiye daha iyi yan?t veren hasta grubunun klinik, fizyolojik, biyolojik ve g?r?nt?leme y?ntemleri ile belirlenmesini ara?t?ran (NCT01185275), bronkoskopik biyopsiler ile termoplastiye klinik ve histolojik (inflamasyon) yan?t? (NCT01974921) belirleyecek olan ve bronkoskopik biyopsiler ile termoplasti ?ncesi ve sonras? bron? d?z kas y?zey alan?n?n ?l??lmesini ara?t?ran (NCT01777360) ?al??malar tamamlan?p sonu?lar? yay?nland?ktan sonra bron?ial termoplastinin ast?m tedavisindeki yeri daha anla??l?r olacakt?r
?neri ve yorum: Tedaviye diren?li a??r ast?ml? hastalarda bron?ial termoplasti konusundaki ?al??ma say?s?n?n az olmas?, ?al??ma sonu?lar?n?n birbirleri ile uyumlu olmamas? nedeniyle "kan?t d?zeyi d???k" bulunmu?tur. Yap?lan oylamada 11 ki?i hay?r ve 3 ki?i ?ekimser oy kullanm??t?r. Etkinli?inin belirsiz olmas?, hasta se?im kriterlerinin net olmamas?, ast?m?n a??rl?kl? olarak k???k hava yolu hastal??? olmas?na kar??n termoplasti ile sadece b?y?k hava yollar?n?n etkilenmesi ve maliyetinin ?ok y?ksek olmas? nedeniyle "kuvvetli negatif" olarak ?nerilmi?tir. Devam etmekte olan ?al??ma sonu?lar?n?n yay?nlanmas? termoplastinin ast?m tedavisindeki yerini belirleyecektir.
A?IR ASTIMDA YEN? TEDAV?LER
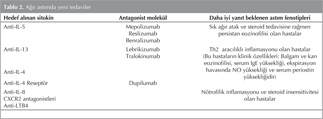
Son y?llarda tedaviye diren?li a??r ast?ml? hastalar?n tedavisinde patogenezde ?nemli roller ?stlenen sitokinler, kemokinler ve mediat?rleri hedef alan ?al??malarda ciddi geli?meler kaydedilmi?tir (Tablo 2). Deneysel ?al??malarda kullan?lan bu biyolojik ajanlar?n ?ok yak?n gelecekte klinik kullan?ma sunulmas? beklenmektedir.
G?n?m?zde tedaviye diren?li a??r ast?ml? hastalar?n tedavisinde kullan?lan biyolojik ajanlar aras?nda en ?ok say?da hastay? kapsayan ve ?al??ma say?s? en y?ksek olan molek?l bir IL-5 antagonisti olan mepolizumabd?r. IL-5, eozinofillerin kemik ili?inde maturasyonuna, bron? mukozas?na g???ne, burada aktive olmas?na ve ya?am s?resinin uzamas?na neden olur. Eozinofilik inflamasyonda rol oynayan en ?nemi sitokin IL-5'tir. Mepolizumab ile yap?lan ilk ?al??malarda balgam ve periferik kan eozinofillerinde ?ok anlaml? d??meler olmas?na kar??n klinik parametrelerde d?zelmelerin olmad??? g?zlenmi?tir (83,84). Daha sonra yap?lan ?al??malarda y?ksek doz inhaler steroid kombinasyon tedavisi ve oral steroide ra?men s?k ata?? ve persistan eozinofilisi olan steroid ba??ml? a??r ast?ml? hastalarda tedaviye mepolizumab eklenmesiyle ataklarda anlaml? azalmalar?n oldu?u g?zlenmi?tir (85,86). ?ok merkezli di?er bir ?al??mada ise s?k ata?? olan eozinofilik ast?ml? hastalarda mepolizumab?n semptomlar, ya?am kalitesi ve solunum fonksiyonlar?nda belirgin bir d?zelme yapmaks?z?n ast?m ataklar?nda anlaml? azalmalara neden oldu?u g?sterilmi?tir (87). Di?er bir IL-5 antagonisti olan reslizumab ile yap?lan bir ?al??mada ya?am kalitesi ve FEV1'de d?zelmeler saptanm??t?r (88). T?m bu ?al??malar?n sonu?lar? y?ksek doz inhaler ya da oral steroid tedavisine ra?men periferik kan ve balgamda eozinofil say?s? y?ksek devam eden (persistan eozinofili) ve s?k ataklar? olan (atak predominant) ast?m fenotipinin anti-IL-5 tedavisi i?in aday hastalar olaca??n? g?stermektedir.
Hedef al?nan di?er iki sitokin ise IL-4 ve IL-13't?r. Her iki sitokin de temel olarak Th2 lenfosit kaynakl?d?r ve IgE yap?m? (atopi) ile remodellingde ?nemli roller oynarlar. Th2 arac?l?kl? inflamasyonun klinik g?stergeleri periferik kan ve balgamda eozinofili olmas?, serum IgE, ekspirayon havas?nda NO ve serum periostin y?ksekli?idir. Bir IL-13 antagonisti olan lebrikizumab ile yap?lan ?al??mada FEV1'de anlaml? art??lar?n oldu?u, serum periostin d?zeyi y?ksek olan hastalarda bu art???n ?ok daha belirgin oldu?u g?sterilmi?tir (89). Di?er bir IL-13 antagonisti olan tralokinumab ?al??mas?nda FEV1'de istatistiksel anlaml? olmayan art??, beta-agonist kullan?m?nda anlaml? azalma sa?lanm??t?r, bu d?zelmeler balgam IL-13 d?zeyi y?ksek olanlarda daha belirgin olmu?tur (90). Bu ?al??malar Th2 arac?l?kl? inflamasyonun rol oynad??? ast?m fenotiplerinde anti-IL-13'?n gelecekte bir tedavi se?ene?i olabilece?ini g?stermektedir.
Y?ksek doz inhaler steroid uzun etkili beta-agonist kombinasyon tedavisi alan, eozinofilik ast?ml? hastalarda bir IL-4 resept?r anagonisti olan dupilumab ile yap?lan 12 haftal?k bir ?al??mada ?ok ?nemli sonu?lar elde edilmi?tir (91). Y?z d?rt hastan?n yar?s?nda ald?klar? tedaviye dupilumab, di?er yar?s?nda ise plasebo eklenmi? ve ?al??man?n d?rd?nc? haftas?nda t?m hastalarda uzun etkili beta-agonist, 6-9. haftalar aras?nda ise inhaler steroid azalt?larak kesilmi? ve 9-12. haftalar aras?nda hastalar?n sadece plasebo veya dupilumab almas? sa?lam??t?r. Her iki grupta 12 hafta boyunca atak oranlar?na bak?ld???nda plasebo grubundaki 52 hastan?n 23'?nde, dupilumab grubunda ise 52 hastan?n 3'?nde atak g?r?lm??t?r. Dupilumab ile atak oranlar?nda %87 azalma saptanm??t?r. Yeni ?al??malar ile bu ilgin? sonu?lar tekrar ara?t?r?lmaktad?r. ?al??malardan olumlu sonu?lar ??kmas? durumunda eozinofilik ast?mda yeni bir tedavi klinik kullan?ma girecektir.
Eozinofilik ast?m fenotiplerinde oldu?u gibi, n?trofilik ast?m fenotiplerinde de n?trofilik inflamasyon mediat?rlerine y?nelik ?al??malar yap?lmaktad?r. N?trofil g???nde rol oynayan kemokinlere kar?? sentez edilen bir antagonist ile a??r ast?ml? hastalarda balgam n?trofil say?lar?nda d???? ve hafif ataklarda k?smi azalmalar saptanm??t?r (92).
Sonu? olarak; tedaviye diren?li ast?m tedavisi g???s hastal?klar? uzmanlar? i?in ?nemli bir sorundur. ?lkemiz ko?ullar?nda bu sorunun ??z?m?nde yard?mc? olabilmek, s?k sorulan sorulara yan?t bulabilmek amac?yla bu yaz? haz?rlanm??t?r.
?IKAR ?ATI?MASI
Bildirilmemi?tir.
KAYNAKLAR
- Sch?nemann HJ, Jaeschke R, Cook DJ, Bria WF, El-Solh AA, Ernst A, et al. An official ATS statement: grading the quality of evidence and strength of recommendations in ATS guidelines and recommendations. Am J Respir Crit Care Med? 2006;174(5):605-14.
- Chung KF , Wenzel SE, Brozek JL, Bush A, Castro M, Sterk PJ, et al. International ERS/ATS guidelines on definition, evaluation and treatment of severe asthma. Eur Respir J? 2014;43(2):343-73.
- Chung KF.? New treatments for severe treatment-resistant asthma: targeting the right patient. Lancet Respir Med 2013;1:84-90.
- Virchow JC Jr, Prasse A, Naya I, Summerton L, Harris A. Zafirlukast improves asthma control in patients receiving high-dose inhaled corticosteroids. Am J Respir Crit Care Med 2000;162(2 Pt 1):578-85.
- Ducharme FM, Lasserson TJ, Cates CJ. Long-acting beta2-agonists versus antileukotrienes as add-on therapy to inhaled corticosteroids for chronic asthma. Cochrane Database Syst Rev 2006(4):CD003137.
- Lemanske RF Jr, Mauger DT, Sorkness CA, Jackson DJ, Boehmer SJ, Martinez FD, et al. Step-up therapy for children with uncontrolled asthma receiving inhaled corticosteroids. N Engl J Med 2010;362(11):975-85.
- Dahl?n B, Nizankowska E, Szczeklik A, Zetterstr?m O, Bochenek G, Kumlin M, et al. Benefits from adding the 5-lipoxygenase inhibitor zileuton to conventional therapy in aspirin-intolerant asthmatics. Am J Respir Crit Care Med 1998;157(4 Pt 1):1187-94.
- Dahl?n SE, Malmstr?m K, Nizankowska E, Dahl?n B, Kuna P, Kowalski M, et al. Improvement of aspirin-intolerant asthma by montelukast, a leukotriene antagonist: a randomized, double-blind, placebo-controlled trial. Am J Respir Crit Care Med 2002;165(1):9-14.
- Evans DJ, Taylor DA, Zetterstrom O, Chung KF, O'Connor BJ, Barnes PJ.? A comparison of low-dose inhaled budesonide plus theophylline and high-dose inhaled budesonide for moderate asthma. N Engl J Med 1997;337(20):1412-8.
- Ukena D, Harnest U, Sakalauskas R, Magyar P, Vetter N, Steffen H, et al. Comparison of addition of theophylline to inhaled steroid with doubling of the dose of inhaled steroid in asthma. Eur Respir J 1997;10(12):2754-60.
- Spears M, Donnelly I, Jolly L, Brannigan M, Ito K, McSharry C, et al. Effect of low-dose theophylline plus beclometasone on lung function in smokers with asthma: a pilot study. Eur Respir J 2009;33(5):1010-7.
- Barnes PJ. Theophylline. Am J Respir Crti Care Med 2013:188;901-6.
- Guyer AC, Long AA. Long-acting anticholinergics in the treatment of asthma. Curr Opin Allergy Immunol 2013; 13:392-98.
- Peters SP, Kunselman SJ, Icitovic N, Moore WC, Pascual R, Ameredes BT, et al. Tiotropium bromide step-up therapy for adults with uncontrolled asthma. N Engl J Med 2010;363(18):1715-26.
- Bateman ED, Kornmann O, Schmidt P, Pivovarova A, Engel M, Fabbri LM. Tiotropium is noninferior to salmeterol in maintaining improved lung function in B16-Arg/Arg patients with asthma. J Allergy Clin Immunol 2011;128(2):315-22.
- Kerstjens HA, Disse B, Schr?der-Babo W, Bantje TA, Gahlemann M, Sigmund R, et al.? Tiotropium improves lung function in patients with severe uncontrolled asthma: a randomized controlled trial. J Allergy Clin Immunol 2011;128(2):308-14.
- Kerstjens HA, Engel M, Dahl R, Paggiaro P, Beck E, Vandewalker M, et al. Tiotropium in asthma poorly controlled with standard combination therapy. N Engl J Med 2012;367(13):1198-207.
- Yoshida M, Nakano T, Fukuyama S, Matsumoto T, Eguchi M, Moriwaki A, et al. Effects of tiotropium on lung function in severe asthmatics with or without emphysematous changes. Pulm Pharmacol Ther? 2013;26(2):159-66.
- Peters SP, Bleecker ER, Kunselman SJ, Icitovic N, Moore WC, Pascual R, et al. Predictors of response to tiotropium versus salmeterol in asthmatic adults. J Allergy Clin Immunol? 2013;132(5):1068-74.
- Tian JW, Chen JW, Chen R, Chen X. Tiotropium versus placebo for inadequately controlled asthma: a meta-analysis. Respir Care? 2013 [Epub ahead of print].
- Rabe KF, Atienza T, Magyar P, Larsson P, Jorup C, Lalloo UG. Effect of budesonide in combination with formoterol for reliever therapy in asthma exacerbations: a randomised controlled, double-blind study. Lancet 2006;368(9537):744-53.
- Rabe KF, Pizzichini E, St?llberg B, Romero S, Balanzat AM, Atienza T, et al. Budesonide/formoterol in a single inhaler for maintenance and relief in mild-to-moderate asthma: a randomized, double-blind trial. Chest 2006;129(2):246-56.
- Scicchitano R, Aalbers R, Ukena D, Manjra A, Fouquert L, Centanni S, et al. Efficacy and safety of budesonide/formoterol single inhaler therapy versus a higher dose of budesonide in moderate to severe asthma. Curr Med Res Opin 2004;20(9):1403-18.
- O'Byrne PM, Bisgaard H, Godard PP, Pistolesi M, Palmqvist M, Zhu Y, et al. Budesonide/formoterol combination therapy as both maintenance and reliever medication in asthma. Am J Respir Crit Care Med 2005;171(2):129-36.
- Kuna P, Peters MJ, Manjra AI, Jorup C, Naya IP, Mart?nez-Jimenez NE, et al. Effect of budesonide/formoterol maintenance and reliever therapy on asthma exacerbations. Int J Clin Pract 2007;61(5):725-36.
-
Bousquet J, Boulet LP, Peters MJ, Magnussen H, Quiralte J, Martinez-Aguilar NE, et al.
Budesonide/formoterol for maintenance and relief in uncontrolled asthma vs.
high-dose salmeterol/fluticasone. Respir Med 2007;101(12):2437-46. - Vogelmeier C, D'Urzo A, Pauwels R, Merino JM, Jaspal M, Boutet S, et al. Budesonide/formoterol maintenance and reliever therapy: an effective asthma treatment option? Eur Respir J 2005;26(5):819-28.
- Papi A, Corradi M, Pigeon-Francisco C, Baronio R, Siergiejko Z, Petruzzelli S, et al. Beclometasone-formoterol as maintenance and reliever treatment in patients with asthma: a double-blind, randomised controlled trial. Lancet Respir Med 2013;1(1):23-31.
- Patel M, Pilcher J, Pritchard A, Perrin K, Travers J, Shaw D, et al. Efficacy and safety of maintenance and reliever combination budesonide-formoterol inhaler in patients with asthma at risk of severe exacerbations: a randomised controlled trial. Lancet Respir Med 2013;1(1):32-42.
- Buhl R, Kuna P, Peters MJ, Andersson TL, Naya IP, Peterson S, et al. The effect of budesonide/formoterol maintenance and reliever therapy on the risk of severe asthma exacerbations following episodes of high reliever use: an exploratory analysis of two randomised, controlled studies with comparisons to standard therapy. Respir Res 2012;20;13:59.
- Holgate S, Casale T, Wenzel S, Bousquet J, Deniz Y, Reisner C. The anti-inflammatory effects of omalizumab confirm the central role of IgE in allergic inflammation.? J Allergy Clin Immunol 2005;115(3):459-65.
- Rodrigo GJ, Neffen H, Castro-Rodriguez JA. Efficacy and safety of subcutaneous omalizumab vs. placebo as add-on therapy to corticosteroids for children and adults with asthma: a systematic review. Chest 2011;139(1):28-35.
- Norman G, Faria R, Paton F, Llewellyn A, Fox D, Palmer S, et al. Omalizumab for the treatment of severe persistent allergic asthma: a systematic review and economic evaluation. Health Technol Assess 2013;17(52):1-342.
- Bousquet J, Cabrera P, Berkman N, Buhl R, Holgate S, Wenzel S, et al. The effect of treatment with omalizumab, an anti-IgE antibody, on asthma exacerbations and emergency medical visits in patients with severe persistent asthma. Allergy 2005;60(3):302-8.
- Molimard M, de Blay F, Didier A, Le Gros V. Effectiveness of omalizumab (Xolair) in the first patients treated in real-life practice in France. Respir Med 2008;102(1):71-6.
- ?zg?r ES, ?zge C, ?lvan A, Nayc? SA Assessment of long-term omalizumab treatment in patients with severe allergic asthma long-term omalizumab treatment in severe asthma. J Asthma. 2013;50(6):687-94.
- Korn S, Thielen A, Seyfried S, Taube C, Kornmann O, Buhl R. Omalizumab in patients with severe persistent allergic asthma in a real-life setting in Germany. Respir Med 2009;103(11):1725-31.
- Storms W, Bowdish MS, Farrar JR. Omalizumab and asthma control in patients with moderate-to-severe allergic asthma: a 6-year pragmatic data review. Allergy Asthma Proc. 2012;33(2):172-7.
- Schumann C, Kropf C, Wibmer T, R?diger S, Stoiber KM, Thielen A, et al. Omalizumab in patients with severe asthma: the XCLUSIVE study. Clin Respir J 2012;6(4):215-27.
- Bousquet J, Siergiejko Z, Swiebocka E, Humbert M, Rabe KF, Smith N, et al. Persistency of response to omalizumab therapy in severe allergic (IgE-mediated) asthma. Allergy 2011;66(5):671-8.
- Hanania NA, Alpan O, Hamilos DL, Condemi JJ, Reyes-Rivera I, Zhu J, et al. Omalizumab in severe allergic asthma inadequately controlled with standard therapy: a randomized trial. Ann Intern Med 2011;154(9):573-82.
- de Llano LP, Vennera Mdel C, ?lvarez FJ, Medina JF, Border?as L, Pellicer C, et al. Effects of omalizumab in non-atopic asthma: results from a Spanish multicenter registry. J Asthma 2013;50(3):296-301.
- Menzella F, Facciolongo N, Piro R, Formisano D, Roggeri A, Simonazzi A, et al. Clinical and pharmacoeconomic aspects of omalizumab: a 4-year follow-up. Ther Adv Respir Dis 2012;6(2):87-95.
- Camargo CA Jr, Weiss ST, Zhang S, Willett WC, Speizer FE. Prospective study of body mass index, weight change, and risk of adult-onset asthma in women. Arch Intern Med 1999; 22;159(21):2582-8.
- Zarga A, Ulrik CS. Obesity and asthma: a coincidence or a causal relationship? A systematic review Respiratory Medicine 2013;1:14.
- Holguin F, Bleecker ER, Busse WW, Calhoun WJ, Castro M, Erzurum SC, et al. Obesity and asthma: an association modified by age of asthma onset. J Allergy Clin Immunol 2011;127(6):1486-93.
- Sideleva O, Black K, Dixon AE. Effects of obesity and weight loss on airway physiology and inflammation in asthma. Pulm Pharmacol Ther 2013;26(4):455-8.
- Dixon AE, Clerisme-Beaty EM, Sugar EA, Cohen RI, Lang JE, Brown ED, et al. Effects of obstructive sleep apnea and gastroesophageal reflux disease on asthma control in obesity. J Asthma 2011;48(7):707-13.
- Chung KF, Wenzel SE, Brozek JL, Bush A, Castro M, Sterk PJ, et al. International ERS/ATS guidelines on definition, evaluation and treatment of severe asthma.? Eur Respir J 2014;43(2):343-73.
- Haldar P, Pavord ID, Shaw DE, Berry MA, Thomas M, Brightling CE, et al. Cluster analysis and clinical asthma phenotypes. Am J Respir Crit Care Med 2008;178(3):218-24.
- Novosad S, Khan S, Wolfe B, Khan A. Role of obesity in asthma control, the Obesity-Asthma Phenotype Journal of Allergy 2013, Article ID 538642.
- Juel CT, Ali Z, Nilas L, Ulrik CS. Asthma and obesity: does weight loss improve asthma control? a systematic review J Asthma Allergy 2012;5:21-6.
- Maniscalco M, Zedda A, Faraone S, Cerbone MR, Cristiano S, Giardiello C, et al. Weight loss and asthma control in severely obese asthmatic females. Respir Med 2008;102(1):102-8.
- Stenius-Aarniala B, Poussa T, Kvarnstr?m J, Gr?nlund EL, Ylikahri M, Mustajoki P. Immediate and long term effects of weight reduction in obese people with asthma: randomised controlled study. BMJ 2000;320(7238):827-32.
- Baruwa P, Sarmah KJ. Obesity and asthma. Lung India 2013;30(1):38-46.
- Reddy RC, Baptist AP, Fan Z, Carlin AM, Birkmeyer NJ. The effects of bariatric surgery on asthma severity. Obes Surg 2011;21(2):200-6.
- Sikka N, Wegienka G, Havstad S, Genaw J, Carlin AM, Zoratti E. Respiratory medication prescriptions before and after bariatric surgery. Ann Allergy Asthma Immunol 2010;104(4):326-30.
- Adeniyi FB ,Young TE. Weight loss interventions for chronic asthma.? Cochrane Database Syst Rev. 2012 Jul 11;7:CD009339
- Moreira A, Bonini M, Garcia-Larsen V, Bonini S, Del Giacco SR, Agache I, et al. Weight loss interventions in asthma: EAACI evidence-based clinical practice guideline (part I). Allergy 2013;68(4):425-39.
- Brusselle GG, Joos G. Is there a role for macrolides in severe asthma? Curr Opin Pulm Med 2014; 20: 95-102.
- Reiter J, Demirel N, Mendy A, Gasana J, Vieira ER, Colin AA, et al. Macrolides for the long-term management of asthma--a meta-analysis of randomized clinical trials. Allergy 2013;68(8):1040-9.
- Simpson JL, Powell H, Boyle MJ, Scott RJ, Gibson PG. Clarithromycin targets neutrophilic airway inflammation in refractory asthma. Am J Respir Crit Care Med 2008;177(2):148-55.
- Hahn DL, Grasmick M, Hetzel S, Yale S; AZMATICS (AZithroMycin-Asthma Trial In Community Settings) Study Group. Azithromycin for bronchial asthma in adults: an effectiveness trial. J Am Board Fam Med 2012;25(4):442-59.
- Brusselle GG, Vanderstichele C, Jordens P, Deman R, Slabbynck H, Ringoet V, et al. Azithromycin for prevention of exacerbations in severe asthma (AZISAST): a multicentre randomised double-blind placebo-controlled trial. Thorax 2013 Apr;68(4):322-9.
- Thomas PS, Yates DH, Barnes PJ. Tumor necrosis factor-alpha increases airway responsiveness and sputum neutrophilia in normal human subjects. Am J Respir Crit Care Med 1995;152:76-80.
- Ying S, Robinson DS, Varney V, Meng Q, Tsicopoulos A, Moqbel R, et al. TNF-alpha mRNA expression in allergic inflammation. Clin Exp Allergy 1991;21(6):745-50.
- Howarth PH, Babu KS, Arshad HS, Lau L, Buckley M, McConnell W, et al. Tumour necrosis factor (TNFalpha) as a novel therapeutic target in symptomatic corticosteroid dependent asthma. Thorax 2005 Dec;60(12):1012-8.
- Berry MA, Hargadon B, Shelley M, Parker D, Shaw DE, Green RH, et al. Evidence of a role of tumor necrosis factor alpha in refractory asthma. N Engl J Med 2006;354(7):697-708.
- Morjaria JB, Chauhan AJ, Babu KS, Polosa R, Davies DE, Holgate ST. The role of a soluble TNFalpha receptor fusion protein (etanercept) in corticosteroid refractory asthma: a double blind, randomised, placebo controlled trial. Thorax? 2008;63(7):584-91.
- Holgate ST, Noonan M, Chanez P, Busse W, Dupont L, Pavord I, et al. Efficacy and safety of etanercept in moderate-to-severe asthma: a randomised, controlled trial. Eur Respir J 2011;37(6):1352-9.
- Wenzel SE, Barnes PJ, Bleecker ER, Bousquet J, Busse W, Dahl?n SE, et al. A randomized, double-blind, placebo-controlled study of tumor necrosis factor-alpha blockade in severe persistent asthma. Am J Respir Crit Care Med 2009;179(7):549-58.
- James AL, Elliot JG, Jones RL, Carroll ML, Mauad T, Bai TR, et al. Airway smooth muscle hypertrophy and hyperplasia in asthma. Am J Respir Crit Care Med? 2012;185(10):1058-64.
- Danek CJ, Lombard CM, Dungworth DL, Cox PG, Miller JD, Biggs MJ, et al. Reduction in airway hyperresponsiveness to methacholine by the application of RF energy in dogs. J Appl Physiol (1985) 2004;97(5):1946-53.
- Miller JD, Cox G, Vincic L, Lombard CM, Loomas BE, Danek CJ. A prospective feasibility study of bronchial thermoplasty in the human airway. Chest 2005;127(6):1999-2006.
- Cox G, Miller JD, McWilliams A, Fitzgerald JM, Lam S. Bronchial thermoplasty for asthma. Am J Respir Crit Care Med 2006;173(9):965-9.
- Cox G, Thomson NC, Rubin AS, Niven RM, Corris PA, Siersted HC, et al.; AIR Trial Study Group. Asthma control during the year after bronchial thermoplasty. N Engl J Med 2007;356(13):1327-37.
- Pavord ID, Cox G, Thomson NC, Rubin AS, Corris PA, Niven RM, et al.; RISA Trial Study Group. Safety and efficacy of bronchial thermoplasty in symptomatic, severe asthma. Am J Respir Crit Care Med 2007;176(12):1185-91.
- Castro M, Rubin AS, Laviolette M, Fiterman J, De Andrade Lima M, Shah PL, et al.; AIR2 Trial Study Group. Effectiveness and safety of bronchial thermoplasty in the treatment of severe asthma: a multicenter, randomized, double-blind, sham-controlled clinical trial. Am J Respir Crit Care Med? 2010;181(2):116-24.
- Thomson NC, Rubin AS, Niven RM, Corris PA, Siersted HC, Olivenstein R, et al.; AIR Trial Study Group. Long-term (5 year) safety of bronchial thermoplasty: Asthma Intervention Research (AIR) trial. BMC Pulm Med? 2011;11:8.
- Wechsler ME, Laviolette M, Rubin AS, Fiterman J, Lapa e Silva JR, Shah PL, et al.; Asthma Intervention Research 2 Trial Study Group. Bronchial thermoplasty: Long-term safety and effectiveness in patients with severe persistent asthma. J Allergy Clin Immunol? 2013;132(6):1295-302.
- Wahidi MM, Kraft M. Bronchial thermoplasty for severe asthma. Am J Respir Crit Care Med 2012:185(1):709-14.
- Sheshadri A, Castro M, Chen A. Bronchial thermoplasty: a novel therapy for severe asthma. Clin Chest Med 2013; 34:437-44.
- Leckie MJ, ten Brinke A, Khan J, Diamant Z, O'Connor BJ, Walls CM, et al. Effects of an interleukin-5 blocking monoclonal antibody on eosinophils, airway hyper-responsiveness, and the late asthmatic response. Lancet? 2000;356(9248):2144-8.
- Flood-Page P, Swenson C, Faiferman I, Matthews J, Williams M, Brannick L, et al.; International Mepolizumab Study Group. A study to evaluate safety and efficacy of mepolizumab in patients with moderate persistent asthma. Am J Respir Crit Care Med? 2007;176(11):1062-71.
- Haldar P, Brightling CE, Hargadon B, Gupta S, Monteiro W, Sousa A, et al. Mepolizumab and exacerbations of refractory eosinophilic asthma. N Engl J Med? 2009;360(10):973-84.
- Nair P, Pizzichini MM, Kjarsgaard M, Inman MD, Efthimiadis A, Pizzichini E, et al. Mepolizumab for prednisone-dependent asthma with sputum eosinophilia. N Engl J Med 2009;360(10):985-93.
- Pavord ID, Korn S, Howarth P, Bleecker ER, Buhl R, Keene ON, et al. Mepolizumab for severe eosinophilic asthma (DREAM): a multicentre, double-blind, placebo-controlled trial. Lancet? 2012;380(9842):651-9.
- Castro M, Mathur S, Hargreave F, Boulet LP, Xie F, Young J, et al.; Res-5-0010 Study Group. Reslizumab for poorly controlled, eosinophilic asthma: a randomized, placebo-controlled study. Am J Respir Crit Care Med? 2011;184(10):1125-32.
- Corren J, Lemanske RF, Hanania NA, Korenblat PE, Parsey MV, Arron JR, et al. Lebrikizumab treatment in adults with asthma. N Engl J Med? 2011;365(12):1088-98.
- Piper E, Brightling C, Niven R, Oh C, Faggioni R, Poon K, et al. A phase II placebo-controlled study of tralokinumab in moderate-to-severe asthma. Eur Respir J? 2013;41(2):330-8.
- Wenzel S, Ford L, Pearlman D, Spector S, Sher L, Skobieranda F, et al. Dupilumab in persistent asthma with elevated eosinophil levels. N Engl J Med 2013;368(26):2455-66.
- Nair P, Gaga M, Zervas E, Alagha K, Hargreave FE, O'Byrne PM, et al.; Study Investigators. Safety and efficacy of a CXCR2 antagonist in patients with severe asthma and sputum neutrophils: a randomized, placebo-controlled clinical trial. Clin Exp Allergy? 2012;42(7):1097-103.
Yaz??ma Adresi (Address for Correspondence)
Dr. Haluk T?RKTA?
Gazi ?niversitesi T?p Fak?ltesi,
G???s Hastal?klar? Anabilim Dal?,?
Be?evler, ANKARA-TURKEY
e-mail: halukturktas@gmail.com